
- 2022淄博高二下学期期末政治试卷 试卷 0 次下载
- 2022淄博高二下学期期末历史试题 试卷 0 次下载
- 2022淄博高二下学期期末地理试题含解析 试卷 1 次下载
- 2022淄博高二(下)期末物理试题含解析 试卷 0 次下载
- 2022淄博高二下学期期末生物试题 试卷 0 次下载
2022淄博高二下学期期末化学试题
展开注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量: H1 C12 O16
一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符合题意。
1.化学与生活、科技、社会发展息息相关。下列有关说法错误的是
A.为防止食用油变质,可向其中加入叔丁基对苯二酚作抗氧化剂
B.冠醚可识别碱金属离子,冠醚与碱金属离子之间形成的配位键属于离子键
C.我国率先研制了预防新冠病毒的灭活疫苗,灭活疫苗利用了蛋白质变性原理
D.以Si3N4为基础,用Al、O取代部分Si、N获得的陶瓷用于制作LED发光材料
2.某有机物常用于生产聚酯纤维和树脂,是一种重要化工合成原料,使用现代仪器对该有机物的结构进行测定,相关谱图如下。下列有关说法错误的是
A.由质谱图可知该有机物相对分子质量为91
B.由核磁共振氢谱可知该有机物中有2种不同化学环境的氢原子
C.由红外光谱可获得该有机物化学键或官能团信息
D.综合以上信息可知该有机物为对二甲苯
3.工业上用甲苯生产对甲苯酚的过程如下。下列说法错误的是
A.①②均为取代反应
B.反应①可用FeCl3作催化剂
C.甲苯发生硝化反应时,产物以间硝基甲苯为主
D.对甲苯酚含苯环的同分异构体共有4种
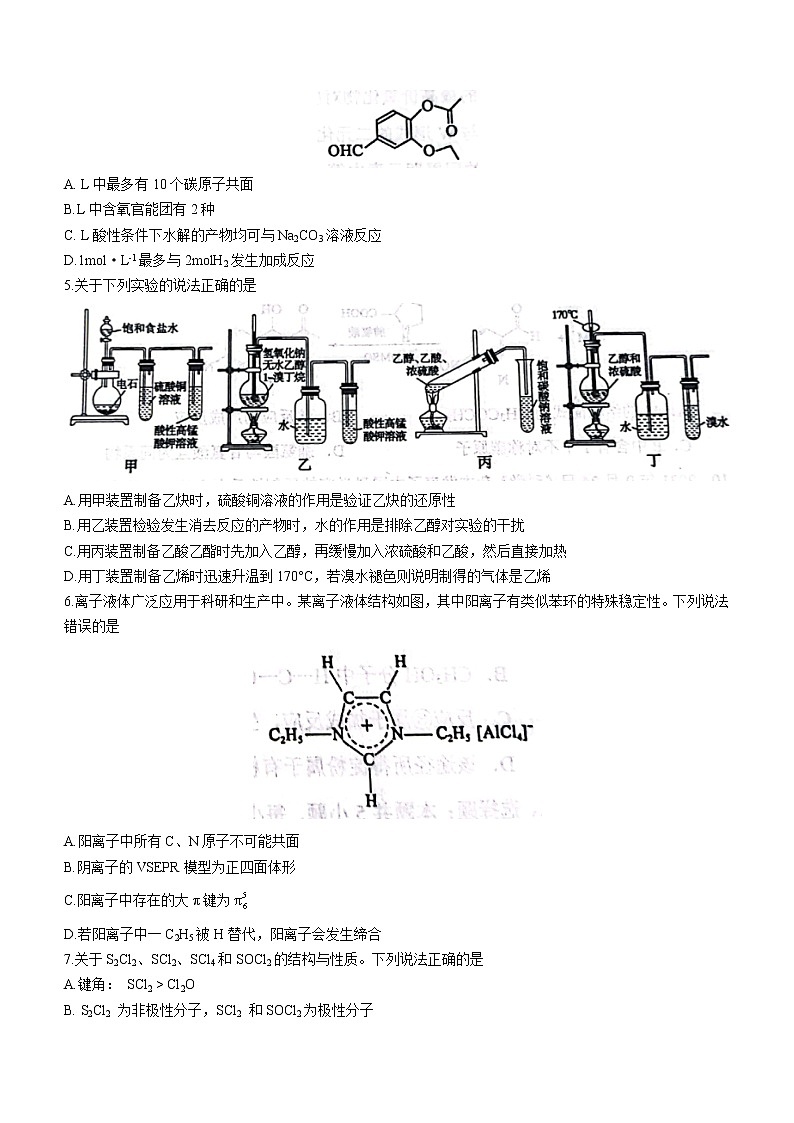
4.化合物L可用作日化香精的定香剂,其结构如图所示。下列说法正确的是
A. L中最多有10个碳原子共面
B.L中含氧官能团有2种
C. L酸性条件下水解的产物均可与Na2CO3溶液反应
D.1ml·L-1最多与2mlH2发生加成反应
5.关于下列实验的说法正确的是
A.用甲装置制备乙炔时,硫酸铜溶液的作用是验证乙炔的还原性
B.用乙装置检验发生消去反应的产物时,水的作用是排除乙醇对实验的干扰
C.用丙装置制备乙酸乙酯时先加入乙醇,再缓慢加入浓硫酸和乙酸,然后直接加热
D.用丁装置制备乙烯时迅速升温到170°C,若溴水褪色则说明制得的气体是乙烯
6.离子液体广泛应用于科研和生产中。某离子液体结构如图,其中阳离子有类似苯环的特殊稳定性。下列说法错误的是
A.阳离子中所有C、N原子不可能共面
B.阴离子的VSEPR模型为正四面体形
C.阳离子中存在的大π键为
D.若阳离子中一C2H5被H替代,阳离子会发生缔合
7.关于S2Cl2、SCl2、SCl4和SOCl2的结构与性质。下列说法正确的是
A.键角: SCl2 > Cl2O
B. S2Cl2 为非极性分子,SCl2 和SOCl2为极性分子
C. S2Cl2、SCl2、SCl4、SOCl2中S原子的杂化方式均为sp3
D. S2Cl2、SCl2、SCl4、SOCl2 与水反应均能产生HCl
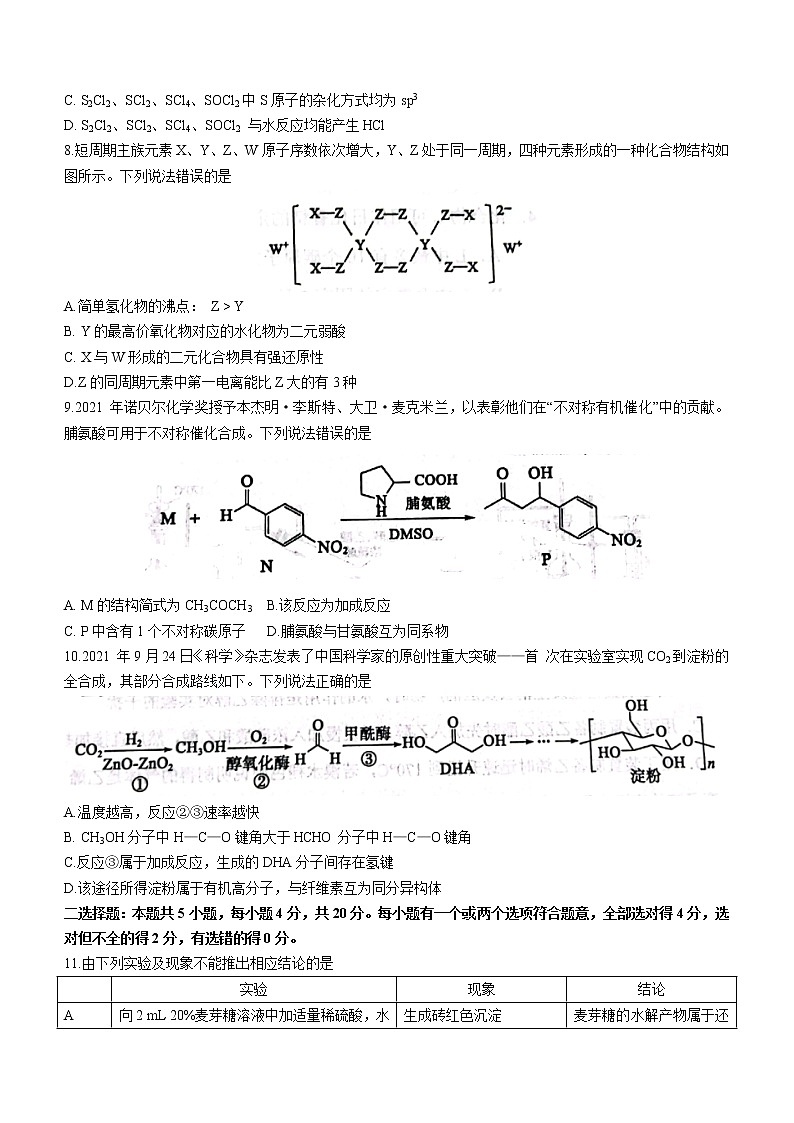
8.短周期主族元素X、Y、Z、W原子序数依次增大,Y、Z处于同一周期,四种元素形成的一种化合物结构如图所示。下列说法错误的是
A.简单氢化物的沸点: Z > Y
B. Y的最高价氧化物对应的水化物为二元弱酸
C. X与W形成的二元化合物具有强还原性
D.Z的同周期元素中第一电离能比Z大的有3种
9.2021 年诺贝尔化学奖授予本杰明·李斯特、大卫·麦克米兰,以表彰他们在“不对称有机催化”中的贡献。脯氨酸可用于不对称催化合成。下列说法错误的是
A. M的结构简式为CH3COCH3 B.该反应为加成反应
C. P中含有1个不对称碳原子 D.脯氨酸与甘氨酸互为同系物
10.2021 年9月24日《科学》杂志发表了中国科学家的原创性重大突破——首 次在实验室实现CO2到淀粉的全合成,其部分合成路线如下。下列说法正确的是
A.温度越高,反应②③速率越快
B. CH3OH分子中H—C—O键角大于HCHO分子中H—C—O键角
C.反应③属于加成反应,生成的DHA分子间存在氢键
D.该途径所得淀粉属于有机高分子,与纤维素互为同分异构体
二选择题:本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题意,全部选对得4分,选对但不全的得2分,有选错的得0分。
11.由下列实验及现象不能推出相应结论的是
12.聚乙烯亚胺捕获CO2并原位氢化为甲醇,反应力程如图所示。下列叙述错误的是
A.聚乙烯亚胺的链节为一NH—CH2— CH2—
B.第1步反应为加成反应
C.总反应为CO2 +3H2CH3OH+ H2O
D.右图涉及的物质中C原子杂化方式有2种
13.己二烯一定条件下可发生闭环反应。下列说法错误的是
A.X分子中σ键与π键的个数比为13:2
B. Y、Z互为对映异构体
C. X被酸性KMnO4溶液氧化生成HOOC — COOH和CH3COOH
D.一定条件下X与乙烯反应生成的六元环状化合物中不含手性碳原子
14.以Li2O晶胞的某一顶点为原点建立坐标系,沿x 、y、 z轴的晶胞投影均如图所示。下列说法错误的是
A.熔点: Li2O> Na2O> K2O
B. Li2O晶体中, O2-的配位数为6
C. Li2O 晶体中,与O2-等距且最近的O2-个数为12
D.若Li2O的晶胞参数为a nm,则Li+与O2-的最近距离为anm
15.制备某杀虫剂中间体的合成路线如下:
已知: Ar-H- Ar-R (Ar为芳基)
下列说法正确的是
A. Q中最多有14个原子共面
B. R能发生加成、取代、消去反应
C. S完全氢化后的产物中有5个手性碳原子
D. Q→R与R→S的反应类型相同
三、非选择题:本题共5小题,共60分。
16. (10分)某聚碳酸酯 可制作车、船、飞机的挡
风玻璃,以及眼镜镜片、光盘、唱片等;其单体为双酚A和一种酯。回答下列问题: .
(1)该聚酯两种单体的结构简式分别为 、 , 由以上两种单体制备该聚
酯的反应类型为_ 。
(2)双酚A中有 种不同化学环境的氢原子,双酚A苯环上的二氯代物有 种。
(3)双酚A可由X、Y两种有机物在催化剂作用下缩合而成,该反应的化学方程式为_ 。
17. (12分)第VIII族元素(Fe、 C、Ni等)在生产、生活中用途广泛。
回答下列问题:
(1)第四周期基态原子与基态Ni3+未成对电子数相同的元素有 种。
(2)邻二氮菲(phen, 结构如图)能通过N原子与Fe2+形成稳定的配合物[Fe(phen)3]2+,该配合物的特征颜色可用于测定Fe2+的浓度。[Fe(phen)3]2+中 Fe2+的配位数为___ _;实验表明, 邻二氮菲检验Fe2+的适宜pH范围是2~9,其原因是 。
(3)草酸亚铁是生产磷酸铁锂动力电池的原料,可由草酸与硫酸亚铁铵反应制得。草酸与甲酸酸性相对强弱:草酸_ 甲酸(填“>”“<”或“=”),其原因是 。
(4) Fe3O4晶胞具有反尖晶石结构,氧离子和不同价态铁离子构成A、B两种结构,如图所示,其晶胞可以看作是由4个A型和4个B型小单元交替并置而成。
①Fe3+填充在O2-围成的_ 空隙处 (填“正四面体” 或“正八面体”)。
②纳米材料的量子尺寸效应可以显著改变材料电磁性能,材料表面原子(或离子)占总原子(或离子)数的比例是重要的影响因素。假设某Fe3O4纳米颗粒恰好是一个Fe3O4晶胞,该颗粒表面离子与总离子数的最简整数比为. __ 。
18. (12 分)化合物G可用作增塑剂,其合成路线如下:
已知: I.
II.
回答下列问题: .
(1) A、E的结构简式分别为_ 、 。
(2) B的名称为_ ____ ; B→C的反应类型为 。
(3) F→G的反应方程式为_ 。
(4)符合下列条件的F的同分异构体有 种(不考虑立体异构)。.
a.属于芳香族化合物
b.能与NaHCO3溶液反应放出CO2
c.核磁共振氢谱为4组峰,峰面积比为3:2:1:1
(5)写出以甲苯为原料制备的合成路线。
19. (14 分)乙酰水杨酸( ) ,俗名阿司匹林,是世界上应用最广泛的解热、镇痛和抗炎药,其实验室制备流程如下:
步骤I的具体操作为:向125 mL锥形瓶中加入2.07 g水杨酸、5 mL乙酸酐和5滴浓硫酸,充分摇动使其完全溶解,装上回流冷凝管,控制加热温度80-85°C,充分反应。稍冷却再边搅拌边加入50 mL冷水,置冰水中冷却,使晶体完全析出,抽滤、洗涤。
已知: I. 水杨酸分子间能发生缩合反应,所得聚合物不溶于饱和NaHCO3溶液;
II.部分物质性质数据如表:
回答下列问题:
(1)制备乙酰水杨酸的化学方程式为_ ____,反应中浓硫酸的作用为 。
(2)冷凝回流时,适合的加热方式为__ __;步骤 I中洗涤时最好选择的洗涤剂为_
A.乙醇 B. NaOH溶液 C.冷水 D.滤液
(3)向粗产品中加入饱和NaHCO3溶液的目的是___ _ , “抽滤”操作相对于普通
过滤的优点是_ 。
(4)为检验所获得的产品中是否含有水杨酸,可使用的试剂为_ ,为得到更纯的产品,应采取的操作名称为_ 。
(5)最后所得纯品的质量为1.51g,则本实验的产率为_ _%。
20. (12 分)化合物G是合成抗炎、镇痛药洛索洛芬钠的中间体,其合成路线如下:
已知: I. NBS是良好的α位溴代试剂;
II. (X=Cl, Br)
回答下列问题:
(1) A的结构简式为___ ; B→C的反应类型为_ 。
(2) C中官能团的名称为_ ___ 。
(3)反应F→G的化学方程式为_ 。
(4)符合下列条件的E的同分异构体有 种 (不考虑立体异构)。
a.属于酯类
b.苯环上有2个取代基
X是E的同分异构体,其在酸性条件下水解,生成的2种化合物核磁共振氢谱都显示4组峰,其中一种遇FeC13溶液显紫色。X水解产物的结构简式为_ 。
(5)写出由制备的合成路线。
实验
现象
结论
A
向2 mL 20%麦芽糖溶液中加适量稀硫酸,水
浴加热5min,冷却后先加足量NaOH溶液,
再加适量新制Cu(OH)2悬浊液并加热煮沸
生成砖红色沉淀
麦芽糖的水解产物属于还原糖
B
向溴的CCl4溶液中加入分子式为C6H12的某有机物
溶液褪色
该有机物中含有碳碳
双键。
C
向CuSO4溶液中加入过量氨水,并振荡
最终得到深蓝色
溶液
与Cu2+的配位能力:NH3 > H2O
D
向2mL某卤代烃样品中加入5mL20%KOH
溶液,振荡后加热,加稀硝酸酸化,再加入
AgNO3溶液
生成白色沉淀
该卤代烃含氯元素
名称
密度/(g·cm-3)
相对分子质量
熔点/°C
水中溶解性
乙醇中溶解性
水杨酸
1.44
138
157~159
溶
易溶
乙酸酐
1.10
102
-73.1
易溶
溶
乙酰水杨酸
1.35
180
135
冷水微溶,热水可溶
易溶
2023淄博高二上学期期末考试化学试题扫描版无答案: 这是一份2023淄博高二上学期期末考试化学试题扫描版无答案,共8页。
山东省淄博市2022-2023学年高二下学期期末考试化学试题: 这是一份山东省淄博市2022-2023学年高二下学期期末考试化学试题,共4页。
2022淄博高二下学期期中考试化学试题含解析: 这是一份2022淄博高二下学期期中考试化学试题含解析,文件包含山东省淄博市2021-2022学年高二下学期期中考试化学试题解析版docx、山东省淄博市2021-2022学年高二下学期期中考试化学试题原卷版docx等2份试卷配套教学资源,其中试卷共33页, 欢迎下载使用。












