

陕西省各市五年(2018-2022)中考化学真题分题型分层汇编-05填空题&计算题
展开陕西省各市五年(2018-2022)中考化学真题分题型分层汇编
05填空题&计算题
一.固体溶解度曲线及其作用(共1小题)
1.(2018•陕西)如图是甲、乙两种固体物质的溶解度曲线,回答问题。
(1)t1℃时,甲、乙物质的溶解度大小关系是 。
(2)t2℃时,要使一定质量的乙固体快速溶解在一定质量的水中,可采用的方法是 (填一种)。
(3)P点表示t3℃时甲物质溶液的某种状态,若使其由该状态变成甲物质曲线上某点的状态,可采用的方法是 (填一种)。
(4)t3℃时,将等质量的甲、乙的饱和溶液降温至t2℃,关于所得溶液的说法不正确的是 (填序号)。
①溶液中溶质质量分数相等 ②所含溶剂质量相等 ③所含溶质质量不相等
二.金属的化学性质(共2小题)
2.(2018•陕西)铝、铁、铜是生活中常见的金属,回答问题。
(1)铝在空气中具有很好的抗腐蚀性的原因是 。
(2)切割钢板时,常用硫酸铜溶液画线即可留下红色印迹,此过程中发生反应的化学方程式是 。
(3)自然界中的金属资源是有限的,写出一条保护金属资源的途径 。
3.(2018•陕西)人类文明进步与金属材料发展关系十分密切。
(1)铝合金被广泛应用于制造飞机、高铁等这是因为铝合金具有 、质量轻、耐腐蚀等特性。
(2)化学兴趣小组为了鉴别某黄色金属是黄金还是黄铜(铜锌合金),设计了如下方案:
①取样,在空气中加热②取样加入硝酸银溶液③取样,加入硫酸锌溶液
其中不合理的是 (填序号)。某同学提出还可以用稀硫酸鉴别他所依据的反应原理是 (用化学方程式表示)。
三.微粒观点及模型图的应用(共1小题)
4.(2018•陕西)合理使用化肥可提高农作物产量。如图是生产尿素的微观示意图,回答问题。
(1)A物质中氮元素的化合价是 。D物质的化学式是 。
(2)下列与尿素不属于同类肥料的是 。
A.NH4HCO3 B.NH4Cl C.K2SO4
四.化学符号及其周围数字的意义(共1小题)
5.(2020•陕西)含义丰富的化学符号是独特的化学语言。根据以下符号回答:
①2N2 ②Al3+ ③2H ④SO42﹣ ⑤CH4
(1)能表示宏观物质的是 (填序号)。
(2)①表示两个 。
(3)由②和④构成的物质的化学式为 。
(4)⑤中数字“4”的含义是 。
五.复分解反应的条件与实质(共1小题)
6.(2018•陕西)化学是研究物质的组成、结构、性质及变化规律的科学。
(1)下列符号能表示2个原子的是 (填序号)。
①2N ②2CO ③Mg2+ ④
(2)如图是碳酸钠溶液与氢氧化钙溶液发生反应的微观示意图。
该反应可观察到的现象是 ,反应的微观本质是 。
六.根据化学反应方程式的计算(共8小题)
7.(2022•陕西)学习小组同学为测定某品牌钙片中含碳酸钙的质量分数,向盛有10g钙片的烧杯中加入过量稀盐酸,充分反应后,测得烧杯内混合物的总质量比反应前稀盐酸与钙片的总质量减少了3.3g。(钙片中其他成分不与稀盐酸反应放出气体)
(1)反应中生成二氧化碳的质量是 g。
(2)计算该品牌钙片中含碳酸钙的质量分数。
8.(2021•陕西)学习小组的同学想测定某种大理石中碳酸钙的质量分数。取大理石样品25g,逐渐缓慢向其中加入150g溶质质量分数为14.6%的稀盐酸(杂质难溶于水,且不与酸反应),测得剩余固体的质量与加入稀盐酸的质量关系如图所示。完成下列分析与计算:
(1)恰好完全反应时消耗稀盐酸的质量是 g。
(2)计算该大理石中碳酸钙的质量分数。
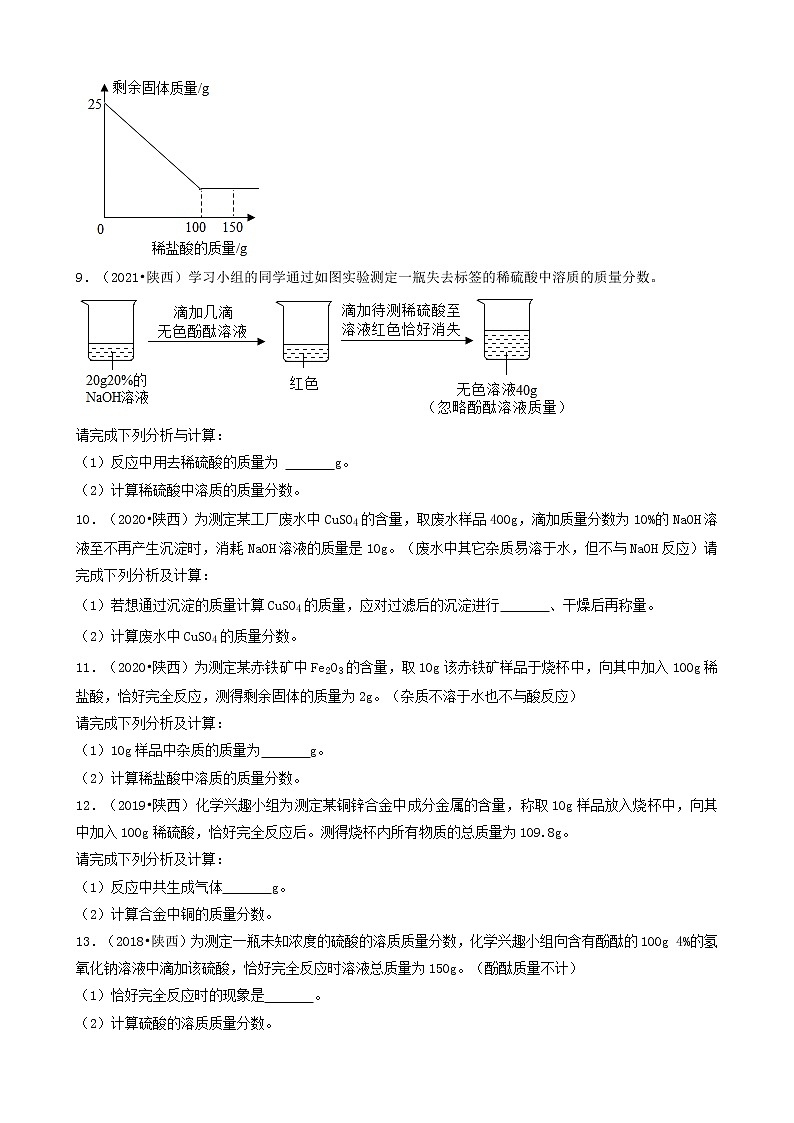
9.(2021•陕西)学习小组的同学通过如图实验测定一瓶失去标签的稀硫酸中溶质的质量分数。
请完成下列分析与计算:
(1)反应中用去稀硫酸的质量为 g。
(2)计算稀硫酸中溶质的质量分数。
10.(2020•陕西)为测定某工厂废水中CuSO4的含量,取废水样品400g,滴加质量分数为10%的NaOH溶液至不再产生沉淀时,消耗NaOH溶液的质量是10g。(废水中其它杂质易溶于水,但不与NaOH反应)请完成下列分析及计算:
(1)若想通过沉淀的质量计算CuSO4的质量,应对过滤后的沉淀进行 、干燥后再称量。
(2)计算废水中CuSO4的质量分数。
11.(2020•陕西)为测定某赤铁矿中Fe2O3的含量,取10g该赤铁矿样品于烧杯中,向其中加入100g稀盐酸,恰好完全反应,测得剩余固体的质量为2g。(杂质不溶于水也不与酸反应)
请完成下列分析及计算:
(1)10g样品中杂质的质量为 g。
(2)计算稀盐酸中溶质的质量分数。
12.(2019•陕西)化学兴趣小组为测定某铜锌合金中成分金属的含量,称取10g样品放入烧杯中,向其中加入100g稀硫酸,恰好完全反应后。测得烧杯内所有物质的总质量为109.8g。
请完成下列分析及计算:
(1)反应中共生成气体 g。
(2)计算合金中铜的质量分数。
13.(2018•陕西)为测定一瓶未知浓度的硫酸的溶质质量分数,化学兴趣小组向含有酚酞的100g 4%的氢氧化钠溶液中滴加该硫酸,恰好完全反应时溶液总质量为150g。(酚酞质量不计)
(1)恰好完全反应时的现象是 。
(2)计算硫酸的溶质质量分数。
14.(2018•陕西)某补钙剂的主要成分是碳酸钙。欲测定该补钙剂中碳酸钙的质量分数,某同学进行了如图所示的操作(假设其它成分可溶于水但不参与反应)。
(1)该实验中,装置的气密性对测定结果 (填“有”或“无”)影响。
(2)计算该补钙剂中碳酸钙的质量分数。
七.合成材料的使用及其对人和环境的影响(共1小题)
15.(2020•陕西)在抗击“新冠肺炎”疫情的战斗中,人们采取了一系列行之有效的防控措施。
(1)口罩是防疫的必备品,其生产原料中用到的聚丙烯属于 (填“无机非金属材料”或“有机合成材料”)。
(2)洗手、消毒能有效防止病毒感染。“84”消毒液能迅速杀菌消毒,其有效成分NaClO中氯元素的化合价为 。
(3)测量体温是防控的重要环节。家庭常备体温计中的液态物质是 。
(4)加强营养有利于增强体质,合理补充维生素能提高人体免疫力。下列食品中富含维生素的是 (填字母)。
A.鸡肉
B.黄瓜
C.面包
八.有机高分子材料的分类及鉴别(共1小题)
16.(2020•陕西)2020年6月1日起,公安部交管局在全国开展“一盔一带”安全守护行动。
(1)骑摩托车必须佩戴头盔。头盔某些部件连接处的铁质铆钉表面常进行电镀处理,其目的是 ,同时兼顾美观。
(2)汽车行驶中必须使用安全带。安全带一般用尼龙制成,尼龙属于 (填“天然纤维”或“合成纤维”)。汽车安全气囊被触发时,气囊中的叠氮化钠(NaN3)会瞬间分解,产生一种空气中最多的气体,其化学式是 。
(3)汽车和摩托车尾气中通常含有CO2、CO、NO、NO2等气体,其中不属于大气污染物的是 。
九.棉纤维、羊毛纤维和合成纤维的鉴别(共1小题)
17.(2018•陕西)中国的许多用具独具一格,既表现了中华民族不同于其他民族的风俗,又为世界文化的进步和发展作出了贡献,其中典型的有被誉为“文房四宝”的笔、墨、纸、砚。
(1)制作毛笔“笔毫”的原料之一是白羊毛,生活中可用 法将其与合成纤维区分开。
(2)古代文人用墨作的字画可以保存至今而不褪色的原因是 。
(3)砚台是“文房四宝”之首,以石砚居多。制作石砚的过程发生了 (填“物理”或“化学”)变化。
一十.食品、药品与健康食品中的有机营养素(共2小题)
18.(2019•陕西)陕西名小吃肉丸糊辣汤的制作原料有:牛肉、淀粉、土豆、胡萝卜、豆角及调料等。
(1)上述原料中富含蛋白质的是 。
(2)淀粉溶液遇碘水能变蓝色,这是淀粉的 (填“物理”“化学”)性质。
(3)在远处就能闻到胡辣汤的香味,说明分子 。
19.(2018•陕西)橄榄油营养丰富、滋润度高、在餐饮、美容及制皂领域越来越受到大家的青睐。
(1)橄榄油中富含的主要营养素是 。
(2)工厂可用活性炭对初榨橄榄油进行脱色处理,这是利用了活性炭的 性。
(3)用橄榄油制成的肥皂在洗涤油污的过程中起 作用。
一十一.鉴别淀粉、葡萄糖的方法与蛋白质的性质(共1小题)
20.(2020•陕西)文房四宝“笔、墨、纸、砚”承载着优秀的中华传统文化。
(1)制作毛笔常用羊毛、兔毛等,检验笔毛是动物毛发的简易方法是 。
(2)用墨汁写绘的字画能从古代保存至今而不褪色,是因为常温下碳的化学性质很 (填“稳定”或“不稳定”)。
(3)宣纸制作过程中,有道工序是从纸浆中用竹帘捞纸,该操作相当于 (填字母)。
A.蒸发
B.过滤
C.结晶
(4)砚台产地不同,成分也有差别,但其中的主要成分都 (填“易溶”或“难溶”)于水。
参考答案与试题解析
一.固体溶解度曲线及其作用(共1小题)
1.(2018•陕西)如图是甲、乙两种固体物质的溶解度曲线,回答问题。
(1)t1℃时,甲、乙物质的溶解度大小关系是 甲<乙 。
(2)t2℃时,要使一定质量的乙固体快速溶解在一定质量的水中,可采用的方法是 搅拌 (填一种)。
(3)P点表示t3℃时甲物质溶液的某种状态,若使其由该状态变成甲物质曲线上某点的状态,可采用的方法是 增加溶质 (填一种)。
(4)t3℃时,将等质量的甲、乙的饱和溶液降温至t2℃,关于所得溶液的说法不正确的是 ② (填序号)。
①溶液中溶质质量分数相等 ②所含溶剂质量相等 ③所含溶质质量不相等
【解答】解:(1)通过分析溶解度曲线可知,t1℃时,甲、乙物质的溶解度大小关系是:甲<乙;
(2)t2℃时,要使一定质量的乙固体快速溶解在一定质量的水中,可采用的方法是:搅拌;
(3)P点表示t3℃时甲物质的不饱和溶液,若使其由该状态变成甲物质曲线上某点的状态,变成饱和溶液,可采用的方法是:增加溶质;
(4)t3℃时,将等质量的甲、乙的饱和溶液降温至t2℃,溶解度都减小,都会析出晶体,溶解度相等,
①溶液中溶质质量分数相等,故①正确;
②t3℃时,甲、乙物质的溶解度不相等,等质量的甲、乙的饱和溶液中含有的溶质质量不相等,所含溶剂质量也不相等,故②错误;
③由②的推导可知,所含溶质质量不相等,故③正确。
故选:②。
故答案为:(1)甲<乙;
(2)搅拌;
(3)增加溶质;
(4)②。
二.金属的化学性质(共2小题)
2.(2018•陕西)铝、铁、铜是生活中常见的金属,回答问题。
(1)铝在空气中具有很好的抗腐蚀性的原因是 铝在空气中能与氧气反应,其表面生成一层致密的氧化铝薄膜,防止内部的铝进一步被氧化 。
(2)切割钢板时,常用硫酸铜溶液画线即可留下红色印迹,此过程中发生反应的化学方程式是 Fe+CuSO4═FeSO4+Cu 。
(3)自然界中的金属资源是有限的,写出一条保护金属资源的途径 防止金属腐蚀(或回收利用废旧金属,有计划、合理地开采矿物,回收利用废旧金属等)。 。
【解答】解:(1)铝在空气中能与氧气反应,其表面生成一层致密的氧化铝薄膜,防止内部的铝进一步被氧化,因此铝制品抗腐蚀性强。
(2)铁能与硫酸铜反应生成硫酸亚铁和铜,反应的化学方程式为Fe+CuSO4═FeSO4+Cu。
(3)保护金属资源的有效途径有:防止金属锈蚀,由于金属锈蚀而浪费的金属约占,要想方设法防止金属腐蚀;回收利用废旧金属可节约原料、节省能源,是一种保护金属资源的有效途径;有计划、合理地开采矿物,否则既浪费了资源,又损害了国家利益;寻找金属的代用品,减少了金属的使用等。
故答案为:
(1)铝在空气中能与氧气反应,其表面生成一层致密的氧化铝薄膜,防止内部的铝进一步被氧化;
(2)Fe+CuSO4═FeSO4+Cu;
(3)防止金属腐蚀(或回收利用废旧金属,有计划、合理地开采矿物,回收利用废旧金属等)。
3.(2018•陕西)人类文明进步与金属材料发展关系十分密切。
(1)铝合金被广泛应用于制造飞机、高铁等这是因为铝合金具有 强度高 、质量轻、耐腐蚀等特性。
(2)化学兴趣小组为了鉴别某黄色金属是黄金还是黄铜(铜锌合金),设计了如下方案:
①取样,在空气中加热②取样加入硝酸银溶液③取样,加入硫酸锌溶液
其中不合理的是 ③ (填序号)。某同学提出还可以用稀硫酸鉴别他所依据的反应原理是 Zn+H2SO4═ZnSO4+H2↑ (用化学方程式表示)。
【解答】解:(1)铝合金被广泛应用于制造飞机、高铁等,这是因为铝合金具有强度高、质量轻、耐腐蚀等特性。
(2)①取样,在空气中加热,黄铜中的铜在加热条件下生成黑色的氧化铜,黄金则不能,可以鉴别。
②取样加入硝酸银溶液,锌和铜均能与硝酸银溶液反应生成置换出银白色的银,黄金则不能,可以鉴别。
③取样,加入硫酸锌溶液,锌、铜、金均不能与硫酸锌溶液反应,不能鉴别。
某同学提出还可以用稀硫酸鉴别,是因为锌能与稀硫酸反应生成硫酸锌和氢气,反应的化学方程式为:Zn+H2SO4═ZnSO4+H2↑。
故答案为:
(1)强度高;
(2)③;Zn+H2SO4═ZnSO4+H2↑。
三.微粒观点及模型图的应用(共1小题)
4.(2018•陕西)合理使用化肥可提高农作物产量。如图是生产尿素的微观示意图,回答问题。
(1)A物质中氮元素的化合价是 ﹣3 。D物质的化学式是 H2O 。
(2)下列与尿素不属于同类肥料的是 C 。
A.NH4HCO3 B.NH4Cl C.K2SO4
【解答】解:(1)根据工业上生产尿素的反应的微观示意和质量守恒定律可知,A、B、C、D分别为NH3、CO2、CO(NH2)2、H2O,反应的方程式是:2NH3+CO2CO(NH2)2+H2O,由此可知:
A物质是NH3,NH3中氢元素的化合价是+1,氮元素的化合价是﹣3,D物质的化学式是H2O;
(2)A.NH4HCO3 中含有氮元素属于氮肥;
B.NH4Cl 中含有氮元素属于氮肥;
C.K2SO4 中含有钾元素属于钾肥;
答案:
(1)﹣3;H2O;
(2)C
四.化学符号及其周围数字的意义(共1小题)
5.(2020•陕西)含义丰富的化学符号是独特的化学语言。根据以下符号回答:
①2N2②Al3+③2H ④SO42﹣⑤CH4
(1)能表示宏观物质的是 ⑤ (填序号)。
(2)①表示两个 氮分子 。
(3)由②和④构成的物质的化学式为 Al2(SO4)3 。
(4)⑤中数字“4”的含义是 1个甲烷分子中含有4个氢原子 。
【解答】解:(1)化学式宏观上可表示一种物质,CH4可表示甲烷这种宏观物质。
(2)由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其分子符号前加上相应的数字,则2N2可表示2个氮分子。
(3)②和④分别是铝离子和硫酸根离子,构成的物质是硫酸铝,其化学式为Al2(SO4)3。
(4)标在化学式中元素右下角的数字表示一个分子中所含原子的数目,CH4中的“4”表示1个甲烷分子中含有4个氢原子。
故答案为:
(1)⑤;
(2)氮分子;
(3)Al2(SO4)3;
(4)1个甲烷分子中含有4个氢原子。
五.复分解反应的条件与实质(共1小题)
6.(2018•陕西)化学是研究物质的组成、结构、性质及变化规律的科学。
(1)下列符号能表示2个原子的是 ① (填序号)。
①2N ②2CO ③Mg2+④
(2)如图是碳酸钠溶液与氢氧化钙溶液发生反应的微观示意图。
该反应可观察到的现象是 产生白色沉淀 ,反应的微观本质是 碳酸根离子和钙离子结合生成碳酸钙沉淀 。
【解答】解:(1)由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,故2N可表示2个氮原子;②2CO可表示2个一氧化碳分子;③Mg2+可表示镁离子;④可表示亚硫酸根的化合价为﹣2价。
(2)碳酸钠溶液与氢氧化钙溶液反应生成碳酸钙沉淀和氢氧化钠,反应的现象是产生白色沉淀;由微观示意图可知,反应的微观本质是碳酸根离子和钙离子结合生成碳酸钙沉淀。
故答案为:
(1)①;
(2)产生白色沉淀;碳酸根离子和钙离子结合生成碳酸钙沉淀。
六.根据化学反应方程式的计算(共8小题)
7.(2022•陕西)学习小组同学为测定某品牌钙片中含碳酸钙的质量分数,向盛有10g钙片的烧杯中加入过量稀盐酸,充分反应后,测得烧杯内混合物的总质量比反应前稀盐酸与钙片的总质量减少了3.3g。(钙片中其他成分不与稀盐酸反应放出气体)
(1)反应中生成二氧化碳的质量是 3.3 g。
(2)计算该品牌钙片中含碳酸钙的质量分数。
【解答】解:(1)根据质量守恒定律,反应后减少的质量为生成二氧化碳的质量,即二氧化碳质量为3.3g;
(2)解:设参加反应的碳酸钙的质量为x。
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 3.3 g
解得:x=7.5g
该品牌钙片中含碳酸钙的质量分数==75%
答:该品牌钙片中含碳酸钙的质量分数为75%。
故答案为:
(1)3.3;
(2)75%。
8.(2021•陕西)学习小组的同学想测定某种大理石中碳酸钙的质量分数。取大理石样品25g,逐渐缓慢向其中加入150g溶质质量分数为14.6%的稀盐酸(杂质难溶于水,且不与酸反应),测得剩余固体的质量与加入稀盐酸的质量关系如图所示。完成下列分析与计算:
(1)恰好完全反应时消耗稀盐酸的质量是 100 g。
(2)计算该大理石中碳酸钙的质量分数。
【解答】解:(1)通过图示可知,剩余固体质量在稀盐酸加入到100g时,不再减少,说明碳酸钙此时反应完全,故恰好完全反应时消耗稀盐酸的质量是100g;故答案为:100;
(2)解:设25 g该大理石样品中CaCO3的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 2×36.5
x 100 g×14.6%
=
x=20 g
该大理石中碳酸钙的质量分数=×100%=80%
答:该大理石中碳酸钙的质量分数为80%。
9.(2021•陕西)学习小组的同学通过如图实验测定一瓶失去标签的稀硫酸中溶质的质量分数。
请完成下列分析与计算:
(1)反应中用去稀硫酸的质量为 20 g。
(2)计算稀硫酸中溶质的质量分数。
【解答】解:(1)反应中用去稀硫酸的质量为:40g﹣20g=20g。
故填:20。
(2)设硫酸质量为x,
2NaOH+H2SO4═Na2SO4+2H2O,
80 98
20×20% x
=,
x=4.9g,
稀硫酸中溶质的质量分数是:×100%=24.5%,
答:稀硫酸中溶质的质量分数是24.5%。
10.(2020•陕西)为测定某工厂废水中CuSO4的含量,取废水样品400g,滴加质量分数为10%的NaOH溶液至不再产生沉淀时,消耗NaOH溶液的质量是10g。(废水中其它杂质易溶于水,但不与NaOH反应)请完成下列分析及计算:
(1)若想通过沉淀的质量计算CuSO4的质量,应对过滤后的沉淀进行 洗涤 、干燥后再称量。
(2)计算废水中CuSO4的质量分数。
【解答】解:(1)若想通过沉淀的质量计算CuSO4的质量,应对过滤后的沉淀进行洗涤、干燥后再称量;
(2)设400 g废水中CuSO4的质量为x
2NaOH+CuSO4═Cu(OH)2↓+Na2SO4
80 160
10 g×10% x
=
x=2g
废水中CuSO4的质量分数为:×100%=0.5%
答:废水中CuSO4的质量分数为0.5%。
故答案为:(1)洗涤;
(2)0.5%。
11.(2020•陕西)为测定某赤铁矿中Fe2O3的含量,取10g该赤铁矿样品于烧杯中,向其中加入100g稀盐酸,恰好完全反应,测得剩余固体的质量为2g。(杂质不溶于水也不与酸反应)
请完成下列分析及计算:
(1)10g样品中杂质的质量为 2 g。
(2)计算稀盐酸中溶质的质量分数。
【解答】解:(1)测得剩余固体的质量为2g,说明杂质质量是2g,则10g样品中杂质的质量为2g。
故填:2。
(2)设稀盐酸中氯化氢质量为x,
Fe2O3+6HCl═2FeCl3+3H2O,
160 219
10g﹣2g x
=,
x=10.95g,
稀盐酸中溶质的质量分数是:×100%=10.95%,
答:稀盐酸中溶质的质量分数是10.95%。
12.(2019•陕西)化学兴趣小组为测定某铜锌合金中成分金属的含量,称取10g样品放入烧杯中,向其中加入100g稀硫酸,恰好完全反应后。测得烧杯内所有物质的总质量为109.8g。
请完成下列分析及计算:
(1)反应中共生成气体 0.2 g。
(2)计算合金中铜的质量分数。
【解答】解:(1)反应中共生成气体质量:10g+100g﹣109.8g=0.2g。
故填:0.2。
(2)设锌质量为x,
Zn+H2SO4═ZnSO4+H2↑,
65 2
x 0.2g
=,
x=6.5g,
合金中铜的质量分数为:×100%=35%,
答:合金中铜的质量分数为35%。
13.(2018•陕西)为测定一瓶未知浓度的硫酸的溶质质量分数,化学兴趣小组向含有酚酞的100g 4%的氢氧化钠溶液中滴加该硫酸,恰好完全反应时溶液总质量为150g。(酚酞质量不计)
(1)恰好完全反应时的现象是 红色褪去 。
(2)计算硫酸的溶质质量分数。
【解答】解:(1)恰好完全反应时溶液呈中性,所以现象是红色褪去。
(2)由质量守恒定律可知,滴入稀硫酸的质量为:150g﹣100g=50g,
设硫酸的溶质质量分数为x
H2SO4+2NaOH=Na2SO4+2H2O
98 80
50gx 100g×4%
解得:x=9.8%
故答案为:(1)红色褪去;(2)硫酸的溶质质量分数为9.8%。
14.(2018•陕西)某补钙剂的主要成分是碳酸钙。欲测定该补钙剂中碳酸钙的质量分数,某同学进行了如图所示的操作(假设其它成分可溶于水但不参与反应)。
(1)该实验中,装置的气密性对测定结果 无 (填“有”或“无”)影响。
(2)计算该补钙剂中碳酸钙的质量分数。
【解答】解:由于是让生成的二氧化碳跑掉,借助质量变化求算生成的二氧化碳的质量,该实验中,装置的气密性对测定结果 没有影响。
根据质量守恒定律,二氧化碳的质量为:370g﹣363.4g=6.6g
设该补钙剂中碳酸钙的质量分数为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
20gx 6.6g
=
x=75%
答:(1)该实验中,装置的气密性对测定结果无影响。
(2)该补钙剂中碳酸钙的质量分数为75%。
七.合成材料的使用及其对人和环境的影响(共1小题)
15.(2020•陕西)在抗击“新冠肺炎”疫情的战斗中,人们采取了一系列行之有效的防控措施。
(1)口罩是防疫的必备品,其生产原料中用到的聚丙烯属于 有机合成材料 (填“无机非金属材料”或“有机合成材料”)。
(2)洗手、消毒能有效防止病毒感染。“84”消毒液能迅速杀菌消毒,其有效成分NaClO中氯元素的化合价为 +1 。
(3)测量体温是防控的重要环节。家庭常备体温计中的液态物质是 汞或Hg 。
(4)加强营养有利于增强体质,合理补充维生素能提高人体免疫力。下列食品中富含维生素的是 B (填字母)。
A.鸡肉
B.黄瓜
C.面包
【解答】解:(1)聚丙烯是一种合成纤维,属于有机合成材料;故填:有机合成材料;
(2)钠元素显+1价,氧元素显﹣2价,设氯的化合价为x,由化合物中各元素正负化合价的代数和为零原则可知:(+1)+x+(﹣2)=0,x=+1;故填:+1;
(3)汞是常温下唯一呈液态的金属,家庭常备体温计中的液态物质是金属汞;故填:汞或Hg;
(4)A.鸡肉富含蛋白质;
B.黄瓜富含维生素;
C.面包富含糖类。
故选:B。
八.有机高分子材料的分类及鉴别(共1小题)
16.(2020•陕西)2020年6月1日起,公安部交管局在全国开展“一盔一带”安全守护行动。
(1)骑摩托车必须佩戴头盔。头盔某些部件连接处的铁质铆钉表面常进行电镀处理,其目的是 防止锈蚀 ,同时兼顾美观。
(2)汽车行驶中必须使用安全带。安全带一般用尼龙制成,尼龙属于 合成纤维 (填“天然纤维”或“合成纤维”)。汽车安全气囊被触发时,气囊中的叠氮化钠(NaN3)会瞬间分解,产生一种空气中最多的气体,其化学式是 N2 。
(3)汽车和摩托车尾气中通常含有CO2、CO、NO、NO2等气体,其中不属于大气污染物的是 CO2 。
【解答】解:(1)头盔某些部件连接处的铁质铆钉表面常进行电镀处理的目的是为了防止锈蚀,同时兼顾美观,故填:防止锈蚀;
(2)尼龙属于合成纤维;气囊中的叠氮化钠(NaN3)瞬间分解产生的空气中最多的气体是氮气,其化学式是N2,故填:合成纤维;N2;
(3)汽车和摩托车尾气中含有的CO2、CO、NO、NO2等气体中二氧化碳不属于大气污染物,故填:CO2。
九.棉纤维、羊毛纤维和合成纤维的鉴别(共1小题)
17.(2018•陕西)中国的许多用具独具一格,既表现了中华民族不同于其他民族的风俗,又为世界文化的进步和发展作出了贡献,其中典型的有被誉为“文房四宝”的笔、墨、纸、砚。
(1)制作毛笔“笔毫”的原料之一是白羊毛,生活中可用 灼烧,闻气体 法将其与合成纤维区分开。
(2)古代文人用墨作的字画可以保存至今而不褪色的原因是 常温下碳的化学性质很稳定 。
(3)砚台是“文房四宝”之首,以石砚居多。制作石砚的过程发生了 物理 (填“物理”或“化学”)变化。
【解答】解:(1)羊毛的主要成分是蛋白质,灼烧时会产生烧焦羽毛的气味,而合成纤维灼烧无此气味;故填:灼烧,闻气体;
(2)用墨汁写绘的字画能从古代保存至今而不褪色,是因为墨汁中含有炭黑,主要成分是碳,常温下碳的化学性质很稳定;故填:常温下碳的化学性质很稳定;
(3)制作石砚的过程没有生成新物质,发生的属于物理变化;故填:物理。
一十.食品、药品与健康食品中的有机营养素(共2小题)
18.(2019•陕西)陕西名小吃肉丸糊辣汤的制作原料有:牛肉、淀粉、土豆、胡萝卜、豆角及调料等。
(1)上述原料中富含蛋白质的是 牛肉 。
(2)淀粉溶液遇碘水能变蓝色,这是淀粉的 化学 (填“物理”“化学”)性质。
(3)在远处就能闻到胡辣汤的香味,说明分子 在不停地运动 。
【解答】解:(1)牛肉中富含蛋白质;
(2)淀粉溶液遇碘水能变蓝色是通过化学变化才能表现出来的性质,属于淀粉的化学性质;
(3)在远处就能闻到胡辣汤的香味,这说明分子是不停运动的。
故答案为:(1)牛肉;(2)化学;(3)在不停地运动。
19.(2018•陕西)橄榄油营养丰富、滋润度高、在餐饮、美容及制皂领域越来越受到大家的青睐。
(1)橄榄油中富含的主要营养素是 油脂 。
(2)工厂可用活性炭对初榨橄榄油进行脱色处理,这是利用了活性炭的 吸附 性。
(3)用橄榄油制成的肥皂在洗涤油污的过程中起 乳化 作用。
【解答】解:(1)橄榄油中富含的主要营养素是油脂;故填:油脂;
(2)活性他具有吸附性,可以除去初榨橄榄油的色素;故填:吸附;
(3)肥皂具有乳化作用,可以用来除去油污;故填:乳化。
一十一.鉴别淀粉、葡萄糖的方法与蛋白质的性质(共1小题)
20.(2020•陕西)文房四宝“笔、墨、纸、砚”承载着优秀的中华传统文化。
(1)制作毛笔常用羊毛、兔毛等,检验笔毛是动物毛发的简易方法是 灼烧,闻气味 。
(2)用墨汁写绘的字画能从古代保存至今而不褪色,是因为常温下碳的化学性质很 稳定 (填“稳定”或“不稳定”)。
(3)宣纸制作过程中,有道工序是从纸浆中用竹帘捞纸,该操作相当于 B (填字母)。
A.蒸发
B.过滤
C.结晶
(4)砚台产地不同,成分也有差别,但其中的主要成分都 难溶 (填“易溶”或“难溶”)于水。
【解答】解:(1)动物毛发的主要成分是蛋白质,检验笔毛是动物毛发的简易方法是灼烧,闻气味,产生烧焦羽毛的气味,说明是笔毛是动物毛发。
(2)用墨汁写绘的字画能从古代保存至今而不褪色,是因为墨汁中含有炭黑,主要成分是碳,常温下碳的化学性质很稳定。
(3)有道工序是从纸浆中用竹帘捞纸,是将纸与纸浆分离,利用的过滤的原理。
(4)砚台产地不同,成分也有差别,墨汁中含有水,砚台能用于研磨墨,说明其中的主要成分都难溶于水。
故答案为:
(1)灼烧,闻气味;
(2)稳定;
(3)B;
(4)难溶。
广西桂林五年(2018-2022)中考化学真题分题型分层汇编-05填空题: 这是一份广西桂林五年(2018-2022)中考化学真题分题型分层汇编-05填空题,共13页。
山西省各市五年(2018-2022)中考化学真题分题型分层汇编-06计算题&推断题: 这是一份山西省各市五年(2018-2022)中考化学真题分题型分层汇编-06计算题&推断题,共12页。试卷主要包含了分析辨识,解决问题等内容,欢迎下载使用。
山西省各市五年(2018-2022)中考化学真题分题型分层汇编-07填空题&流程题: 这是一份山西省各市五年(2018-2022)中考化学真题分题型分层汇编-07填空题&流程题,共16页。试卷主要包含了周末,小明和妈妈一起清洗油烟机,3+3H2O]等内容,欢迎下载使用。












