





人教版九年级上册课题4 化学式与化合价示范课课件ppt
展开物质的化学式可以清晰地表示物质的组成。
Na2O Na2S H2O H2S
CaO MgO CO NaCl
CaCl2 MgCl2 CO2 SiO2
一、化合价的概念和规律
1、 概念:一种元素一定数目的原子跟其他元素一定数目的原子相化合的性质。
2、规定: (1)在离子构成的化合物中,化合价与离子所带电荷数有关。Na原子失去一个电子变成Na+,规定Na元素的化合价为+1;Cl原子得到一个电子变成Cl-,规定Cl元素的化合价为-1。(2)在分子构成的化合物中,化合价与共用电子对的数目有关。
当n=1时,1不能省略
4、基本规律:(1)化合价有正负之分,在化合物里,各元素正负化合价的代数和等于零;(2)元素的化合价是元素在形成化合物时表现出来的性质,因此单质中元素的化合价为零;(3)在化合物中氢元素通常显+1价,氧元素通常显-2价,常以它们为基准来推算化合物中其他元素的化合价;(4)有些元素在不同的化合物中,显示不同的价态。
二、常见元素和原子团的化合价
1、常见元素的化合价(记忆)
钾钠银氢正一价,钙镁钡锌正二价;铝是正三氧负二,氯负一价最常见;硫有负二正四六,正二正三铁可变;正一二铜二四碳,单质零价永不变。
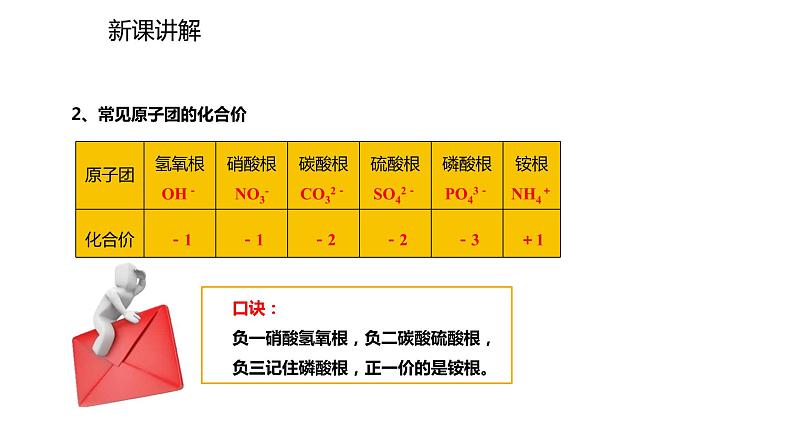
2、常见原子团的化合价
口诀: 负一硝酸氢氧根,负二碳酸硫酸根, 负三记住磷酸根,正一价的是铵根。
1、根据已知元素的化合价,求未知元素的化合价
HCl HClO KClO3 Cl2
H2S SO2 H2SO4
-1 +1 +5 0
-2 +4 +6
【例题】根据已知元素的化合价,求算指定元素的化合价。
+2 +3
FeCl2 FeCl3
2、根据化合价,书写化学式——十字交叉法
书写步骤:(1)符号:正价前、负价后;(2)标价 (3)约简(4)交叉:数字1省略不写。(5)检查:各元素正负化合价的 代数和是否为零。
已知磷元素的化合价为+5价,请写出这种磷的氧化物的化学式。
【练习】写出下列物质的化学式
1、化合价是元素的一种重要性质,熟练记忆各种元素的化合价是学好化学的基础; 2、在化合物里,各元素正负化合价的代数和等于零;单质中元素的化合价为零。
1、飞机C919开创了两个全国首次。其中之一是先进铝锂合金的应用,Li的质子数是3,最外层电子数为1,则Li元素在化合物中的常见化合价是( ) A.0 B.+1 C.+2 D.+3
【方法点拨】根据原子结构中最外层电子数与元素化合价的关系来分析解答。 【解析】金属元素的化合价的数值就是金属原子在化学反应中失去电子的数目。锂原子的质子数为3,则锂原子的核外有3个电子,第一层2个,第二层也就是最外层有1个电子,所以在化学反应中易失去最外层的1个电子而显+1价。
2、偏钛酸钡(BaxTiO3)因其显著地“压电效应”而广泛的应用于超声波发生装置中。已知偏钛酸钡中钛元素的化合价为+4价,则其化学式中x的数值为( ) A、1 B、2 C、3 D、4
【方法点拨】根据“在化合物里,各元素正负化合价的代数和为零”,进行计算。 【解析】钡元素显+2价,钛元素显+4价,氧元素显-2价,根据在化合物中正负化合价代数和为零,可得(+2)×x+(+4)+(-2)×3=0,则x=1。
3、在下列四种含有氯元素的物质中,氯元素化合价最高的是( )A.Cl2 B.NaC1 C.HClO4 D.HClO
【方法点拨】根据单质中元素的化合价为0,在化合物中正负化合价代数和为零,结合各选项中的化学式进行解答。 【解析】A、根据单质中元素的化合价为0,Cl2属于单质,故氯元素的化合价为0。B、钠元素显+1价,设氯元素的化合价是x,根据在化合物中正负化合价代数和为零,可得(+1)+x=0,则x=-1价。C、氢元素显+1价,氧元素显-2价,设氯元素的化合价是m,根据在化合物中正负化合价代数和为零,可得(+1)+m+(-2)×4=0,则m=+7价。D、氢元素显+1价,氧元素显-2价,设氯元素的化合价是z,根据在化合物中正负化合价代数和为零,可得(+1)+z+(-2)=0,则z=+1价。
超导材料为具有零电阻及反磁性的物质,以Y2O3、BaCO3和CuO为原料,经研磨烧结后合成一种高温超导物质Y2Ba4Cu6Ox,假设在研磨烧结过程中各元素的化合价均无变化,则x的值为多少?
解:在Y2O3中O为-2价,则由正负化合价的代数和为0,可得Y的化合价为+3价,BaCO3中碳酸根的化合价为-2价,则Ba元素的化合价为+2价,CuO中O为-2价,则Cu元素的化合价为+2价,由在研磨烧结过程中各元素的化合价无变化,则在Y2Ba4Cu6Ox中,Y的化合价为+3价,Ba元素的化合价为+2价,Cu元素的化合价为+2价,O为-2价,根据正负化合价的代数和为0,则有 (+3)×2+(+2)×4+(+2)×6+(-2)×x=0,解得x=13。
初中化学人教版九年级上册课题4 化学式与化合价说课课件ppt: 这是一份初中化学人教版九年级上册课题4 化学式与化合价说课课件ppt,共22页。PPT课件主要包含了说课环节,教材分析,教学目标,学情分析,教学重难点,教学方法,教学过程,表示的意义,化学式,H2O表示的意义等内容,欢迎下载使用。
人教版九年级上册课题3 水的组成教学演示ppt课件: 这是一份人教版九年级上册课题3 水的组成教学演示ppt课件,共20页。PPT课件主要包含了自主学习,水的物理性质,小组交流合作,水分子分解图解,合作探究等内容,欢迎下载使用。
人教版九年级上册第四单元 自然界的水综合与测试优秀复习ppt课件: 这是一份人教版九年级上册第四单元 自然界的水综合与测试优秀复习ppt课件,共40页。PPT课件主要包含了爱护水资源,小卵石,石英砂,肥皂水,氢元素,氧元素,氢原子,氧原子,增强导电性,物质的分类等内容,欢迎下载使用。













