
高中化学鲁科版 (2019)选择性必修3第3节 合成高分子化合物第2课时学案
展开能力课时3 常见有机反应类型的判断方法
探 究 任 务 | 1.通过明确有机反应类型与有机物类别的关系,加深对有机反应的认知,提升宏观辨识与微观探析的化学核心素养。 2.通过对各反应类型的反应条件的认知,提升证据推理与模型认知的化学核心素养。 |
探究要点
归纳整合
1.利用有机反应类型与有机物类别的关系判断
基本类型 | 有机物类别 | |
取代反应 | 卤代反应 | 饱和烃、苯和苯的同系物、卤代烃等 |
酯化反应 | 醇、羧酸、糖类等 | |
水解反应 | 卤代烃、酯、低聚糖、多糖、蛋白质等 | |
硝化反应 | 苯和苯的同系物等 | |
磺化反应 | 苯和苯的同系物等 | |
加成反应 | 烯烃、炔烃、苯和苯的同系物、醛等 | |
消去反应 | 卤代烃、醇等 | |
氧化反应 | 燃烧 | 绝大多数有机物 |
酸性KMnO4溶液 | 烯烃、炔烃、苯的同系物(侧链烃基与苯环直接相连的碳原子上有氢原子)等 | |
直接(或催化) 氧化 | 酚、醇、醛、葡萄糖等 | |
还原反应 | 醛、葡萄糖等 | |
聚合反应 | 加聚反应 | 烯烃、炔烃等 |
缩聚反应 | 苯酚与甲醛、多元醇与多元羧酸等 | |
与浓硝酸的颜色反应 | 蛋白质(含苯环的) | |
与FeCl3溶液的显色反应 | 酚类物质 | |
2.利用反应条件判断
(1)在NaOH的水溶液中发生水解反应,可能是酯的水解反应或卤代烃的水解反应。
(2)在NaOH的乙醇溶液中加热,发生卤代烃的消去反应。
(3)在浓H2SO4存在的条件下加热,可能发生醇的消去反应、酯化反应、成醚反应或硝化反应等。
(4)与H2在Ni作用下发生反应,则为烯烃、炔烃、芳香烃、醛的加成反应或还原反应。
(5)在O2、Cu(或Ag)、加热或CuO、加热条件下,发生醇的氧化反应。
(6)与O2或新制Cu(OH)2悬浊液或银氨溶液反应,则该物质发生的是—CHO的氧化反应。(如果连续两次出现O2,则为醇―→醛―→羧酸的过程)
(7)在稀H2SO4、加热条件下,发生酯的水解反应。
(8)在光照、X2条件下,发生烷基上的取代反应;在Fe粉、X2条件下,发生苯环上的取代反应。
典例探究
【例题】 某有机物结构简式如下,则此有机物可发生的反应类型有( )
①取代反应 ②加成反应 ③消去反应 ④酯化反应 ⑤水解反应 ⑥氧化反应 ⑦中和反应 ⑧加聚反应 ⑨缩聚反应
A.①②③⑤⑥⑨ B.②③④⑤⑥⑧
C.①②③④⑤⑥ D.①②③④⑤⑥⑦⑧⑨
D [该有机物中含有的官能团有碳碳双键能发生加成、加聚反应、氧化反应,酯基能发生水解(取代)反应;含有羟基和羧基,能发生酯化(取代)、氧化、消去、中和、缩聚反应。]
对点训练
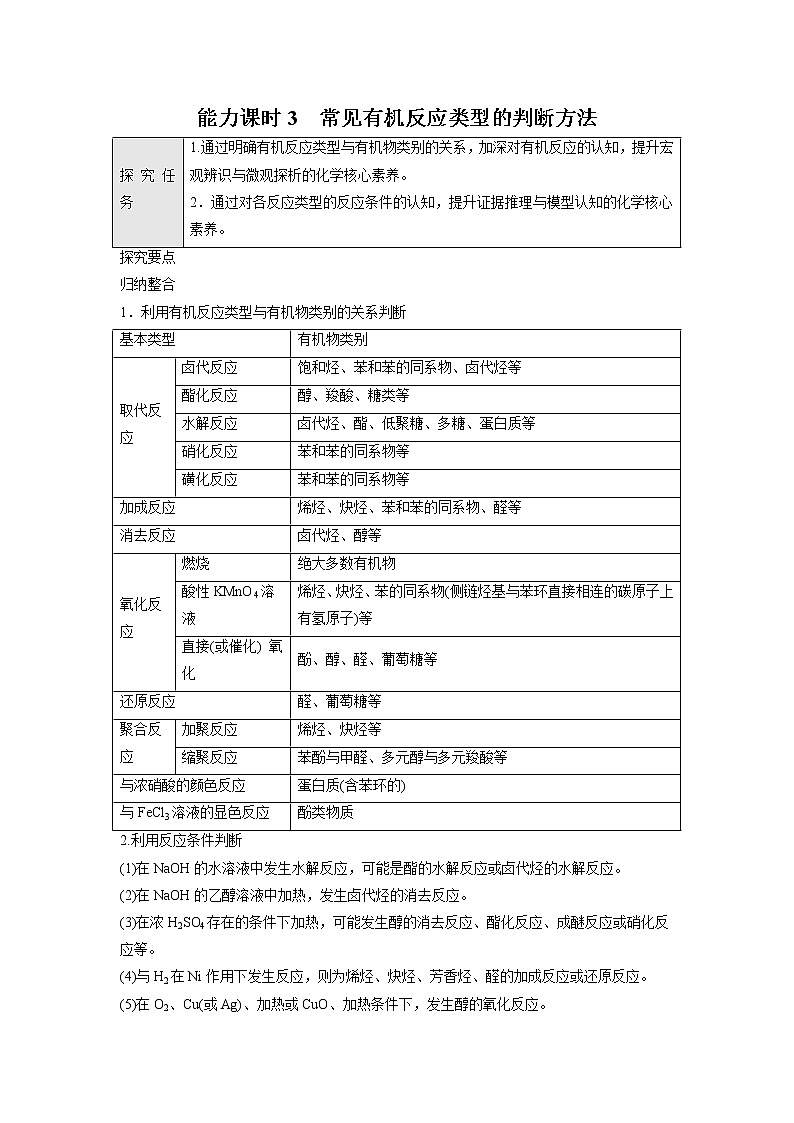
1.诺贝尔奖科学成果被应用于工业合成重要的治疗帕金森症(震颤麻痹症)的药物左旋多巴(C)。下面是它们的结构简式以及科学家设计的合成路线。
在上述反应中,关于(1)、(2)两步的反应类型,全部正确的是( )
A.消去反应,水解反应 B.氧化反应,取代反应
C.加成反应,取代反应 D.还原反应,消去反应
C [A生成B是加成反应也是还原反应,A、B错误;B在酸性条件下生成C是水解反应或取代反应,没有不饱和键的生成,不是消去反应,C正确,D错误。]
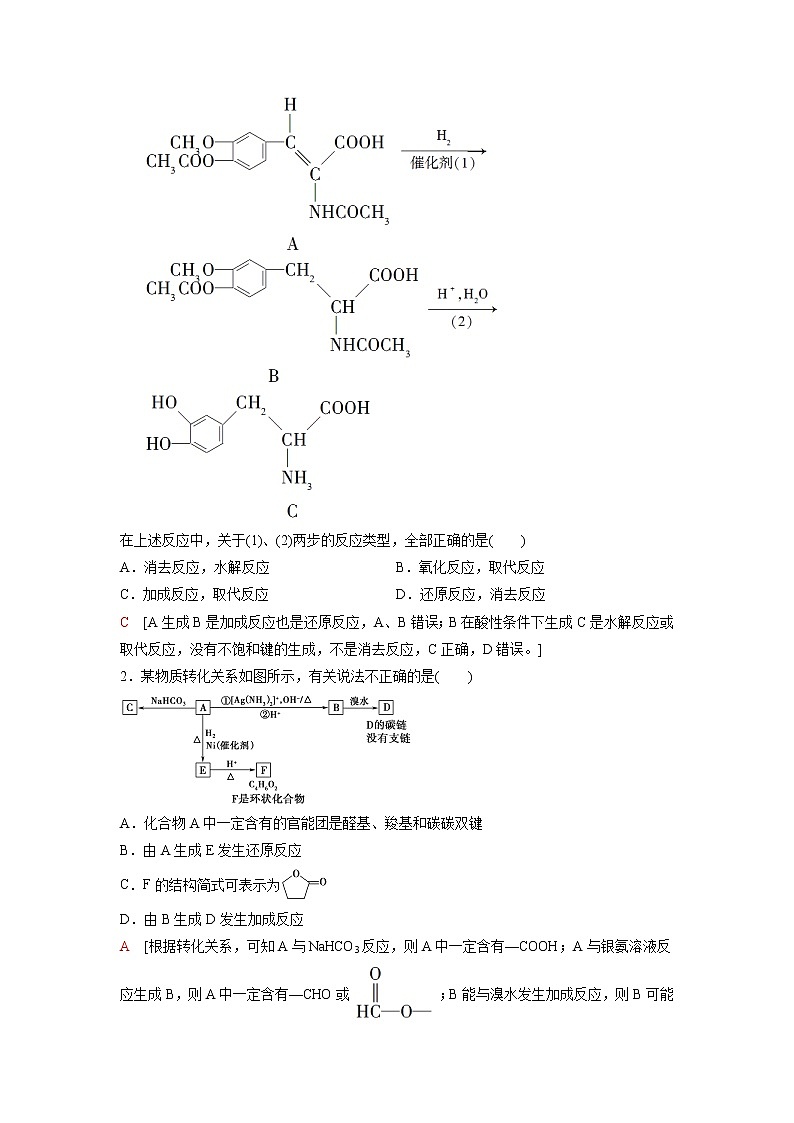
2.某物质转化关系如图所示,有关说法不正确的是( )
A.化合物A中一定含有的官能团是醛基、羧基和碳碳双键
B.由A生成E发生还原反应
C.F的结构简式可表示为
D.由B生成D发生加成反应
A [根据转化关系,可知A与NaHCO3反应,则A中一定含有—COOH;A与银氨溶液反应生成B,则A中一定含有—CHO或;B能与溴水发生加成反应,则B可能含有或—C≡C—;A与H2加成生成E,E在H+、加热条件下生成的F是环状化合物,应该是发生分子内酯化反应;推断A可能是OHC—CH===CH—COOH或OHC—C≡C—COOH,故A项不正确。]
学科素养
情境素材
我国科学家屠呦呦因发现植物黄花蒿的茎叶中含有的抗疟疾的物质——青蒿素而荣获2015年诺贝尔生理学或医学奖。科学家们对青蒿素进行进一步转化,合成药效更佳的双氢青蒿素、蒿甲醚,具体转化过程如图所示。
问题探究
1.反应①的有机反应类型是还原反应吗?反应②属于取代反应吗?
提示:反应①的有机反应类型是还原反应;反应②属于取代反应。
2.双氢青蒿素可以发生消去反应吗?
提示:双氢青蒿素中与羟基相连碳原子的邻位碳原子上有氢原子,可以发生消去反应。
3.青蒿素、双氢青蒿素、蒿甲醚三种物质都能与氢气发生加成反应吗?
提示:不能。青蒿素中含有的酯基不能与氢气发生加成反应;双氢青蒿素、蒿甲醚中均不含不饱和键,不能与氢气发生加成反应。
素养养成
通过本情境素材对青蒿素、双氢青蒿素、蒿甲醚的结构及反应类型的探究,提升了证据推理与模型认知的核心素养。
随堂测评
1.下列反应中,属于加成反应的是( )
A.CH2===CHCH3+Cl2CH2===CHCH2Cl+HCl
B.CH3CHO+H2CH3CH2OH
C.CH3CH2OHCH2===CH2↑+H2O
D.2CH3CHO+O22CH3COOH
B [A为取代反应;B为加成反应;C为消去反应;D为氧化反应;故选B。]
2.(2021·湖南常德高二上期末)下列反应中,属于取代反应的是 ( )
B [A项,乙烯和氢气反应生成乙烷,为加成反应;B项,苯和溴单质在催化剂作用下反应生成溴苯和溴化氢,属于取代反应;C项,乙醇燃烧属于氧化反应;D项,乙烯和水反应生成乙醇,属于加成反应;故选B。]
3.4溴环己烯主要用于有机合成,它可发生如图所示的转化,下列叙述错误的是 ( )
A.反应①为氧化反应,产物含有溴原子和羧基两种官能团
B.反应②为取代反应,产物含有羟基和碳碳双键两种官能团
C.反应③为消去反应,产物含碳碳双键和溴原子两种官能团
D.反应④为加成反应,产物只含溴原子一种官能团
C [酸性高锰酸钾溶液可以氧化碳碳双键,碳碳双键断裂生成两个羧基,与溴原子不反应,产物含有溴原子和羧基两种官能团,A正确;在强碱水溶液加热条件下,4溴环己烯中的溴原子被羟基取代,产物含有羟基和碳碳双键两种官能团,B正确;在强碱醇溶液加热条件下,4溴环己烯发生消去反应,生成碳碳双键,产物只含碳碳双键一种官能团,C错误;4溴环己烯中的碳碳双键与HBr发生加成反应,产物只含溴原子一种官能团,D正确。]
4.下列高聚物中,由两种不同的单体通过缩聚反应制得的是( )
D [A项是由CH2===CH2和CH2===CHCN加聚而成的;B项是由CH2===CH—CH===CH2加聚而成的;C项是由CH2===CH—CH===CH2和CH2===CHC6H5加聚而成的;D项是由缩聚而成,D正确。]
5.有以下一系列反应:
判断下列转化的反应类型:
(1)A→B:____________________________________________;
(2)B→C:____________________________________________;
(3)C→D:_____________________________________________;
(4)E→F:_____________________________________________;
(5)E+G→H:_________________________________________。
[答案] (1)取代反应 (2)消去反应 (3)加成反应 (4)氧化反应 (5)酯化反应(或取代反应)
高中化学第3节 烃第2课时学案: 这是一份高中化学第3节 烃第2课时学案
鲁科版 (2019)选择性必修3第3节 合成高分子化合物第1课时导学案: 这是一份鲁科版 (2019)选择性必修3第3节 合成高分子化合物第1课时导学案
化学第3节 合成高分子化合物第3课时导学案及答案: 这是一份化学第3节 合成高分子化合物第3课时导学案及答案













