

初中化学鲁教版九年级下册第二节 海水“晒盐“第2课时练习
展开第八单元 第二节 第2课时 溶解度
一、选择题
1.某同学模拟化学家侯德榜的“侯氏制碱法”制纯碱,需用50.0 g水配制20 ℃的氯化钠饱和溶液(20 ℃时氯化钠的溶解度为36.0 g),应称取氯化钠的质量为 ( )
A.18.0 g B.16.0 g C.13.2 g D.11.5 g
2.能使气体物质溶解度增大的操作是 ( )
A.增加溶剂 B.振荡溶液
C.增大压强 D.升高温度
3.20 ℃时,50 g水中最多能溶解0.8 g A物质,则A物质属于 ( )
A.易溶物质 B.可溶物质
C.微溶物质 D.难溶物质
4.[2019·福建] KNO3的溶解度曲线如图1所示,下列说法错误的是 ( )
A.0~60 ℃,KNO3的溶解度随温度的升高而增大
B.60 ℃时的KNO3饱和溶液降温至20 ℃,有晶体析出
C.20 ℃时,100 g水中最多能溶解31.6 g KNO3
D.60 ℃时,可配制溶质质量分数为60%的KNO3溶液 图1
5.下面两个实验的目的是探究影响物质溶解性的因素,关于该实验下列说法正确的是 ( )
实验一 | 实验二 |
A.实验一的目的是探究溶剂的性质对硝酸钾溶解性的影响
B.实验一需要控制相同的变量是水的体积、硝酸钾的质量
C.实验二是探究溶质性质对物质溶解性的影响
D.实验二不需要控制相同的变量是水和酒精的质量
6.[2019·嘉兴] 20 ℃时,把36 g氯化钠放入64 g水中,使其充分溶解(20 ℃时氯化钠的溶解度为36 g)。下列关于所得溶液的说法错误的是 ( )
A.该溶液是饱和溶液
B.溶液中Na+和Cl-个数一定相等
C.溶液质量为100 g
D.溶质与溶剂质量比为9∶25
7.如图2是X、Y两种固体物质的溶解度曲线。下列叙述正确的是 ( )
A.温度低于t2 ℃时,物质Y的溶解度小于X
B.X、Y的溶解度都随温度的升高而增大
C.a点表示t1 ℃时X、Y的溶液都不饱和
D.Y的饱和溶液降低温度后,溶质质量分数不变 图2
8.生石灰的主要成分是氧化钙,能与水反应生成氢氧化钙并放出大量的热。室温时,将生石灰加入饱和石灰水中,参照如图3所示氢氧化钙的溶解度曲线,下列判断错误的是 ( )
A.反应过程中,石灰水始终是饱和溶液
B.反应过程中,氢氧化钙的溶解度增大
C.反应结束后,溶液的质量减少
D.反应结束后,恢复至室温时,溶液的溶质质量分数不变 图3
二、填空题
9.[2020·临沂改编] 如图4是甲、乙、丙三种固体物质的溶解度曲线。
图4
(1)P点表示的含义为 。
(2)t1 ℃时,60 g甲物质的饱和溶液升温到t2 ℃,再加 g甲物质,溶液达到饱和。
(3)t2 ℃时,甲溶液中含有少量丙,要想提纯甲,用 结晶法。
(4)将t2 ℃时甲、乙、丙的饱和溶液降温到t1 ℃,所得溶液中溶质的质量分数由大到小的顺序为 。
10.某兴趣小组利用家中的材料探究影响物质溶解性的因素,实验设计(实验所需仪器略)如下:
Ⅰ.称取一定质量的冰糖,研磨成粉末备用。
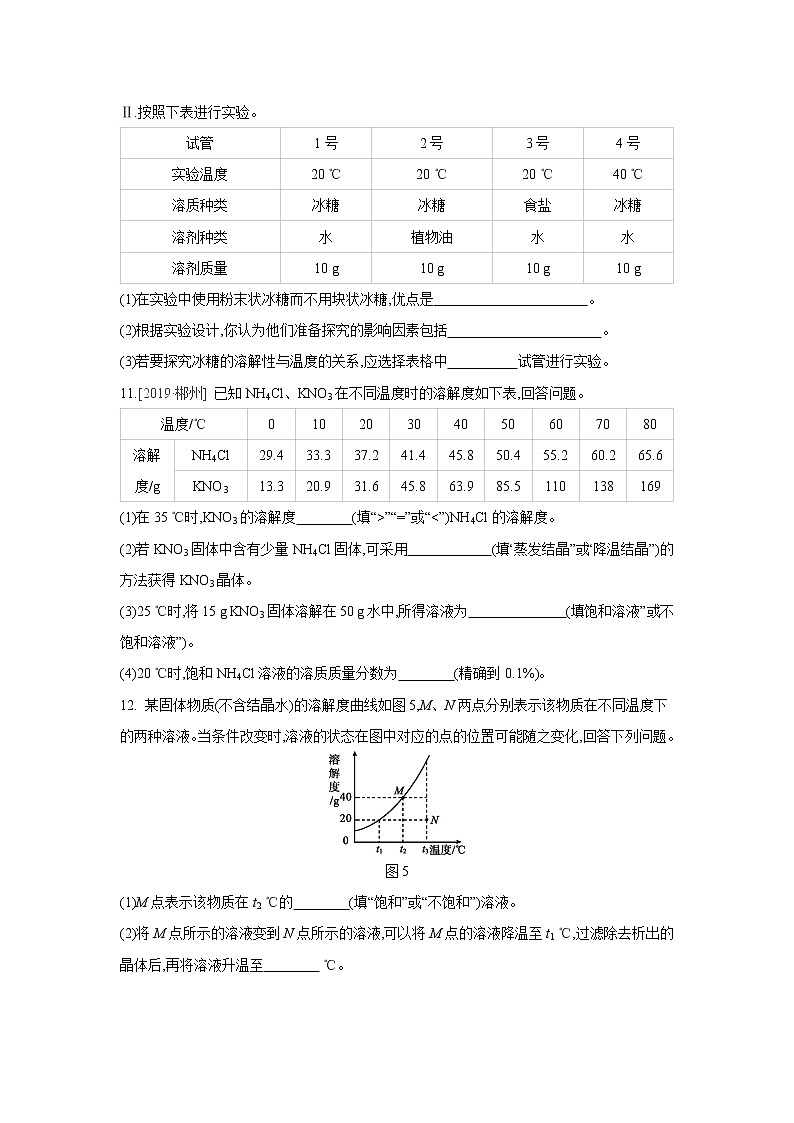
Ⅱ.按照下表进行实验。
试管 | 1号 | 2号 | 3号 | 4号 |
实验温度 | 20 ℃ | 20 ℃ | 20 ℃ | 40 ℃ |
溶质种类 | 冰糖 | 冰糖 | 食盐 | 冰糖 |
溶剂种类 | 水 | 植物油 | 水 | 水 |
溶剂质量 | 10 g | 10 g | 10 g | 10 g |
(1)在实验中使用粉末状冰糖而不用块状冰糖,优点是 。
(2)根据实验设计,你认为他们准备探究的影响因素包括 。
(3)若要探究冰糖的溶解性与温度的关系,应选择表格中 试管进行实验。
11.[2019·郴州] 已知NH4Cl、KNO3在不同温度时的溶解度如下表,回答问题。
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | |
溶解 度/g | NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 | 60.2 | 65.6 |
KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 | 169 | |
(1)在35 ℃时,KNO3的溶解度 (填“>”“=”或“<”)NH4Cl的溶解度。
(2)若KNO3固体中含有少量NH4Cl固体,可采用 (填“蒸发结晶”或“降温结晶”)的方法获得KNO3晶体。
(3)25 ℃时,将15 g KNO3固体溶解在50 g水中,所得溶液为 (填“饱和溶液”或“不饱和溶液”)。
(4)20 ℃时,饱和NH4Cl溶液的溶质质量分数为 (精确到0.1%)。
12. 某固体物质(不含结晶水)的溶解度曲线如图5,M、N两点分别表示该物质在不同温度下的两种溶液。当条件改变时,溶液的状态在图中对应的点的位置可能随之变化,回答下列问题。
图5
(1)M点表示该物质在t2 ℃的 (填“饱和”或“不饱和”)溶液。
(2)将M点所示的溶液变到N点所示的溶液,可以将M点的溶液降温至t1 ℃,过滤除去析出的晶体后,再将溶液升温至 ℃。
(3)t2 ℃时,若M点所示溶液的质量为70 g,其中含溶质 g,再将该溶液降温到t1 ℃,溶液的溶质质量分数变为 (保留一位小数)。
(4)当恒温蒸发溶剂时,M、N两点的位置变化正确的是 (填字母)。
A.M、N两点均不动
B.M、N两点均垂直上移
C.M点沿曲线下移,N点垂直上移
D.M点不动,N点垂直上移至曲线,不再变动
13.甲、乙两种固体物质的溶解度曲线如图6Ⅰ所示。
图6
(1)t1 ℃时,溶解度的大小关系为:甲 (填“>”“<”或“=”)乙。
(2)t2 ℃时,配制180 g甲物质的饱和溶液,需称量甲的质量为 g。
(3)由图Ⅱ推测硝酸钾是图Ⅰ中的 物质。
(4)图Ⅱ“某种操作”前后的溶液状态变化过程可以在图Ⅰ中表示为 (填字母)。
A.b点→a点 B.c点→a点
C.b点→c点 D.c点→d点
答案
1.A [解析] 20 ℃时氯化钠的溶解度为36.0 g,根据溶解度的意义可知,每100 g水中最多溶解36.0 g氯化钠,则用50.0 g水配制该温度下的氯化钠饱和溶液需要氯化钠的质量为18.0 g。
2.C [解析] 气体的溶解度主要受温度和压强的影响,随温度的升高而减小,随温度的降低而增大;随压强的增大而增大,随压强的减小而减小。
3.B
4.D [解析] 60 ℃时,硝酸钾的溶解度为110 g,其饱和溶液中溶质质量分数为×100%=52.4%,不能配制成60%的硝酸钾溶液。
5.B [解析] 实验一中硝酸钾在低温下不溶,在加热时溶解,说明物质的溶解性与温度有关;实验二中将氯化钠分别加入酒精和水中,是在探究溶剂种类对物质溶解性的影响;实验二的变量是溶剂种类,其他量必须相同。
6.C [解析] 20 ℃时,64 g水中最多溶解23.04 g氯化钠,故该溶液的质量是87.04 g。
7.D [解析] 由溶解度曲线可得出,温度低于t2 ℃时,物质Y的溶解度大于X;Y的溶解度随温度的升高而减小;a点表示t1 ℃时X的饱和溶液,表示t1 ℃时Y的不饱和溶液。
8.B [解析] 室温时,将生石灰加入饱和石灰水中,生石灰能和水反应生成氢氧化钙,反应放出热量,溶液的温度升高,氢氧化钙的溶解度减小。
9.(1)t1 ℃时,甲、丙两物质的溶解度相等
(2)15 (3)降温
(4)乙>甲>丙
[解析] (3)甲物质的溶解度随温度的升高而增大,丙物质的溶解度随温度的升高而减小,甲溶液中含有少量丙,提纯甲可用降温结晶的方法。(4)t1 ℃时,乙物质的溶解度最大,甲、丙物质的溶解度相等;温度由t2 ℃降到t1 ℃,甲、乙两物质的溶解度减小,丙物质的溶解度增大,则丙物质应该按照t2 ℃时的溶解度计算,所以将t2 ℃时甲、乙、丙的饱和溶液分别降温至t1 ℃,所得溶液中溶质的质量分数由大到小的顺序为乙>甲>丙。
10.(1)粉末状冰糖比块状冰糖的溶解速率快,节约实验时间
(2)温度、溶剂的种类、溶质的种类
(3)1号和4号
11.(1)> (2)降温结晶 (3)不饱和溶液
(4)27.1%
[解析] (2)硝酸钾的溶解度受温度变化影响较大,而NH4Cl的溶解度受温度变化影响较小,若KNO3固体中含有少量NH4Cl固体,可采用降温结晶的方法获得KNO3晶体。(3)25 ℃时,硝酸钾的溶解度在31.6~45.8 g之间,50 g水中最多能溶解硝酸钾15.8~22.9 g,所以25 ℃时,将15 g KNO3固体溶解在50 g水中,所得溶液为不饱和溶液。(4)饱和溶液中溶质质量分数=×100%,20 ℃时,饱和NH4Cl溶液的溶质质量分数为×100%=27.1%。
12.(1)饱和 (2)t3 (3)20 16.7% (4)D
[解析] (3)t2 ℃时,M点的溶解度是40 g,所以若M点所示溶液的质量为70 g,其中含溶质20 g。将该溶液降温到t1 ℃,溶液仍为饱和溶液,溶液的溶质质量分数变为×100%=16.7%。(4)M点对应的是该物质的饱和溶液,N点对应的是该物质的不饱和溶液,所以当恒温蒸发溶剂时,M点不动,N点垂直上移至曲线,不再变动。
13.(1)> (2)80 (3)甲 (4)B
[解析] (1)t1 ℃时甲的溶解度曲线在乙的上方,说明该温度下甲的溶解度大于乙的溶解度。(2)t2 ℃时甲的溶解度为80 g,所以该温度下配制180 g甲物质的饱和溶液,需称量甲的质量为80 g。(3)由图 Ⅱ 可知,t2 ℃时硝酸钾的溶解度大于60 g,而图Ⅰ中,t2 ℃时甲的溶解度大于60 g,所以硝酸钾是图Ⅰ中的甲物质。(4)图Ⅱ中“某一步操作”是使硝酸钾溶液由不饱和变成饱和,该过程中溶液的质量不变,说明仅通过改变温度使硝酸钾的溶解度变小,即溶液状态变化是c点→a点。
初中鲁教版第二节 金属的化学性质第2课时同步训练题: 这是一份初中鲁教版第二节 金属的化学性质第2课时同步训练题,共7页。试卷主要包含了选择题,填空题,计算题等内容,欢迎下载使用。
初中化学鲁教版九年级下册第二节 碱及其性质第2课时课后测评: 这是一份初中化学鲁教版九年级下册第二节 碱及其性质第2课时课后测评,共6页。试卷主要包含了选择题,填空题,计算题等内容,欢迎下载使用。
鲁教版九年级下册第二节 海水“晒盐“第1课时课后练习题: 这是一份鲁教版九年级下册第二节 海水“晒盐“第1课时课后练习题,共6页。试卷主要包含了选择题,填空题等内容,欢迎下载使用。













