



化学选择性必修2第二章 分子结构与性质第三节 分子结构与物质的性质课文配套课件ppt
展开第2课时 溶解性、手性和无机含氧酸分子的酸性
(1)内因:相似相溶原理(2)外因:影响固体溶解度的主要因素是温度;影响气体溶解度的主要因素是温度和压强。(3)其他因素:A)如果溶质与溶剂之间能形成氢键,则溶解度增大,且氢键越强,溶解性越好。如:NH3。B)溶质与水发生反应时可增大其溶解度,如:SO2。
溶质分子与溶剂分子的结构越相似,相互溶解越容易。 溶质分子的分子间力与溶剂分子的分子间力越相似,越易互溶。
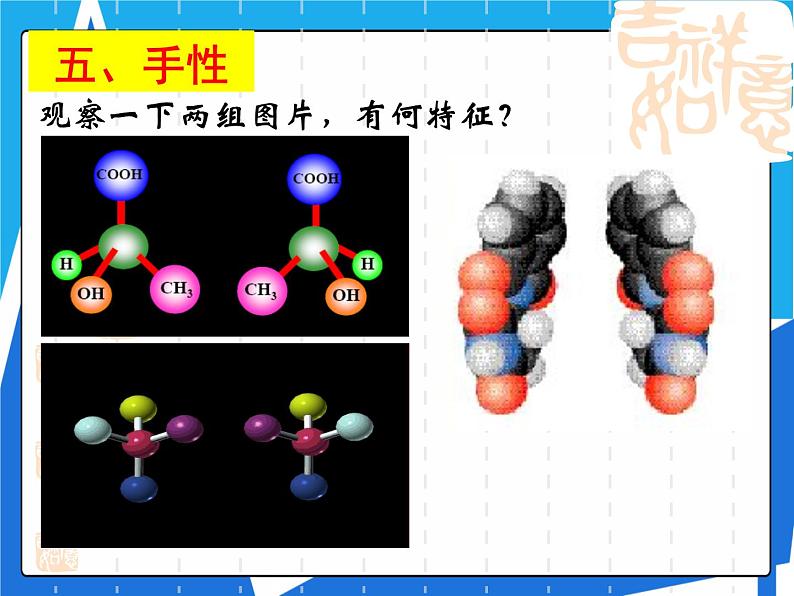
观察一下两组图片,有何特征?
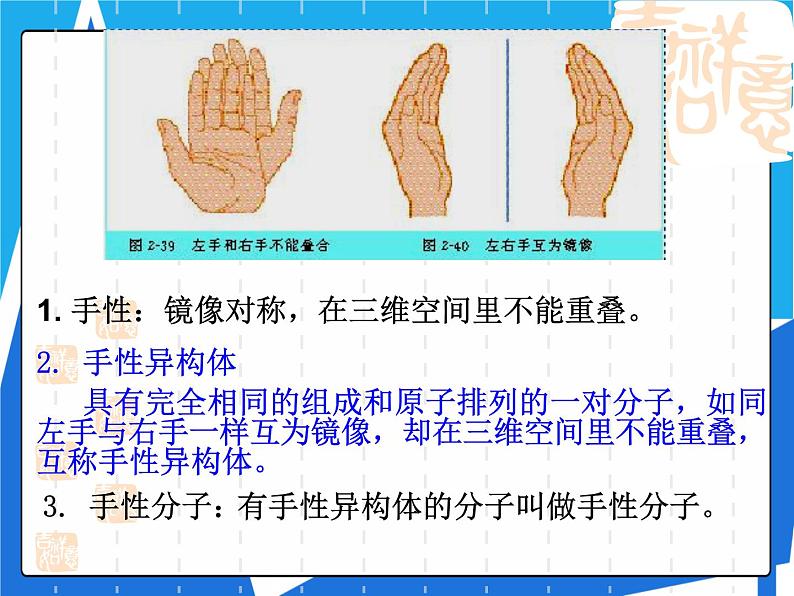
1. 手性:镜像对称,在三维空间里不能重叠。
具有完全相同的组成和原子排列的一对分子,如同左手与右手一样互为镜像,却在三维空间里不能重叠,互称手性异构体。
有手性异构体的分子叫做手性分子。
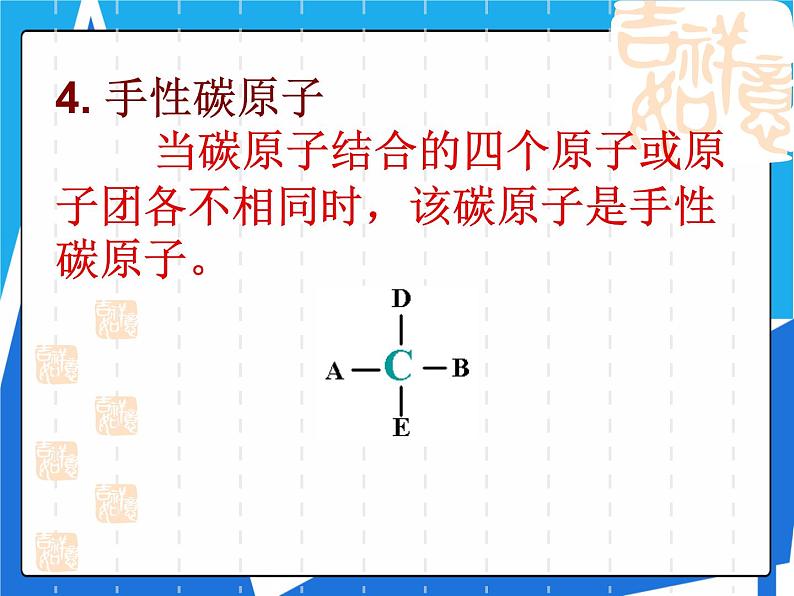
4. 手性碳原子 当碳原子结合的四个原子或原子团各不相同时,该碳原子是手性碳原子。
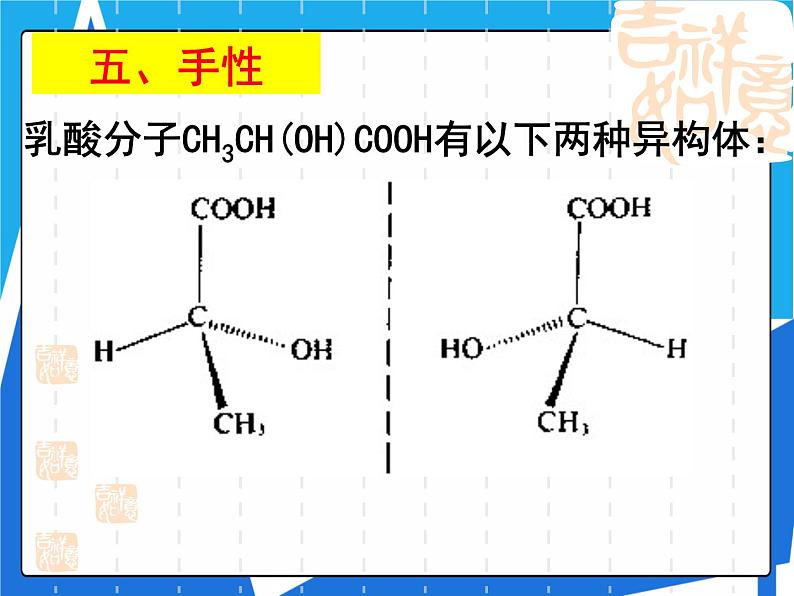
乳酸分子CH3CH(OH)COOH有以下两种异构体:
具有手性的有机物,是因为含有手性碳原子造成的。如果一个碳原子所联结的四个原子或原子团各不相同,那么该碳原子称为手性碳原子,记作﹡C 。
注意:也有一些手性物质没有手性碳原子
5. 判断分子是否手性的依据:(1) 凡具有对称面、对称中心的分子,都是非手性分子。(2)有无对称轴,对分子是否有手性无决定作用。
一般:※ 当分子中只有一个C* ,分子一定有手性。※ 当分子中有多个手性中心时,要借助对称因素。无对称 面,又无对称中心的分子,必是手性分子。
手性分子在生命科学和生产手性药物方面有广泛的应用。如图所示的分子,是由一家德国制药厂在1957年10月1日上市的高效镇静剂,中文药名为“反应停”,它能使失眠者美美地睡个好觉,能迅速止痛并能够减轻孕妇的妊娠反应。然而,不久就发现世界各地相继出现了一些畸形儿,后被科学家证实,是孕妇服用了这种药物导致的随后的药物化学研究证实,在这种药物中,只有图左边的分子才有这种毒副作用,而右边的分子却没有这种毒副作用。人类从这一药物史上的悲剧中吸取教训,不久各国纷纷规定,今后凡生产手性药物,必须把手性异构体分离开,只出售能治病的那种手性异构体的药物。
拓展体验
1. 下列说法不正确的是( )A. 互为手性异构的分子组成相同,官能 团不同B. 手性异构体的性质不完全相同C. 手性异构体是同分异构体的一种D. 利用手性催化剂合成可得到或主要得 到一种手性分子
2. 下列化合物中含有手性碳原子的是( )A.CCl2F2 B.CH3—CH—COOHC.CH3CH2OH D.CH3—OH
六. 无机含氧酸的酸性
1.在同一周期中,处于最高价态的元素,其含氧酸的酸性随原子序数递增,自左至右增强。
如:H3PO4 < H2SO4 < HClO4
高氯酸是非金属含氧酸中酸性最强的无机酸
(一)知识回顾与归纳:
2.在同一主族中,处于相同价态的不同元素,其含氧酸的酸性随成酸元素的原子序数递增,自上而下减弱。
HClO>HBrO>HIO
HClO2>HBrO2>HIO2
HClO3>HBrO3>HIO3
HClO4>HBrO4>HIO4
3.同一元素若能形成几种不同价态的含氧酸,其酸性依化合价的递增而递增;
如:HClO< HClO2< HClO3
把含氧酸的化学式写成(HO)m ROn,就能根据n值判断常见含氧酸的强弱。n=0,极弱酸,如硼酸(H3BO3)。n=1,弱酸,如亚硫酸(H2SO3)。n=2,强酸,如硫酸(H2SO4)、硝酸(HNO3)。n=3,极强酸,如高氯酸(HClO4)。
(二)无机含氧酸酸性规律
某些含氧酸可表示为:(HO)mROn,它的强度与酸中的非羟基氧原子数n有关;n越大,酸性越强:n=0 →弱酸;n=1→中强酸;n=2→强酸;n=3 →超强酸。
含氧酸的强度取决于中心原子的电负性、原子半径、氧化数。 当中心原子的电负性大、原子半径小、氧化数高时,使O-H键减弱,酸性增强。
(HO)mROn,如果成酸元素R不同时,则非羟基氧原子数n值越大,即酸性越强。
化学第三节 分子结构与物质的性质课文内容课件ppt: 这是一份化学<a href="/hx/tb_c4002448_t3/?tag_id=26" target="_blank">第三节 分子结构与物质的性质课文内容课件ppt</a>,共60页。PPT课件主要包含了青蒿素的提取,溶解性,分子的手性,不溶于水,水溶性,O2与O3的物理性质,反应停事件,手性分子,对称性,右盘的蛇-左盘的蛇等内容,欢迎下载使用。
高中化学人教版 (2019)选择性必修2第三节 分子结构与物质的性质背景图ppt课件: 这是一份高中化学人教版 (2019)选择性必修2第三节 分子结构与物质的性质背景图ppt课件,共16页。PPT课件主要包含了目标一溶解性,溶解性,压强等,③从分子结构角度,分子的极性,“相似相溶”,分子的结构相似,②化学反应,非极性溶剂,极性溶剂等内容,欢迎下载使用。
高中化学人教版 (2019)选择性必修2第三节 分子结构与物质的性质授课ppt课件: 这是一份高中化学人教版 (2019)选择性必修2第三节 分子结构与物质的性质授课ppt课件,文件包含人教版高中化学选择性必修2第2章第3节基础课时9氢键溶解性分子的手性课件ppt、人教版高中化学选择性必修2第2章第3节基础课时9氢键溶解性分子的手性学案doc等2份课件配套教学资源,其中PPT共60页, 欢迎下载使用。













