






初中人教版课题2 溶解度多媒体教学ppt课件
展开如何定义饱和溶液、不饱和溶液?怎样判断溶液是否饱和的方法?饱和溶液和不饱和溶液如何相互转化?饱和溶液、不饱和溶液与浓、稀溶液关系如何?
最多能溶解多少氯化钠,是无限制的溶解吗
加热后,硝酸钾又能溶解了
可溶物在一定的水中不能无限的溶解
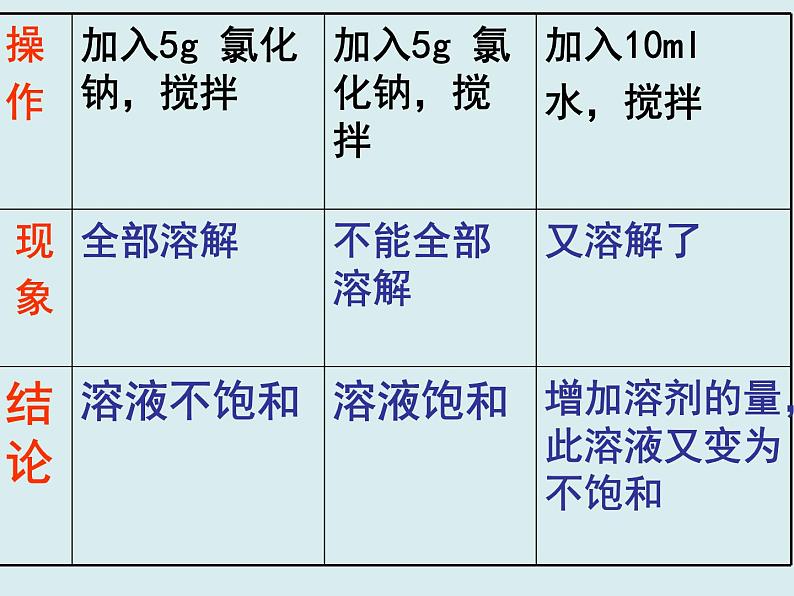
温度升高,溶液变为不饱和
增加溶剂的量,溶液变为不饱和
冷却热的饱和溶液时,硝酸钾晶体从溶液中析出
一、饱和溶液、不饱和溶液
1.定义: 在一定温度下,向一定量溶剂里加入某溶质,当溶质不能继续溶解时,所得到的溶液叫做饱和溶液;还能继续溶解的的溶液,叫做不饱和溶液。
不能继续再溶解某种溶质的溶液称为饱和溶液;还能继续再溶解某种溶质的溶液称为不饱和溶液
在一定的温度下,一定量的溶剂中,
这种溶质在这种溶剂里的
饱和溶液的前提条件:在一定温度下,一定量的溶剂
在上面的前提条件下,关键还要看是否能继续溶解
必须说明是“这种溶质”的饱和溶液。
1、实验①中是什么条件改变后使溶液的饱和情况发生了变化?2、实验②中是什么条件改变后使溶液的饱和情况发生了变化?3、实验说明了什么?
4、你认为在饱和溶液和不饱和溶液的定义中应限定什么条件?能重新给饱和溶液和不饱和溶液下一个定义吗?
某溶质的饱和溶液对于其他物质而言则是不饱和的
指出下列各题的错误之处,并加以改正:1.不能再溶解某种溶质的溶液叫饱和溶液;
在一定温度.一定量的溶剂中,不能…….
不一定,有可能刚好达到饱和.
2.装有饱和溶液的瓶的瓶底,一定有这种溶质的固体;
2、不饱和溶液与饱和溶液间的转化关系
判断硝酸钾溶液是否饱和的方法:
饱和溶液与不饱和溶液相互转化的方法
夏天晒盐 冬天捞碱
你能说说它们之间的相同点和不同点吗?
相同点:都是食盐溶液,溶质是食盐,溶剂是水。
含有较多溶质的溶液叫浓溶液,含有较少溶质的溶液叫稀溶液。
饱和溶液是否一定是浓溶液?不饱和溶液是否一定是稀溶液?
不同点:A是食盐的不饱和溶液,溶质比较少 B是食盐的饱和溶液。溶质比较多。
饱和溶液不一定是浓溶液,不饱和溶液不一定是稀溶液
浓溶液 稀溶液
不饱和溶液 饱和溶液
稀溶液 浓溶液
不饱和溶液 饱和溶液
结论:1.对于不同溶质来说:饱和溶液不一定是浓溶液,不饱和溶液也不一定是稀溶液。2. 在同一条件下,对于同一种溶质来说,饱和溶液要比不饱和溶液浓些。
浓溶液一定是饱和溶液吗? 稀溶液一定是不饱和溶液吗?
20℃时,在100克水中达到饱和时溶解不同物质的质量:
判断:1、 20℃时,在100克水中加入0.165克的氢氧化钙,充分溶解所得的溶液是 (浓溶液或稀溶液),是 (饱和溶液或不饱和溶液)。2、 20℃时,在100克水中加入0.1克的氢氧化钙,充分溶解所得的溶液 是 (浓溶液或稀溶液),是 (饱和溶液或不饱和溶液)。3 、 20℃时,在100克水中加入加入220克的硝酸银固体,充分溶解所得的溶液是 (浓溶液或稀溶液),是 (饱和溶液或不饱和溶液)。 4、20℃时,在100克水中加入加入222克的硝酸银固体,充分溶解所得的溶液是 (浓溶液或稀溶液),是 (饱和溶液或不饱和溶液)。
饱和溶液、不饱和溶液与浓溶液、稀溶液之间的关系
饱和溶液不一定是浓溶液,可能是稀溶液.2. 不饱和溶液不一定是稀溶液,可能是浓溶液.3.对于同一种溶质的溶液来说,在一定温度下,饱和溶液比不饱和溶液浓 .
降温.减少溶剂.加溶质
不饱和溶液:饱和溶液:
在一定条件下,能否继续溶解该溶质?
在一定温度下,一定量溶剂里还能继续溶解某种溶质的溶液叫这种溶质的不饱和溶液。 在一定温度下,一定量溶剂里不能再继续溶解某种溶质的溶液叫这种溶质的饱和溶液。
溶质较多的溶液溶质较少的溶液
二、饱和溶液、不饱和溶液 浓溶液、稀溶液
对于不同物质来说,饱和溶液不一定是浓溶液,不饱和溶液也不一定是稀溶液。 只是在同一条件下,对于同一种物质而言,饱和溶液要比不饱和溶液要浓些。
1、关于饱和溶液的说法中正确的是( ) A.含有溶质很多的溶液 B. 在一定温度下,一定量的溶剂里,不能再继续溶解某种溶质的溶液 C.不能继续溶解某种溶质的溶液 D.还能继续溶解某种溶质的溶液
2、若要将一杯不饱和KNO3溶液变为饱和溶液,下列方法不正确的( ) A、加KNO3 固体 B、蒸发水 C、倒出一部分溶液 D、降低温度
3、将a g 氯化钠粉末放入b g 水中,充分搅拌后,所得溶液的质量为( ) A、=(a+b)g B、<(a+b)g C、>(a+b)g D、≤(a+b)g
4、下列所例举的是20℃时氯化钠溶解的一组数据:
从上述事实可以看出,其中 溶液是20℃时氯化钠的不饱和溶液; 溶液是20℃时氯化钠的饱和溶液;在20℃时10克水中溶解 克氯化钠刚好达到饱和溶液。
现有一瓶接近饱和的硝酸钾溶 液,使它变成饱和溶液的方法中, 不正确的是( )
A、加入硝酸钾固体 B、降低溶液的温度C、蒸发一部分溶剂后再恢复到原温度 D、用滴管吸出一部分溶液
(1) 一般说来,可以向原溶液中再加入少量原溶质,如果不能再溶解,则说明是饱和溶液;如果还能再溶解,则说明是不饱和溶液。(2)有未溶解的溶质时为饱和溶液。
判断溶液是否饱和的方法:
饱和溶液一定是浓溶液,不饱和溶液一定是稀溶液吗?
食盐在水中溶解能力较大,而熟石灰在水溶解能力很差。
对于不同溶质来说,浓溶液不一定是饱和溶液,稀溶液不一定是不饱和溶液。 对于同一种溶质来说,在一定温度时,饱和溶液一定比不饱和溶液要浓。
1.不同物质在水中溶解能力是否相同?举例说明。
答:不同。例如食盐在水中溶解能力较大,而熟石灰在水溶解能力很差。
2.同种物质在不同溶剂中溶解能力是否相同?
答:不同。例如油易溶于汽油而难溶于水。
通常把一种物质溶解在另一种物质里的能力叫做溶解性。
溶解性的大小跟溶质和溶剂的性质有关。且受温度等外界条件的影响。
如何比较两种物质的溶解能力大小?
比较不同物质的溶解能力,应该控制的条件有:
与溶质和溶剂的性质、及温度有关
一种物质溶解在另一种物质的能力
溶解性能力的大小常用溶解度来表示
定量比较固体溶解能力大小的要素:
讨论:设计实验——怎样比较食盐和蔗糖哪一个更易溶于水?
在一定温度下,某固态物质的在100克溶剂里达到饱和状态时所溶解的质量,叫做这种物质在这种溶剂里的溶解度(符号S)。
100克溶剂(一般指水)
固体的溶解度的四要素:
例:蔗糖在20℃是的溶解度是203.9g。
在20℃时,100g水中最多可溶解203.9g蔗糖。
在20℃时,100g水中溶解203.9g蔗糖,溶液达到饱和。
从溶解度可以获得的信息
食盐在20℃时的溶解度S=36克在 ___℃时,食盐(氯化钠)在_____ 克水里达到 ____ 时溶解了____克。此时的溶液一定是______溶液。该溶液的质量为_________。溶液中食盐(NaCl)的质量为________ ,水为___ 。归纳:若某物质在某温度时的溶解度为S克,则此时M质 = S克,M剂 = 100克,M液= M质+M剂 = 100+S 克
其含义是:在20ºC时,该物质在100克水中达 到饱和状态时溶解的质量为.5克。 或说:在20ºC时,该物质在100克水中最多 能溶解.5克。
例1,某物质在20ºC的溶解度为.5克,其含义是什么?
例:判断正误:1.l00g水中最多溶解38g氯化钠,所以氯化钠在水中的溶解度是38g。( )2.在10℃时,烧杯内水中最多溶有140g硝酸铵,所以硝酸铵在水中的溶解度是140g。( )3.在60℃,100g水中溶有75g硝酸钾,所以60℃时硝酸钾的溶解度为75g。( )4.60℃,100g水中最多溶解124g硝酸钾,所以硝酸钾在这温度下的溶解度是124。( )
1、在20℃时,100g水中溶解36g氯化钠溶液达到饱和,则20 ℃时氯化钠溶解度是____g。
2、在0℃时,100g水中最多可溶解13.3g硝酸钾,则0℃时硝酸钾溶解度是____g。
3、20℃时硝酸钾的溶解度是31.6g,这句话的含义是什么?将其关系代入下表:
4、20℃时硝酸钾的溶解度是31.6g,求该温度下饱和溶液中溶质的质量分数。
2、溶解度与溶解性的关系
练习: 1、不溶物就是绝对不溶于水的物质。此话是否正确? 2、20℃时碳酸钙的溶解度是0.0013g,所以碳酸钙是___溶物质。 3、20℃时氯化钠的溶解度是36g,则氯化钠属于( ) A.易溶 物质 B.可溶物质 C.微溶物质 D.难溶物质
下列有关溶解度的说法正确的是( )A、100克水中溶解了20克物质刚好达到饱和,则该 物质的溶解度是20克。B、20℃时,100g水中溶解了10g某物质,在20℃时,该物质的溶解度是10g。C、20℃时,50g水中最多可溶解18g食盐,在20℃ 时食盐的溶解度是18g。D、20℃时,31.6g硝酸钾需要100g水才能溶解,则20℃时硝酸钾的溶解度是31.6g。
错。没有指明溶液是饱和状态。
错。 100g水里最多可溶解36克食盐,20℃时食盐的溶解度是36g。
溶解度随温度变化有两种表示方法:①列表法; ②溶解度曲线。
4.固体溶解度的表示方法
⑴溶解度曲线: 由于固体物质的溶解度随温度变化而变化,随温度一定而一定,这种变化可以用溶解度曲线来表示。我们用纵坐标表示溶解度,横坐标表示温度,绘出固体物质的溶解度随温度变化的曲线,这种曲线叫做溶解度曲线。
硝酸钾在不同温度时的溶解度:
3、溶解度的表示方法:
熟石灰的溶解度随温度升高而降低
固体的溶解度曲线意义:
横坐标60,纵坐标110 的交点表示什么意义?
b.能比较同一温度下不同物质S的大小
c.交点表示该温度下两物质的S相等
d.表示物质的S随温度的变化关系
a.表示某物质在不同温度下的S
固体物质溶解度受温度变化规律:
a、大多数固体物质溶解度随温度升高而增大 例如 硝酸钾等。
b、少数固体物质溶解度受温度影响不大, 例如食盐。
c、极少数固体物质溶解度随温度升高反减小例如熟石灰。
右图是A.B两种物质的溶解度曲线,试回答下列问题(1)t1ºC时,A 的溶解度 B 的溶解度.(填< > 或=)(2)当A、B两物质的溶液接近饱和时,采用增加溶质、蒸发溶剂、降低温度的方法可以达到饱和的是 物质的溶液。
1:同种物质在不同温度下的溶解度不同。
2:曲线的交点表示这两种物质在该温度下的溶解度相同。
3:曲线越陡,该物质的溶解度受温度影响越大。
找一找50度各物质的溶解度
1、横坐标60,纵坐标110 的交点表示什么意义?
2.比较硝酸钠与硝酸钾的溶解度大小
在680C时,NaNO3与KNO3的溶解度相等
温度大于680C时, KNO3的溶解度大于NaNO3
温度小于680C时,NaNO3的溶解度大于KNO3
氯化铵、氯化钾、氯化钠、硼酸
讨论: 固体物质溶解度受温度变化影响情况:
大多数固体物质溶解度随温度升高而增大,例如 硝酸钾等。
少数固体物质溶解度受温度影响不大,例如食盐。
极少数固体物质溶解度随温度升高反而减小,例如熟石灰。
从溶解度曲线分析结晶情况
1、降温结晶(又叫冷却热饱和溶液法)
适用于溶解度随温度变化较小的物质如:NaCl
适用于溶解度随温度变化较大的物质如:KNO3
给熟石灰的饱和溶液升高温度会有什么现象?为什么?
变浑浊,因为熟石灰的溶解度随温度升高而减小,升温后会有熟石灰固体析出
甲、乙两种固体的溶解度曲线如下图。现将两试管分别装入甲、乙两种物质的饱和溶液(试管底部均有未溶解的固体),再放进盛有冰水的烧杯里, 则下列说 法正确的是( ) A.甲溶液中溶质的质量分数增大 B.乙溶液中剩余的固体减少 C.试管里甲、乙物质的溶解度都增大 D.试管里甲、乙两溶液中的溶质都减少
右图是A.B两种物质的溶解度曲线,试回答下列问题(1)t1ºC时,A 的溶解度 B 的溶解度.(填< > 或=)(2)A、B两物质饱和溶液溶质的质量分数相等的温度是 ºC。(3)当A、B两物质的溶液接近饱和时,采用增加溶质、蒸发溶剂、降低温度的方法可以达到饱和的是 物质的溶液。
硝酸钾固体中含有少量氯化钠,如何提纯硝酸钾?
滤液中:大部分NaCl 少量KNO3
降温结晶法提纯硝酸钾(又叫冷却热饱和溶液法)
2.右图是A.B.C三种固体物质的溶解度曲线,回答下列问题:(1)从B溶液中得到晶体宜采用的方法是(2)除去A中混有的少量B的方法是(3)除去B中混有的少量A的方法是( 4)分离B与C混合物采用的方法是
溶解,蒸发结晶,过滤,
配制热饱和溶液,降温结晶,过滤
同种溶质在不同的溶 剂中的溶解能力不同
不同的溶质在同种溶 剂中的溶解能力不同
易溶 、可溶 、 微溶 、 难(不)溶
影响因素 (温度、压强)
滤液液面低于滤纸的边缘
粗盐的主要成分:不溶性泥沙、氯化钠
1、使用什么方法可将粗盐中的泥沙除去?
2、除去泥沙后,再怎样操作才能得到食盐晶体?
蒸发操作过程中的注意事项:
a、注意蒸发皿的溶液不超过蒸发皿容积的2/3;b、加热过程中要不断搅拌,以免溶液溅出;c、不能蒸干,应当析出大量晶体时就应熄灭酒精灯,利用余热蒸发至干
通常讲的气体溶解度是指该气体在压强为101KPa, 一定温度时溶解在1体积水里达到饱和状态时的气体体积。
0℃时,氧气的溶解度为0.049的含义是什么?
在0℃,氧气压强为101kPa时,1体积水最多能溶解0. 049体积氧气
1标准大气压下,20℃时部分气体的溶解度
气体溶解度一般随压强增大而增大,压强减小而减小。
气体溶解度一般随温度升高而减小,温度降低而增大。
1、影响气体溶解度的因素:
汽水中含有大量二氧化碳
[讨论] 天气闷热时,鱼儿为什么总爱在水面上进行呼 吸?
为什么要向鱼缸中通入空气
把水喷向空中可以增加养鱼池水中氧气的溶解量
1.固体溶解度与气体溶解度的概念表示有何不同之处?为何不同? 2. 增大二氧化碳在水中的溶解度的方法( ) A. 升温增压; B. 升温减压; C. 降温增压; D. 降温减压。
3.下列几种物质①硝酸钾②熟石灰③氧气④二氧化碳 溶解度随温度的升高而增大的是( ) A.①② B.③④ C.①③④ D.只有①
1.在 温度下,在 的溶剂里,不能再溶解某种溶质的溶液叫这种溶质的 ; 叫做这种溶质的不饱和溶液。2.对一杯接近饱和的KNO3溶液,如果变成饱和溶液,可有多种方法,下列方法不能实现其转化的是( )A.蒸发H2O B.加KNO3晶体 C.升高温度 D.降低温度3.关于饱和溶液的说法正确的是( )A.饱和溶液加热时会变成不饱和溶液B.饱和溶液加热时仍然是饱和溶液C.大多数物质的饱和溶液加热时会变成不饱和溶液D.饱和溶液降温时,会有晶体析出4.下列关于饱和溶液的说法中,错误的是( )A.在温度不变时, KNO3饱和溶液不能再溶解KNO3B.在温度升高时,饱和溶液一定能继续溶解溶质C.室温下与固体溶质共存的溶液是这种溶质的饱和溶液D.改变条件可以使饱和溶液变为不饱和溶液
5.某温度下,将 3 g A物质放入7 g水中,得到 10 g溶液,该溶液是( )A.饱和溶液 B.不饱和溶液 C.浓溶液 D.无法确定6.A物质的水溶液已接近饱和,下列措施一定能使该溶液达到饱和的是( )A.升高溶液的温度B.降低溶液的温度C.在温度不变的条件下向溶液中加入A物质,直至不再溶解D.蒸发溶液中的水(温度不变)直至有A析出7.一定温度下,向100g硝酸钾的饱和溶液中加入10g硝酸钾,则溶液的质量是( )A.100g B.110g C.90g D.无法确定8.在10℃时,25g水最多可溶解20gNaNO3,另一温度下,在50g水中加入40gNaNO3没有形成饱和溶液,其原因可能是( )A.温度降低了 B.温度升高了C.溶液质量相对增加了 D.溶质的质量相对减少
9.饱和溶液降低温度析出晶体后,剩下的溶液是( )A.稀溶液 B.浓溶液 C.不饱和溶液 D.饱和溶液10.20℃时,从某饱和蔗糖溶液中取出一部分后,则剩下的溶液一定是( )A.饱和溶液 B.不饱和溶液 C.变浓 D.变稀11.一瓶接近饱和的硝酸钾溶液,逐渐加入硝酸钾固体,下列图像(如图所示)中符合溶液中溶质质量变化的是( )
13.已知20℃时,100 g水中最多能够溶解36 g食盐。①20℃时,将33g食盐放入100 g水中全部溶解,此时所得溶液的质量为________;②再向上述溶液中加入3g食盐,又恰好全部溶解,则原来的溶液为________(填写"饱和溶液"或"不饱和溶液"),此时所得溶液的质量为________;③再向上述溶液中加入3g食盐,所加食盐________(填“能”或“不能”)溶解,此时所得溶液为________________(填写“饱和溶液”或“不饱和溶液”),溶液的质量为________。 14.如图所示,在室温下的饱和食盐水中,放了一个塑料小球,当采取以下几种方法后,请分析小球在液面沉浮的情况。①加入少量食盐晶体;②加入少量水;③把温度升高到30℃。
15.下列的硝酸钾溶液是否饱和?①把硝酸钾晶体放到硝酸钾溶液里,晶体减少,则原溶液为 。②把常温下配制的硝酸钾饱和溶液升温到80℃,则溶液变为 。③在10℃时的硝酸钾溶液中含有少量硝酸钾晶体,则此溶液为 。④将50℃时接近饱和的硝酸钾溶液降温至10℃,则溶液为 。16.室温下的饱和食盐水中,加入食盐固体不能溶解,加入蔗糖能溶解吗?它是蔗糖的饱和溶液吗?
下图是A、B、C三种物质的溶解度曲线。据图回答下列问题:(1)30℃时,A物质的溶解度为______g。 (2)10℃时,三种物质的溶解度从大到小的顺序是____。 (3)____℃时,AB两种物质的溶解度相同。 (4)当温度变化时,溶解度变化最明显的是__ _物质,溶解度变化不大的是_ __物质。
1.固体溶解度是指 。2.要使KNO3溶解度增大,采用的方法是( )A. 增加水 B. 增加KNO3 C. 不断搅拌 D. 升高温度3.在10℃时,某固体物质的溶解度为5g,在此温度下该物质饱和溶液里,下列相互之间的质量比例关系正确的是( )A. 溶液:溶质=:1 B. 溶剂:溶质=19:1C. 溶液:溶剂=20: D. 溶质:溶液=1:204.t℃时,把14g氯化钾饱和溶液蒸干,得到氯化钾4g,t℃时氯化钾的溶解度为( )A. 40g B. 20g C. 140g D. 120g5.已知下列物质在20℃时的溶解度,其中属于微溶物质的是( )A. CaCO3:0.0013g B. NaCl:36g C. Ca(OH)2:0.17g D. KClO3:7.4g
7.在0℃和1标准大气压下,1L水里最多能溶解5L气体A,则0℃时,A的溶解度为( )A.5L B.5 C.500L .要使一瓶氢氧化钙饱和溶液变成不饱和溶液,所应采取的方法是( ) A.升高温度 B.降低温度C.加入一定量蒸馏水 D.静置后过滤9.如图所示,表示物质x在水中的溶解度随温度,压强的变化关系x可能是( )A. NaCl B. CO2 C. Cu(OH)2 D. KNO3
10.生活中的下列现象不能说明气体溶解度随温度升高而减小的是( )A. 烧开水时,沸腾前有气泡逸出 B. 喝下汽水感到有气体冲到鼻腔C. 揭开啤酒瓶盖,有大量泡沫溢出 D. 夏季黄昏,池塘里的鱼常浮出水面11.20℃时,在10g水中溶解6gA物质,下列结论正确的是( )A. 20℃时,A物质的溶解度为60g B. 温度降到5℃时,一定有晶体析出C. A物质属于易溶物质 D. 保持温度不变时,若蒸发掉5g水,则析出3g晶体16.自然界中的某些现象都跟物质的溶解度有关。请根据下列事实推测外界因素如何影响物质的溶解度。请简单解释下列现象:⑴将凉开水倒入鱼缸养鱼,鱼不久会死掉。 ⑵ 加热到20℃时的饱和石灰水,石灰水变浑浊。⑶1999年我国科考队首次在西藏羌北无人区发现,当地进入严冬时,广大冰冻湖泊中析出十分壮观的多面体的碳酸钠晶体。⑷夏天,贮存自来水的瓶子内壁挂满一层气泡。⑸打开汽水瓶盖时,常常有大量气泡涌出。⑹利用蒸发的方法从海水中提取食盐
17.如图所示是A,B,C三种物质溶解度曲线,看图回答:(1)溶解度受温度影响最大的是______,最小的是____;(2)在____℃时,A,B,C物质的溶解度相同,都是_____g,这句话的含义是___ __;(3)当温度在40℃以下时,三种物质的溶解能力大小的顺序是_______。(4)当60℃,把100gA物质放在100g水中充分搅拌,可得饱和溶液_____g.(5)在60℃时,把A,B,C三种物质各40g分别放到100g水中充分搅拌,所得溶液为_ __(饱和或不饱和)溶液,若把该三杯溶液都变为另一状态,在不添加溶质和改变溶剂质量的条件下,可采取什么措施?_____ __
人教版九年级下册第九单元 溶液课题2 溶解度评课课件ppt: 这是一份人教版九年级下册第九单元 溶液课题2 溶解度评课课件ppt,共18页。PPT课件主要包含了探究活动一,全部溶解,我们初步认为,问题2,剩余食盐全部溶解,硝酸钾又继续溶解,问题3,有硝酸钾晶体析出,饱和溶液,加溶剂等内容,欢迎下载使用。
初中化学人教版九年级下册课题2 溶解度教课内容课件ppt: 这是一份初中化学人教版九年级下册课题2 溶解度教课内容课件ppt,共45页。PPT课件主要包含了学习目标,-----饱和溶液,-----不饱和溶液,应该在同一温度下,这样行吗,溶剂的量应该相同,溶液应该达到饱和状态,一定温度,BCA,气体溶解度等内容,欢迎下载使用。
初中化学人教版九年级下册课题2 溶解度教学ppt课件: 这是一份初中化学人教版九年级下册课题2 溶解度教学ppt课件,共60页。PPT课件主要包含了陡升型,缓升型,想一想等内容,欢迎下载使用。













