


2020-2021学年第一节 共价键背景图ppt课件
展开1.认识共价键的本质,原子间通过原子轨道重叠形成共价键。2.熟知共价键的概念与形成,知道共价键的特征。3.能够从不同的角度对共价键分类,会分析σ键和π键的形成及特点。
诺贝尔物理学奖得主理查德·费曼曾说过,假如发生了大灾难,人类全部的科学知识只能概括为一句话传诸后世,那么这句话应该是“万物皆由原子构成”。
早在19世纪中叶,化学家就已经把分子中原子之间的相互作用形象地称作化学键。20世纪初,在原子结构理论的基础上,建立了化学键的电子理论。共价键是现代化学键理论的核心。分子的空间结构和分子之间的作用力是理解分子结构与性质关系的重要内容。
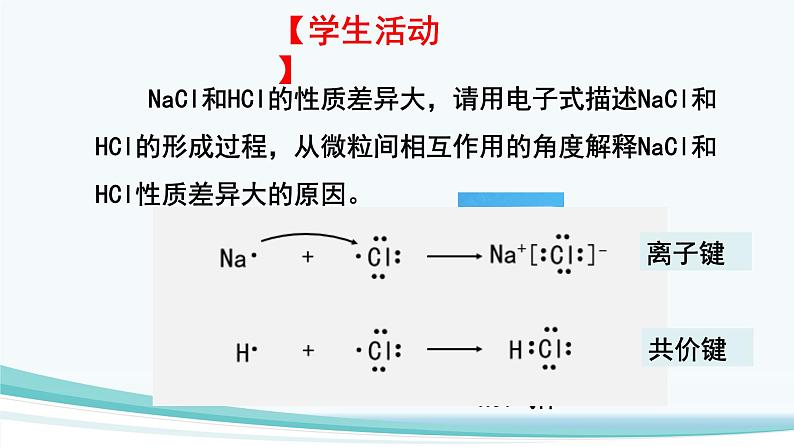
NaCl和HCl的性质差异大,请用电子式描述NaCl和HCl的形成过程,从微粒间相互作用的角度解释NaCl和HCl性质差异大的原因。
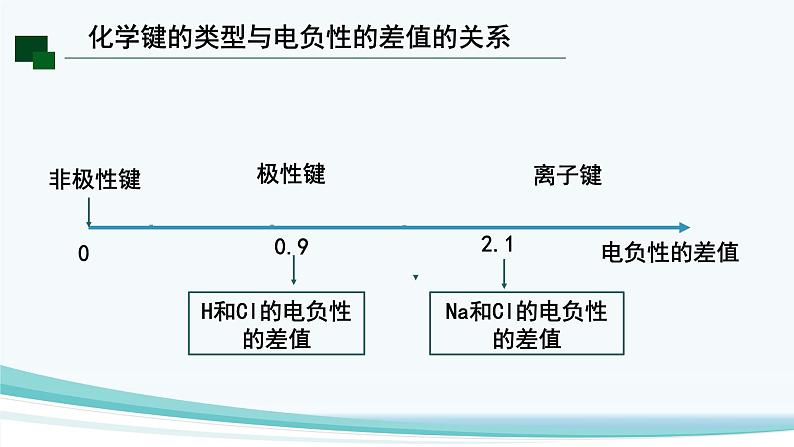
Na和Cl的电负性的差值
H和Cl的电负性的差值
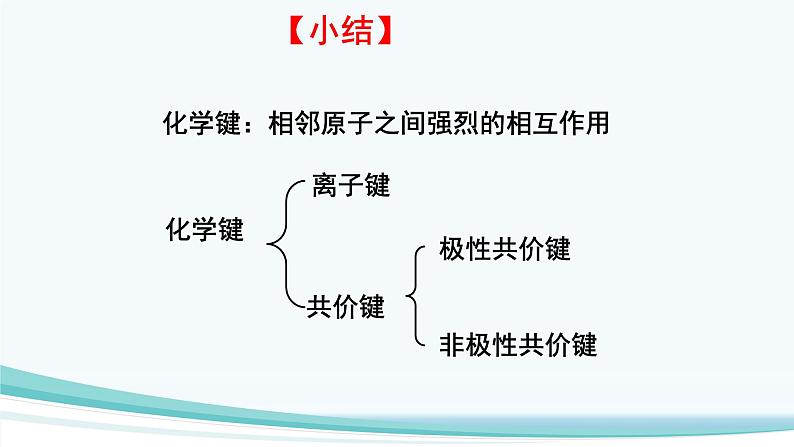
化学键:相邻原子之间强烈的相互作用
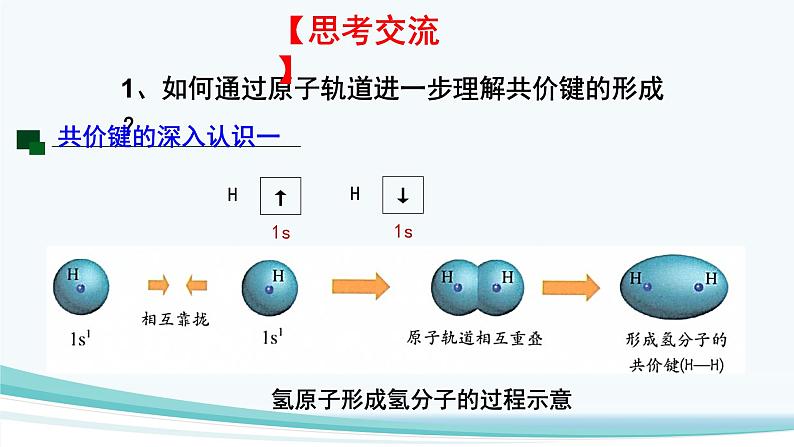
1、如何通过原子轨道进一步理解共价键的形成?
氢原子形成氢分子的过程示意
氢原子形成氢分子的过程
按照共价键的共用电子对理论,一个原子有几个 ,便可和几个 电子配对成键,这就是共价键的饱和性
例如只能有H2、HCl、Cl2等,不可能H3、H2Cl和Cl3等
共价键的饱和性决定了共价化合物的分子组成。
现代价键理论的基本要点:
共价键的方向性决定了共价化合物的立体构型。
2、除了s轨道和s轨道重叠形成共价键外,还能找到其他轨道重叠形成共价键的例子吗?
3、请用橡皮泥制作这些共价键的电子云模型。 通过制作电子云模型,你发现这些共价键有什么特征?
HCl中的共价键是由氢原子提供的未成对电子的1s原子轨道和氯原子提供的未成对电子的3p原子轨道重叠形成的。
Cl2中的共价键是由2个氯原子各提供1个未成对电子的3p原子轨道重叠形成的。
请归纳H-H、H-Cl和Cl-Cl的特点。
4、原子轨道除了以“头碰头”的方式重叠以外,还有没有可能以其他的方式重叠成键?
未成对电子的原子轨道相互靠拢
5、π键与δ键相比有何不同点呢?
①对比两个p轨道形成的δ键和π键可以发现,δ键是由两个原子的p轨道“头碰头”重叠形成的。而π键是由两个原子的p轨道“肩并肩”重叠形成的。
②π键的电子云形状与δ键的电子云形状有明显差别:每个π键的电子云由两块组成,它们互为镜像,这种特征称为镜面对称。
③π键与δ键的强度不同。例如,乙炔、乙烯分子中的π键不如δ键牢固,比较容易断裂。因而含有π键的乙烯、乙炔与只有δ键的乙烷的化学性质不同。
6、如果将π键沿着键轴旋转,会发生什么情况呢?
用电子式表示N2的形成过程,并用原子轨道重叠来解释其共价键的形成过程。
N2中共价三键的形成过程
7、通过氮气中氮氮三键形成过程的分析,如何判断共价键是σ键或是π键?
观察乙烷、乙烯和乙炔的分子结构,它们的分子中的共价键分别由几个σ键和几个π键构成?
①乙烷中含有1个C-C键和6个C-H键,所以乙烷中含有7个σ键; ②乙烯中含有1个C=C键和4个C-H键,即含有5个σ键和1个π键; ③乙炔中含有1个三键和2个C-H键,即含有3个σ键和2个π键;
8、所有共价键都有方向性和饱和性吗?
所有的共价键都有饱和性,但并不是所有的共价键都有方向性,如s-s σ键就没有方向性。
1、氰气的化学式为(CN)2,结构式为NCCN,性质与Cl2相似,下列叙述不正确的是( ) A.在一定条件下可发生加成反应 B.分子中NC键的键长大于C—C键的键长 C.分子只含有2个σ键和4个π键 D.不和NaOH溶液反应
高中化学人教版 (2019)选择性必修2第一节 共价键备课ppt课件: 这是一份高中化学人教版 (2019)选择性必修2第一节 共价键备课ppt课件,共47页。PPT课件主要包含了学习目标,新课导入,NaCl晶体,HCl气体,离子键,共价键,思考讨论,化学键,极性共价键,非极性共价键等内容,欢迎下载使用。
人教版 (2019)选择性必修2第一节 共价键图文课件ppt: 这是一份人教版 (2019)选择性必修2第一节 共价键图文课件ppt,文件包含211共价键第1课时共价键习题精练高二化学同步习题精练人教版2019选择性必修2含解析docx、211共价键第1课时共价键课件精讲高二化学同步课件精讲人教版2019选择性必修2pptx等2份课件配套教学资源,其中PPT共0页, 欢迎下载使用。
人教版 (2019)选择性必修2第二章 分子结构与性质第一节 共价键课堂教学课件ppt: 这是一份人教版 (2019)选择性必修2第二章 分子结构与性质第一节 共价键课堂教学课件ppt,共29页。PPT课件主要包含了教学目标,问题反馈,离子键,共价键,化学键,金属键,成键微粒,共价键的存在,一般为非金属原子,共价键的类型等内容,欢迎下载使用。













