






科粤版九年级下册8.4 常用的盐课堂教学ppt课件
展开“食盐是盐,反之,盐就是食盐。”这一说法对吗?给出理由,并举例说明。
化学:食盐是盐,但是盐不一定是食盐
③用途——调味品、制生理盐水、化工原料、选种、腌渍品 消除积雪。
1、氯化钠(化学式NaCl)
②白色晶体,易溶于水,有咸味,溶液呈中性。
2、碳酸钙(CaCO3)
②物理性质:白色粉末,不溶于水
①大理石、石灰石、鸡蛋壳、贝壳的主要成分
CaCO3+2HCl=CaCl2+H2O+CO2↑
CaCO3 === CaO + CO2↑
④建筑装饰材料;补钙剂;制生石灰制熟石灰的原料、水泥,炼铁、炼钢的原料。
3、碳酸钠(Na2CO3)
②物理性质:白色粉末,易溶于水。
③化学性质:A.碳酸钠的水溶液呈碱性,使紫色石蕊变蓝,使无色酚酞变红
Na2CO3 + 2HCl ==2NaCl + H2O + CO2↑
实验现象:有大量气泡产生
C.与碱(溶液)反应:
Na2CO3 + Ca(OH)2 ==2NaOH + CaCO3↓
实验现象:有白色沉淀产生
D.与盐(溶液)反应:
Na2CO3 + CaCl2 ==2NaCl + CaCO3↓
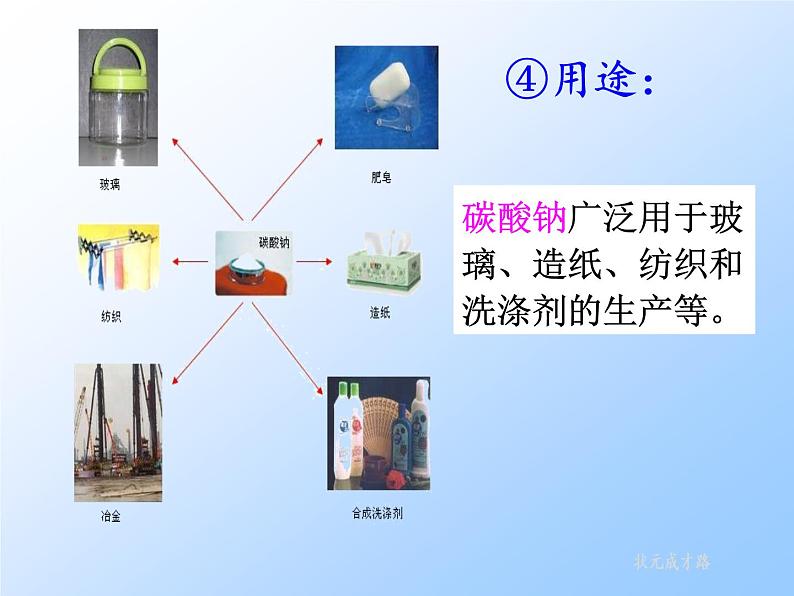
碳酸钠广泛用于玻璃、造纸、纺织和洗涤剂的生产等。
3.碳酸氢钠(NaHCO3)
②物理性质:白色粉末,易溶于水的
NaHCO3 + HCl ==NaCl + H2O + CO2↑
2NaHCO3 Na2CO3+H2O+CO2↑
A.碳酸氢钠水溶液呈碱性,可以使紫色石蕊溶液变蓝,无色酚酞溶液变红
发酵粉的主要成分,治疗胃酸过多症的一种药剂,做灭火剂的原料。
发明了将制碱与制氨结合起来的联合制碱法(又称侯氏制碱法)
侯德榜为纯碱和氮肥工业技术的发展做出了杰出的贡献
总结得出:纯碱叫碱不是碱,它是盐,水溶液显碱性。
阅读教材P245的知识视窗
Na2CO3+2HCl=2NaCl+ CO2↑+H2O
NaHCO3+HCl= NaCl+ CO2↑+H2O
CaCO3+ 2HCI = CaCI2 + CO2↑+ H2O
观察:三个反应有什么共同特点?
(1)检验试剂:稀盐酸和澄清石灰水(2)检验方法:取盐的样品少量于试管中,滴加稀盐酸,若有气泡产生,将生成的气体通入澄清的石灰水,若石灰水变浑浊,则证明原盐的样品中含有 (或 )。
碳酸盐【CO32-或HCO3-】应如何检验?
1、盐的组成有什么特点?2、不同盐各由什么相关的酸和碱反应得到的?并完成填空。
【总结】盐根据阳离子和阴离子的不同的分类。
Na2SO4 K2CO3 Mg(NO3)2 FeCl3 NH4Cl
阳离子是金属离子(或铵根离子),阴离子是酸根离子
根据阳离子不同,盐可以分为钠盐、钾盐、镁盐、铁盐、铵盐等。
根据阴离子不同,盐可以分为硫酸盐、碳酸盐、硝酸盐等
不同的盐可以由对应的酸和碱发生中和反应得到
1 下列物质中,不属于盐的是( ) A.硝酸钾 B.碳酸钙 C.氯化钾 D.硫化氢
2. 只用水不能鉴别出的一组物质是( ) A.Na2SO4 和 CuSO4 B. CaCO3 和 Na2CO3 C.BaCl2 和 KNO3 D.浓硫酸 和 稀硫酸
初中化学科粤版九年级下册8.4 常用的盐图片ppt课件: 这是一份初中化学科粤版九年级下册<a href="/hx/tb_c12510_t3/?tag_id=26" target="_blank">8.4 常用的盐图片ppt课件</a>,共20页。
科粤版九年级下册8.4 常用的盐背景图课件ppt: 这是一份科粤版九年级下册<a href="/hx/tb_c12510_t3/?tag_id=26" target="_blank">8.4 常用的盐背景图课件ppt</a>,共21页。
初中化学科粤版九年级下册第八章 常见的酸、碱、盐8.4 常用的盐精品课件ppt: 这是一份初中化学科粤版九年级下册第八章 常见的酸、碱、盐8.4 常用的盐精品课件ppt,共22页。PPT课件主要包含了学习目标,新课导入,纯碱碳酸钠,大理石碳酸钙,食盐氯化钠,小苏打碳酸氢钠,几种常见盐,新课讲解,洗衣粉,造纸原料等内容,欢迎下载使用。













