

2021年高考化学三轮冲刺《金属及其化合物》练习二(含答案)
展开下列是部分矿物资源铝土矿(主要含有氧化铝、氧化铁)和黄铜矿(主要成分CuFeS2)的利用及产品生产流程,有关说法不正确的是( )
A.除杂过程中铝元素的存在形式的变化可以如下:Al2O3―→AlOeq \\al(-,2)―→Al(OH)3―→Al2O3
B.Al和Cu(精)均在电解槽的阴极获得
C.粗铜炼制过程中反应2CuFeS2+O2eq \(=====,\s\up7(高温))Cu2S+2FeS+SO2,每转移1.2 ml电子,
则有0.2 ml硫被氧化
D.若电解法分别制铝和铜的过程中转移电子数相等,理论上获得的铝和铜的物质的量之比为3:2
下列叙述中不正确的是
A.向含有CaCO3沉淀的水中通入CO2至沉淀恰好溶解,再向溶液中加入NaOH饱和溶液,又有CaCO3沉淀生成
B.向Na2CO3溶液中逐滴加入溶质物质的量相等的稀盐酸,生成的CO2与原Na2CO3的物质的量之比为1∶2
C.等质量的NaHCO3和Na2CO3分别与足量盐酸反应,在同温同压下,生成的CO2体积前者大
D.向Na2CO3饱和溶液中通入CO2,有NaHCO3结晶析出
下列物质组合中,既能和酸反应又能和碱反应的化合物共有( )
①(NH4)2CO3 ②Al2O3 ③Al2(SO4)3 ④Al ⑤NaHSO3 ⑥Al(OH)3
A.3种 B.4种 C.5种 D.6种
固体粉末X中可能含有K2SO3、KAlO2、MgCl2、Na2CO3中的一种或几种。为确定该固体粉末的成分,取X少量溶于水得澄清透明溶液。再取X进行下列实验,实验过程及现象如下:
根据上述实验,以下说法正确的是( )
A.气体1可能为SO2和CO2的混合物
B.沉淀3可能为Mg(OH)2和Al(OH)3的混合物
C.固体粉末X中一定有Na2CO3,可能有KAlO2
D.固体粉末X中一定有K2SO3和KAlO2
取一支大试管,加入20 mL饱和澄清石灰水(ρ=1.6 g·cm-3),再加入5 mL苯(ρ=0.87 g·cm-3),静置后缓慢加入黄豆粒大小的钠块(ρ=0.97 g·cm-3)。能观察到的现象有( )
①钠在饱和澄清石灰水层反应并四处游动
②有气体产生
③澄清石灰水变浑浊
④钠在石灰水与苯的界面处反应并上下跳动
⑤钠停留在苯层不反应 ⑥钠块最后消失
A.①②⑥ B.②③④⑥ C.⑤ D.①②③⑥
下列有关Fe2(SO4)3溶液的叙述正确的是( )
A.该溶液中,K+、Fe2+、C6H5OH、Br-可以大量共存
B.和KI溶液反应的离子方程式:Fe3++2I-===Fe2++I2
C.和Ba(OH)2溶液反应的离子方程式:Fe3++SOeq \\al(2-,4)+Ba2++3OH-===Fe(OH)3↓+BaSO4↓
D.1 L 0.1 ml·L-1该溶液和足量的Zn充分反应,生成11.2 g Fe
某化合物由两种单质直接反应生成,将其加入Ba(HCO3)2溶液中同时有气体和沉淀产生。下列化合物中符合上述条件的是( )
A.AlCl3 B.Na2O C.FeCl2 D.SiO2
某实验小组通过下图所示实验,探究Na2O2与水的反应:
下列说法中正确的是( )
A.②中的大量气泡的主要成分是氢气
B.③中溶液变红,说明有酸性物质生成
C.④中现象可能是由于溶液中含有强氧化性物质造成的
D.⑤中MnO2的主要作用是降低了水中氧气的溶解度
通过对实验现象的观察、分析推理得出正确的结论是化学学习的方法之一。对下列实验事实的解释正确的是( )
某校化学兴趣小组用如图所示过程除去AlCl3溶液中含有的Mg2+、K+杂质离子并尽可能减小AlCl3的损失。
下列说法正确的是( )
A.NaOH溶液可以用氨水来代替
B.溶液a中含有Al3+、K+、Cl-、Na+、OH-
C.溶液b中只含有NaCl
D.向溶液a中滴加盐酸需控制溶液的pH
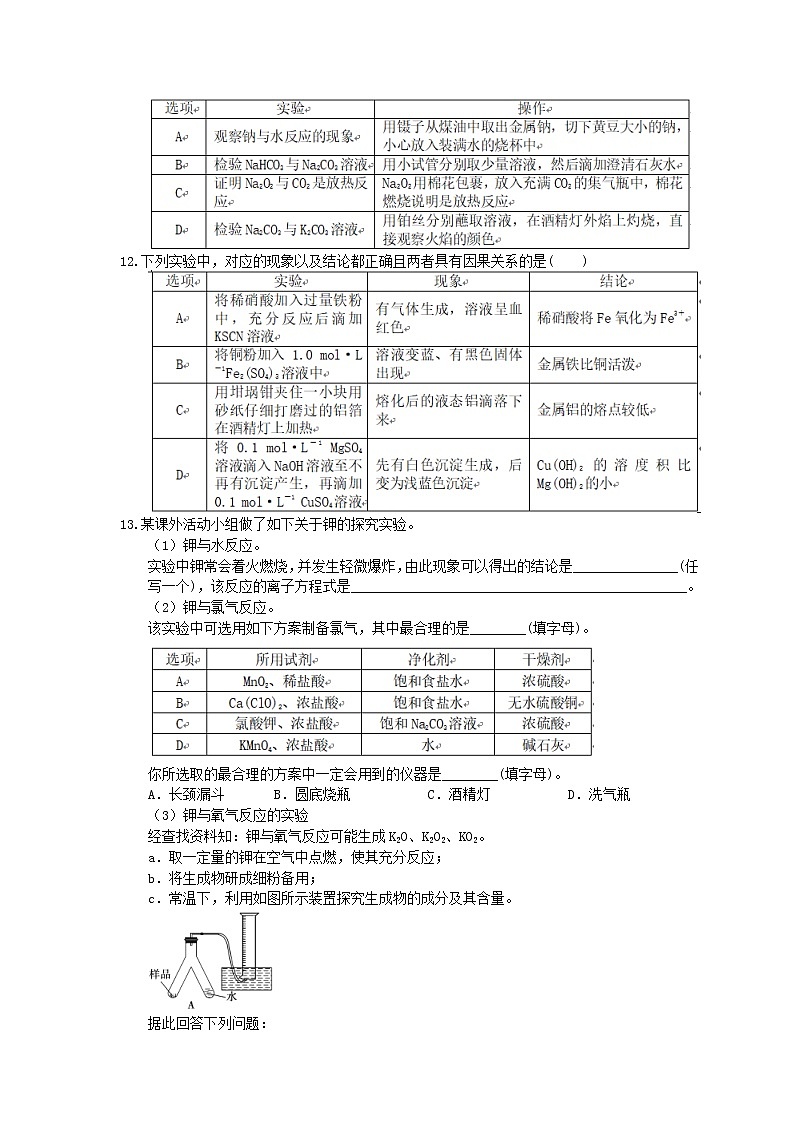
下列实验操作正确的是( )
下列实验中,对应的现象以及结论都正确且两者具有因果关系的是( )
某课外活动小组做了如下关于钾的探究实验。
(1)钾与水反应。
实验中钾常会着火燃烧,并发生轻微爆炸,由此现象可以得出的结论是_______________(任写一个),该反应的离子方程式是________________________________________________。
(2)钾与氯气反应。
该实验中可选用如下方案制备氯气,其中最合理的是________(填字母)。
你所选取的最合理的方案中一定会用到的仪器是________(填字母)。
A.长颈漏斗 B.圆底烧瓶 C.酒精灯 D.洗气瓶
(3)钾与氧气反应的实验
经查找资料知:钾与氧气反应可能生成K2O、K2O2、KO2。
a.取一定量的钾在空气中点燃,使其充分反应;
b.将生成物研成细粉备用;
c.常温下,利用如图所示装置探究生成物的成分及其含量。
据此回答下列问题:
①使细粉末与水反应的操作是______________________________________________。
②测量气体体积时应注意的事项是______________________。
③若钾与氧气燃烧的产物为K2O2、KO2,取燃烧产物3.94 g 进行上述实验,测得气体的体积为868.0 mL,则KO2的质量分数约为________(已知:常温下,气体的摩尔体积为24.8 L·ml-1)。
我国是世界上最早制得和使用金属锌的国家,一种以闪锌矿(ZnS,含有SiO2和少量FeS、CdS、PbS杂质)为原料制备金属锌的流程如图所示:
相关金属离子[c0(Mn+)=0.1 ml·L-1]形成氢氧化物沉淀的pH范围如下:
回答下列问题:
(1)焙烧过程中主要反应的化学方程式为_______________________。
(2)滤渣1的主要成分除SiO2外还有___________;氧化除杂工序中ZnO的作用是____________,若不通入氧气,其后果是________________。
(3)溶液中的Cd2+可用锌粉除去,还原除杂工序中反应的离子方程式为_________________。
(4)电解硫酸锌溶液制备单质锌时,阴极的电极反应式为______________;沉积锌后的电解液可返回_______工序继续使用。
某班化学兴趣小组做如下实验,请你回答相关问题。
Ⅰ.甲组同学想用金属钠和空气制备纯度较高的Na2O2(不考虑空气中N2),可利用的装置如下。回答下列问题:
Ⅰ Ⅱ Ⅲ Ⅳ
(1)装置Ⅳ中盛放的药品是________,若没有该装置可能导致生成的Na2O2中含有________,其反应方程式为____________________________。
(2)若规定气体的气流方向从左到右,各仪器接口的标号字母(a、b……)顺序:空气进入________,________接________,________接________,________接________。
(3)装置Ⅱ的作用是_____________________________________________________。
Ⅱ.乙组利用下图所示实验装置进行某些气体的制备、性质等实验(图中夹持装置已省略)。
A B C D
(4)为验证氯气不能使干燥的红布条褪色,置红布条于B中,按A-C-B-D连接成实验装置体系。A锥形瓶中试剂选用高锰酸钾晶体,则分液漏斗中的液体是________,
A中发生反应的化学方程式是__________________________________________;
C中试剂是____________,
D的作用是______________________________。
工业上利用硫铁矿烧渣(主要成分为Fe2O3、FeO、SiO2)为原料制备高档颜料——铁红(Fe2O3),具体生产流程如下:
试回答下列问题:
(1)硫铁矿烧渣用稀硫酸酸溶时的不溶物为________(填化学式)。
(2)实验室实现“步骤Ⅱ”中分离操作所用的玻璃仪器有____________________;
步骤Ⅳ中应选用________试剂调节溶液的pH(填字母编号)。
A.稀硝酸 B.氢氧化钠溶液 C.高锰酸钾溶液 D.氨水
(3)检验步骤Ⅲ已经进行完全的试剂是_______________________________________。
(4)步骤Ⅴ的反应温度一般需控制在35 ℃以下,其目的是________________________。
(5)步骤Ⅵ中发生反应的化学方程式为_________________________________________。
(6)欲测定硫铁矿烧渣中Fe元素的质量分数,称取a g样品,充分“酸溶”“水溶”后过滤,向滤液中加入足量的H2O2,充分反应后加入NaOH溶液至不再继续产生沉淀,经过滤、洗涤、灼烧至固体恒重,冷却后称得残留固体b g。
①写出加入足量的H2O2发生反应的离子方程式:
________________________________________________________________________;
②测得该样品中Fe元素的质量分数为____________。
\s 0 答案详解
答案为:D;
解析:制铝过程中Al~3e-,制铜过程中Cu~2e-,当转移电子数相等时,铝和铜的物质的量之比为2:3。
答案为:B
解析:向含有CaCO3沉淀的水中通入CO2至沉淀恰好溶解,生成Ca(HCO3)2,再向溶液中加入NaOH饱和溶液,又有CaCO3沉淀生成,A正确;向Na2CO3溶液中逐滴加入稀盐酸首先发生反应:Na2CO3+HCl===NaCl+NaHCO3,所以Na2CO3和HCl的物质的量相等时,不会产生CO2,B错误;NaHCO3和Na2CO3与足量盐酸反应均生成二氧化碳气体,等物质的量的Na2CO3和NaHCO3分别与足量盐酸反应,放出CO2的质量相等,NaHCO3和Na2CO3的质量相等时,NaHCO3的物质的量大,所以同温同压下,生成的CO2体积大,C正确;向Na2CO3饱和溶液中通入CO2,会发生反应:Na2CO3+CO2+H2O===2NaHCO3,常温下,NaHCO3的溶解度比Na2CO3小,且反应消耗水,所以有NaHCO3晶体析出,D正确。
答案为:B;
解析:Al为单质,排除④;(NH4)2CO3与酸反应生成CO2,与碱反应生成NH3;Al2O3、Al(OH)3为两性物质,均能与强酸、强碱反应;NaHSO3与酸反应生成SO2,与碱反应生成Na2SO3;Al2(SO4)3只能与碱反应,不能与酸反应。故既能与酸反应也能与碱反应的化合物是①②⑤⑥,B正确。
答案为:D;
解析:固体X加入足量稀硝酸后的溶液2中加BaCl2溶液有沉淀4生成,则沉淀4为BaSO4,X中一定含K2SO3,它被稀硝酸氧化成K2SO4,同时生成的气体不是SO2,而是NO。X溶于水得澄清透明溶液,因K2SO3与MgCl2在溶液中不能共存,故X中无MgCl2。固体X加足量稀硝酸后的溶液2中加足量氨水能生成沉淀3,结合Al+4H+Al3++2H2O、Al3++3NH3·H2OAl(OH)3↓+3N,可推知X中一定有KAlO2,沉淀3是Al(OH)3。题给实验现象无法确定Na2CO3是否存在。综上分析,可知A、B、C项错误,D项正确。
答案为:B;
解析:金属钠的密度小于水大于苯,将金属钠投入盛有澄清石灰水和苯的大试管中,钠会处于二者的界面处;同时由于钠与水反应生成H2,H2对金属钠产生推动作用,金属钠在界面处可能上下跳动。由于有NaOH生成,并放出热量,Ca(OH)2的溶解度减小,饱和澄清石灰水中有Ca(OH)2析出,溶液变浑浊。
答案为:D;
解析:Fe3+与苯酚发生反应,A错误;
离子方程式中电子得失不守恒,电荷不守恒,B错误;
没有遵循物料守恒原则,C错误;
1 L 0.1 ml·L-1的Fe2(SO4)3溶液中含Fe3+ 0.2 ml,足量的Zn可将0.2 ml Fe3+还原得到0.2 ml的Fe,即质量为11.2 g,D正确。
答案为:A;
解析:AlCl3可由Cl2和Al直接反应生成,在Ba(HCO3)2溶液中加入AlCl3,Al3+和HC发生相互促进的水解反应:Al3++3HCAl(OH)3↓+3CO2↑,同时生成沉淀和气体,A项符合题意;Na2O可由Na和O2直接反应生成,在Ba(HCO3)2溶液中加入Na2O有沉淀生成,但没有气体生成,B项不符合题意;在Ba(HCO3)2溶液中加入FeCl2也有沉淀和气体生成,但FeCl2不能由Fe和Cl2直接化合得到,C项不符合题意;SiO2可由Si和O2直接反应得到,但在Ba(HCO3)2溶液中加入SiO2没有沉淀和气体生成,D项不符合题意。
答案为:C;
解析:②中大量气泡的主要成分是氧气,A项错误;③中溶液变红,说明有碱性物质生成,B项错误;④中红色褪去,应该是由溶液中的强氧化性物质造成的,C项正确;⑤中加入MnO2产生较多气泡,说明溶液中存在H2O2,MnO2的主要作用是作催化剂,D项错误。
答案为:D;
解析:A项中Fe3+将I-氧化为I2,淀粉遇碘变蓝;B项中红棕色斑点是Fe2O3;C项中铁与稀硝酸反应产生的气体为NO。
答案为:D;
解析:A项,若用氨水,则Mg2+、Al3+均转化为沉淀,不能分离Mg(OH)2和Al(OH)3,错误;B项,Al3+与过量NaOH反应生成NaAlO2,溶液a中含AlOeq \\al(-,2)、K+、Cl-、Na+、
OH-,错误;C项,K+、Cl-、Na+在整个过程中不参加反应,溶液b中含KCl、NaCl,错误;D项,因Al(OH)3能溶于盐酸,则向溶液a中滴加盐酸需控制溶液的pH,正确。
答案为:C;
解析:A项,应将钠表面的煤油用滤纸吸干,烧杯中不能装满水,错误;
B项,都有白色沉淀产生,错误;
C项,Na2O2与CO2反应生成氧气,如果棉花燃烧说明达到了着火点,证明是放热反应,正确;
D项,观察钾的焰色反应需透过蓝色钴玻璃,错误。
答案为:D;
解析:稀硝酸中加入过量的铁粉,生成硝酸亚铁,溶液中没有三价铁离子,加入硫氰化钾溶液,溶液不变红,A项错误;铜的活泼性弱于铁,只能发生反应2Fe3++Cu===2Fe2++Cu2+,B项错误;铝和氧气反应生成了氧化铝,又因氧化铝的熔点远高于铝的熔点,而氧化铝在铝的表面,所以加热铝箔的时候铝熔化了但是不会滴落,C项错误;对于组成类似(阴、阳离子个数比相同)的难溶电解质,溶度积大的易转化为溶度积小的,D项正确。
答案为:
(1)钾与水反应放热(其他合理答案也可) 2K+2H2O===2K++2OH-+H2↑
(2)B D
(3)①将仪器A向左倾斜,使水与样品充分接触 ②将气体冷却至室温;移动量筒使量筒内外液面相平,使量筒内的气体压强与大气压强相等;平视读数 ③72.08%
解析:
(2)MnO2与稀盐酸不反应;Cl2能与饱和Na2CO3溶液反应生成CO2、NaCl和NaClO等;碱石灰能吸收Cl2,故方案A、C、D均不合理。
(3)③设样品中K2O2为x ml,KO2为y ml,根据反应2K2O2+2H2O===4KOH+O2↑,
4KO2+2H2O===4KOH+3O2↑,则有110x+71y=3.94①;eq \f(x,2)+eq \f(3y,4)=eq \f(0.868,24.8)②,
联立①②得x=0.01,y=0.04,故KO2的质量分数为eq \f(0.04 ml×71 g·ml-1,3.94 g)×100%≈72.08%。
答案为:
ZnS+1.5O2ZnO+SO2 PbSO4 调节溶液的pH 无法除去杂质Fe2+
Zn+Cd2+Zn2++Cd Zn2++2e-Zn 溶浸
解析:
(1)由于闪锌矿的主要成分是ZnS,因此焙烧过程中主要反应的化学方程式
为2ZnS+3O22ZnO+2SO2。
(2)由于硫酸铅不溶于水,因此滤渣1的主要成分除SiO2外还有PbSO4;要测定铁离子,需要调节溶液的pH,又因为不能引入新杂质,所以需要利用氧化锌调节pH,即氧化除杂工序中ZnO的作用是调节溶液的pH。根据表中数据可知沉淀亚铁离子的pH较大,所以若不通入氧气,其后果是无法除去杂质Fe2+。
(3)溶液中的Cd2+可用锌粉除去,反应的离子方程式为Zn+Cd2+=Zn2++Cd。
(4)电解硫酸锌溶液制备单质锌时,阴极发生得到电子的还原反应,因此阴极是锌离子放电,则阴极的电极反应式为Zn2++2e-=Zn;阳极是氢氧根放电,破坏水的电离平衡,产生氢离子,所以电解后还有硫酸产生,因此沉积锌后的电解液可返回溶浸工序继续使用。
答案为:
(1)NaOH溶液 Na2CO3 2Na2O2+2CO2===2Na2CO3+O2↑
(2)h g f e a b c
(3)防止空气中的水蒸气和二氧化碳进入装置Ⅰ
(4)浓盐酸 2KMnO4+16HCl(浓)===2MnCl2+2KCl+5Cl2↑+8H2O 浓硫酸 吸收氯气以免污染环境
解析:
(1)装置Ⅳ是利用NaOH溶液除去空气中的二氧化碳,若没有该装置,空气的CO2会和Na2O2反应生成碳酸钠。
(2)依据上述分析确定连接顺序,组合实验装置时各仪器的正确连接顺序为Ⅳ、Ⅲ、Ⅰ、Ⅱ,根据气流方向各接口的连接顺序为h、g、f、e、a、b、c。
(3)利用装置Ⅱ中的碱石灰防止空气中的水分和二氧化碳倒吸进入装置Ⅰ。
(4)高锰酸钾和浓盐酸混合可制备氯气,因此分液漏斗中为浓盐酸;氯气能和水反应生成HClO,HClO能使红布条褪色,因此需要用浓硫酸干燥氯气;氯气有毒,不能直接排放到大气中,所以装置D是用于吸收氯气,以免污染环境。
答案为:
(1)SiO2
(2)漏斗、玻璃棒、烧杯 D
(3)KSCN溶液(或其他合理答案)
(4)防止NH4HCO3分解,减少Fe2+的水解
(5)4FeCO3+O2eq \(=====,\s\up7(高温))2Fe2O3+4CO2
(6)①2Fe2++H2O2+2H+===2Fe3++2H2O ②eq \f(7b,10a)×100%
解析:
(1)SiO2为酸性氧化物,不与稀H2SO4反应。
(2)NaOH溶液不易控制溶液pH,应选氨水。
(4)既防止NH4HCO3分解,又减少Fe2+水解。
(5)FeCO3转变为Fe2O3,肯定有氧化剂O2参与反应。
(6)残留b g固体为Fe2O3,根据Fe原子守恒,Fe元素的质量分数为eq \f(b g×\f(112,160),a g)×100%=eq \f(7b,10a)×100%。
高考化学三轮冲刺复习巩固练习二 (含解析): 这是一份高考化学三轮冲刺复习巩固练习二 (含解析),共7页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
高考化学三轮冲刺 单元检测三含答案 金属及其化合物: 这是一份高考化学三轮冲刺 单元检测三含答案 金属及其化合物,共13页。试卷主要包含了本试卷共4页,已知酸性条件下有反应等内容,欢迎下载使用。
2021年高考化学三轮冲刺《有机化学》练习二(含答案): 这是一份2021年高考化学三轮冲刺《有机化学》练习二(含答案),共9页。












