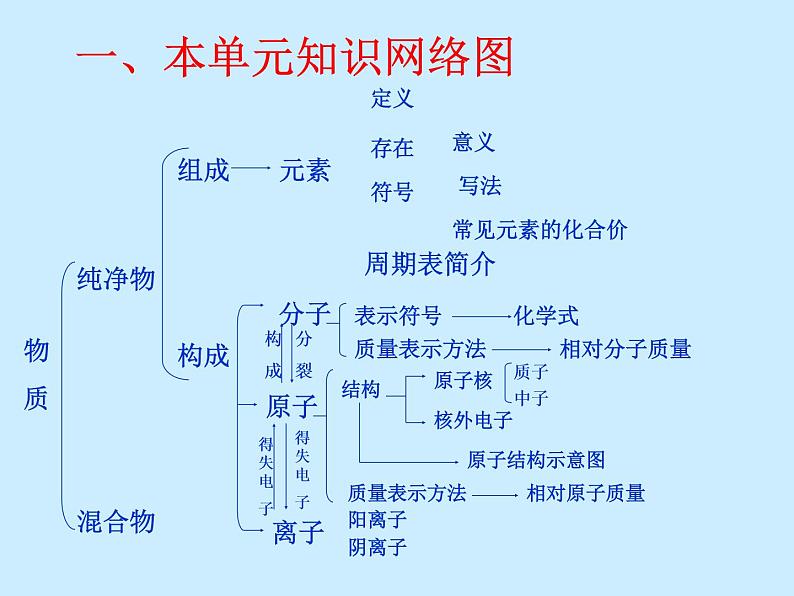





初中化学人教版九年级上册第三单元 物质构成的奥秘综合与测试复习课件ppt
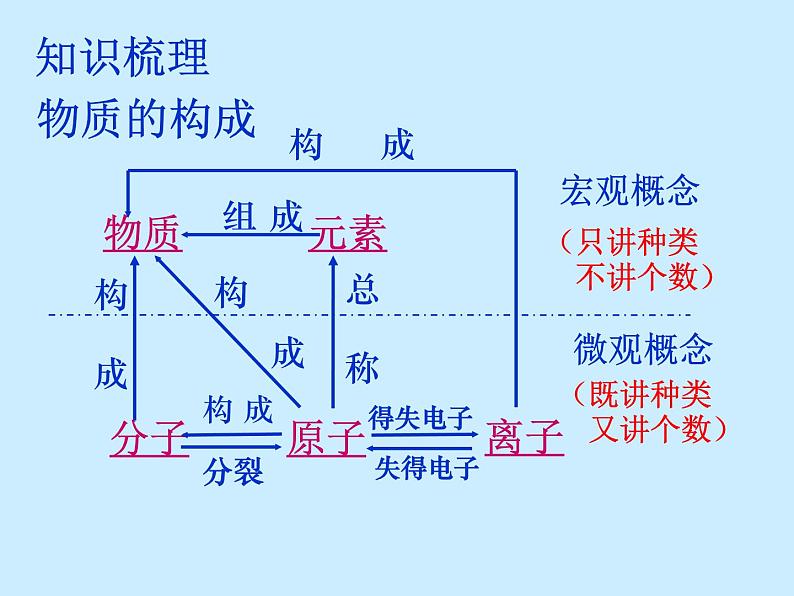
展开(只讲种类 不讲个数)
(既讲种类 又讲个数)
(1)分子体积、质量很小
温度越高,分子能量越大,分子运动速率就越快.
通常状况, 气体分子间隙>液体分子间隙>固体分子间隙
一、构成物质的微粒-分子
2、分子与物质变化的关系物理变化——分子本身不发生改变;化学变化——分子本身发生改变,生成新的分子
3、分子的定义: 分子是保持物质(分子构成)的化学性质的最小粒子
原子是构成物质的另一种微粒。原子构成分子,原子可以直接构成物质
1、原子——是化学变化中的最小微粒。“最小”指在化学反应中不能再分。
(1)原子的体积和质量很小。
(2)原子在不断的运动。
(4)原子在化学变化中不可再分,原子发生重新组合。
分子与原子的主要区别:分子在化学变化中可分,而原子不可分
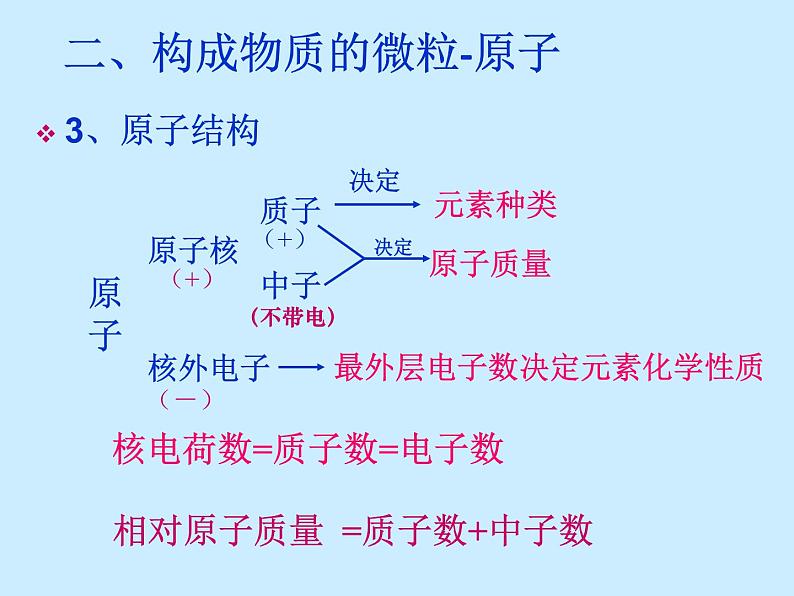
二、构成物质的微粒-原子
1.吸烟有害健康,非吸烟者往往会因吸烟者吸烟而造成被动吸烟,这是因为( )A.分子在不断运动 B.分子之间有间隔C.分子的体积很小 D.分子的质量很小2.将50 mL水与50 mL酒精混合,所得溶液体积小于100 mL,对此现象的解释最科学的是( )A.分子之间有间隔 B.分子是不断运动的C.分子具有一定的质量 D.分子是由原子构成的
3.水与人类的生活和生产密切相关。在水蒸发的过程中,下列说法正确的是( )A.水分子不断运动B.水分子之间间隔不变C.水分子分解成氢原子和氧原子D.水分子可以保持水的物理性质
最外层电子数决定元素化学性质
核电荷数=质子数=电子数
相对原子质量 =质子数+中子数
9.著名化学家徐光宪获得了2008年度国家最高科学技术奖,他的研究成果使稀土元素的分离变得更加简单。其中稀土元素中的钇(Y)元素的原子序数为39,其相对原子质量为90,下列关于钇的说法正确的是( )A.钇元素原子的中子数为39B.钇元素的质子数为51C.钇元素核外电子数为39D.钇元素核电荷数为90
元素的化学性质与原子最外层电子数关系密切
5.元素的化学性质与原子最外层电子的关系
核电荷数=质子数=电子数(分子、原子)核电荷数=质子数≠电子数(离子)相对原子质量≈质子数+中子数
元素种类由_________决定,元素化学性质主要由_____________决定,元素的相对原子质量由_____________决定。
我国在2007年发射一颗绕月探测卫星,其任务之一是寻找一种新能源——氦3。氦3原子核是由一个中子和两个质子构成的,其原子核外电子数为( )A.1 B.2 C.3 D.6
1. 定义:带电的原子或原子团叫做离子。2. 离子形成的过程阳离子:带正电荷的离子阴离子:带负电荷的离子
4. 离子的表示方法:
3. 离子符号:阳离子:Mg2+ 阴离子:Cl -
6. 离子符号里的数字的意义:
表示每个镁离子带2个单位的正电荷
5. 离子符号的意义:
原子中:质子数=电子数(原子不带电)
阳离子中:质子数>电子数(带正电) 阴离子中:质子数<电子数(带负电)
(2)原子和离子的区别和联系
构成物质的微粒有:分子、原子和离子。由原子构成的物质:铁、氦气等由分子构成的物质:水、二氧化碳等4 由离子构成的物质:氯化钠等
1.科学研究证明,物质是由微粒构成的。请用原子、分子或离子填空: (1)应用最广泛的铁是由铁 构成的;(2)保持氮气化学性质的是氮 ;(3)调味用的氯化钠是由钠 和氯 构成的。
2.某微粒结构示意图为 , 下列说法中错误的是( )A.该微粒为稳定结构B.该微粒原子核内有13个质子C.该微粒属于原子 D.该微粒带3个单位正电荷
小结:一般最外层电子要达到8个电子才稳定(只有一个或两个电子层,并且最外层电子数少于4的,失去最外层也达到稳定,氦只有一个电子层,最外层是2也是稳定的)
1、定义:质子数(即核电荷数)相同的一类原子的总称。
注意事项:(1)“一类原子”指的化学变化中不能再分的粒子。
(2)原子的质子数(即核电荷数)决定元素种类。
元素——是一类原子的总称,只能讲种类,不 能讲个数。
原子——是一种粒子,有种类、个数
2、地壳中含量较多的几种元素
氧硅铝铁钙钠钾,还有镁氢和其他
3.元素符号书写的要求:(1)由一个字母表示的元素符号要大写;(2)由两个字母表示的元素符号,第一个字母大写 ,第二个字母小写
2 3 4 5 6 7 8 9 10 H He Li Be B C N O F Ne 氢 氦 锂 铍 硼 碳 氮 氧 氟 氖11 12 13 14 15 16 17 18 19 20Na Mg Al Si P S Cl Ar K Ca钠 镁 铝 硅 磷 硫 氯 氩 钾 钙
(1至20号元素)的原子序数(质子数):
4、元素符号表示的意义
微观:表示该元素的一个原子
注意事项:(1)在元素符号前的系数,只表示原子的个数,失去宏观意义,不再表示元素。
5、元素与原子的区别和联系
元素用于描述物质的宏观组成;只讲种类,不讲个数原子用于描述物质的微观构成;既讲种类,又讲个数
(1)、元素概念建立在原子基础上;(2)、原子的核电荷数(即核内质子数)决定了元素的种类,原子的最外层电子数决定了元素的化学性质
则该元素的质子数为 ,该原子核外有 个电子层,该元素属于 。 (填“金属”或“非金属”)元素。
1.某元素是人体中的常量元素,它在人体内99%存在于骨骼和牙齿中。该元素的原子结构示意图为:
元素的化学性质决定于最外层,最外层<4个电子是金属元素,在化学变化中易失去电子最外层≥4个电子是非金属元素,在化学变化中得到去电子,
2.下面是五种粒子的结构示意图
(1)图中粒子共能表示 种元素。A所表示的元素位于元素周期表的第 周期。(2)图中表示的阳离子是 (用离子符号表示),表示的阴离子是
1.周期:每一个横行称为一个周期。2.族:每一个纵行称为一个族。3.原子序数=核电荷数=核内质子数=核外电子数
26铁 Fe55.847
4.元素周期表所能提供的信息
下表是元素周期表的一部分:
1. 原子序数为94的钚(Pu)是一种核原料,该元素一种原子的质子数和中子数之和为239,下列关于该原子的说法不正确的是( )A.中子数为145 B.核外电子数为94C.质子数为94 D.核电荷数为239
[解析] D 在原子中,核电荷数=核内质子数=核外电子数=原子序数;相对原子质量=质子数+中子数,故钚原子核内中子数为:239-94=145。
2.下列说法正确的是( ) A.分子质量比原子的大 B.分子之间有间隔而原子之间没有间隔 C.离子不能构成物质 D.在化学变化中分子可以再分而原子不能再分3.下列粒子不能构成物质的是( ) A.分子 B.电子 C.原子 D.离子
[解析] A、B、C、D分别表示的是氩原子、镁原子、氯原子和钠离子。
化学九年级上册课题3 元素教学ppt课件: 这是一份化学九年级上册课题3 元素教学ppt课件,共38页。PPT课件主要包含了特别提醒等内容,欢迎下载使用。
山东诗营市初中化学学业水平考试总复习第三单元物质构成的奥秘课件: 这是一份山东诗营市初中化学学业水平考试总复习第三单元物质构成的奥秘课件,共60页。PPT课件主要包含了三或3,MgF2,硅原子,非金属,H2O,H2O2,Na2O,熔点低,Ga2O3,门捷列夫等内容,欢迎下载使用。
2022届初中化学一轮复习 第三单元 物质构成的奥秘 课件: 这是一份2022届初中化学一轮复习 第三单元 物质构成的奥秘 课件













