






高中化学人教版 (新课标)必修1第四章 非金属及其化合物第四节 氨 硝酸 硫酸示范课ppt课件
展开1、硫酸、硝酸、盐酸都是酸,它们在组成上用什么特点?
它们都是酸,在水溶液中电离出H+,硫酸、硝酸是含氧酸,盐酸是无氧酸;硫酸是二元酸,硝酸和盐酸是一元酸
2、这些特点与酸的通性有什么关系?用电离方程式表示。
在水溶液中都电离出氢离子
3、实验室里用金属与酸反应制取氢气时,往往用稀硫酸或盐酸,而不用浓硫酸或硝酸,这是为什么?
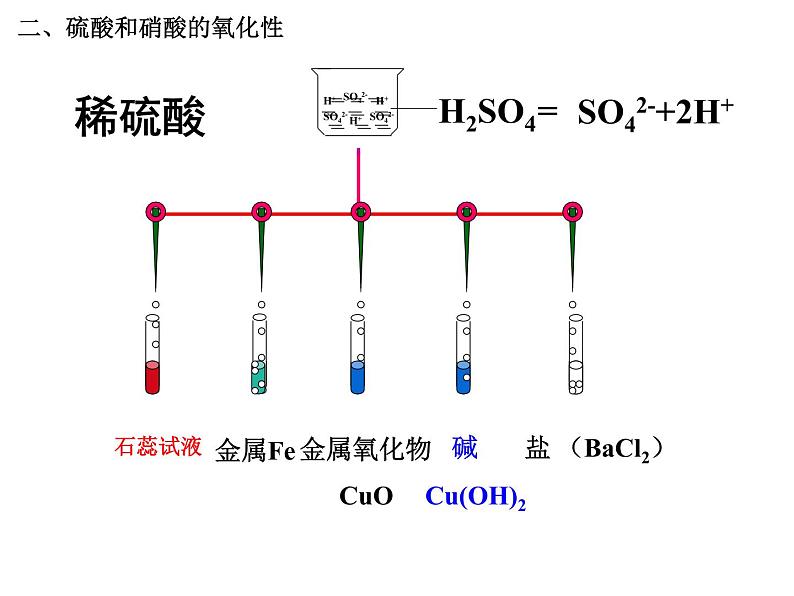
二、硫酸和硝酸的氧化性
(一)稀硫酸具有酸的通性 H2SO4=2H++SO42-
一、硫酸(H2SO4)
①与指示剂反应; ②与活泼金属反应; ③与金属氧化物反应生成盐和水; ④与盐的反应生成新盐和新酸; ⑤与碱的反应,生成盐和水。
①、纯硫酸是无色、油状、液体(常用浓硫酸质量分数为98.3%)。
②、纯硫酸难挥发,沸点338℃。 (高沸点酸)
③、密度:质量分数为98.3%的硫酸的密度为1.84g/cm3
④、易溶于水,能以任意比与水混溶
(浓硫酸溶解时放出大量的热)
浓硫酸的特点“两高”、“两大”:高沸点,密度高,溶解度大,溶解放热量大。
思考:如何稀释浓硫酸?
将浓硫酸沿着容器内壁(或沿着玻璃棒)缓慢地注入水中,并用玻璃棒不断搅拌,使产生的热量迅速扩散。
将浓硫酸与其它低密度的液体混合时,方法与硫酸在水中的溶解方法相同。
【讨论】:现有浓硫酸、浓盐酸各一瓶(无标签,试剂瓶大小一样,酸的体积相同),不用化学方法怎样识别?根据是什么?
气味、状态(油状)、重量、白雾
浓硫酸吸收物质本来就有的水),直接与水分子结合;
可用来干燥与它不起反应的气体,如 H2、O2、Cl2、CO2、CO、CH4、SO2、N2、NO2、NO、HCl。
不能干燥NH3、H2S、HBr、HI
脱水性是指浓硫酸能把有机物中的氢氧原子按2:1(H2O)的个数比脱去。
【实验】取10g蔗糖放入小烧杯中,加入几滴水,用玻璃棒搅拌均匀,再加入10mL浓硫酸,并用玻璃棒迅速搅拌。观察物质的颜色、体积变化并闻味。
现象:蔗糖变黑,体积膨胀,形成疏松多孔的海绵状的炭,并有刺激性气味的气体产生。
浸有碱液的棉团的作用,吸收多余的SO2,防止大气污染
有使品红褪色的气体产生
铜分别和浓、稀硫酸反应比较
①与不活泼金属反应 Cu + 2H2SO4(浓) = CuSO4+ SO2↑+ 2H2O
0 +6 +2 +4
还原剂 氧化剂 氧化产物 还原产物
若铜过量,硫酸能否完全反应?为什么?
在常温下,浓硫酸跟某些金属,如铁、铝等接触时,能够使金属表面生成一薄层致密的氧化物薄膜,从而阻止内部的金属继续跟硫酸发生反应(钝化现象)。因此,冷的浓硫酸可以用铁或铝的容器贮存。但受热时,浓硫酸可以与Fe、Al反应。
气态的CO2、SO2从炭的空隙中冲出,导致了炭内形成无数个分布不均的孔洞,使炭呈多孔蓬松状。
如何用实验方法证明木炭与浓硫酸反应的产物?
提供以下试剂与装置(装置可多次使用):
说明:应首先用无水硫酸铜验证水,然后用品红验证二氧化硫,再用高锰酸钾氧化多余的二氧化硫,接着再次验证二氧化硫是否全部被氧化,最后才验证二氧化碳。
③与活泼金属 常温下,与铁和铝等接触发生钝化 受热时,能跟绝大多数金属发生反应
【思考】浓硫酸具有强氧化性,稀硫酸是否有氧化性?如果有,其氧化性与浓硫酸的氧化性有何不同?浓硫酸与稀硫酸比较:稀H2SO4:由H+和SO42-构成——弱氧化性(由H+体现)——可与活泼金属反应生成H2 浓H2SO4:由H2SO4分子构成——强氧化性(由 S 体现)—
加热时可与大多数金属和某些非金属反应,通常生成SO2
练习:下列现象反映了硫酸的哪些主要性质 (1)浓硫酸滴在木条上,过一会儿,木条变黑。 (2)敞口放置浓硫酸时,质量增加。 (3)锌粒投入稀硫酸中,有气泡产生。 (4)把铜片放入浓硫酸里加热,有气体产生。 (5)利用浓硫酸和食盐固体反应可制HCl气体。 (6)浓硫酸不能用来干燥硫化氢气体。 (7)利用硫化亚铁跟稀硫酸反应可制H2S气体。
答案: (1)脱水性 (2) 吸水性 (3) 酸性 (4)酸性和强氧化性 (5)难挥发性 (6)强氧化性 (7)强酸性
①高沸点——制取挥发性酸。②吸水性——做干燥剂。③脱水性——做催化剂。④酸性——去金属表面的氧化物、 制取硫酸盐、制造化肥。⑤强氧化性——制炸药。
硫酸的消费量被视为一个国家工业发水平的标志
硫酸是世界上用量最大、用途最广的化工基本原料之一,故素有“化学工业之母”之称。
化学必修1第四节 氨 硝酸 硫酸教学课件ppt: 这是一份化学必修1第四节 氨 硝酸 硫酸教学课件ppt,共1页。
高中化学人教版 (新课标)必修1第四章 非金属及其化合物第四节 氨 硝酸 硫酸多媒体教学ppt课件: 这是一份高中化学人教版 (新课标)必修1第四章 非金属及其化合物第四节 氨 硝酸 硫酸多媒体教学ppt课件,共53页。PPT课件主要包含了思考·交流,HCl,NH3,现象产生大量白烟,实验探究,实验·探究,如何检验SO42-,浓硫酸的特性,⑵脱水性,3氧化性等内容,欢迎下载使用。
人教版 (新课标)必修1第四节 氨 硝酸 硫酸图文ppt课件: 这是一份人教版 (新课标)必修1第四节 氨 硝酸 硫酸图文ppt课件,共47页。PPT课件主要包含了氨的化学性质,2氨与酸的反应,现象产生大量白烟,思考与交流,氨的用途,制铵盐,制硝酸,制尿素,制冷剂,试剂及操作等内容,欢迎下载使用。













