
初中化学沪教版九年级下册第2节 溶液组成的表示优秀学案
展开【学习目标】1、掌握用溶质的质量分数表示溶液组成的方法和有关计算。
2、学会配制一定质量的溶质质量分数的溶液。
3、通过实验探究,增强学生对化学好奇心和探究欲,激发学生的学习兴趣。
【学习重点、难点】
1、溶质的质量分数的计算中涉及溶液体积时的计算及配制的步骤
2、配制中误差的分析
【学习过程】
一、回顾、预习与交流
【旧知回顾】
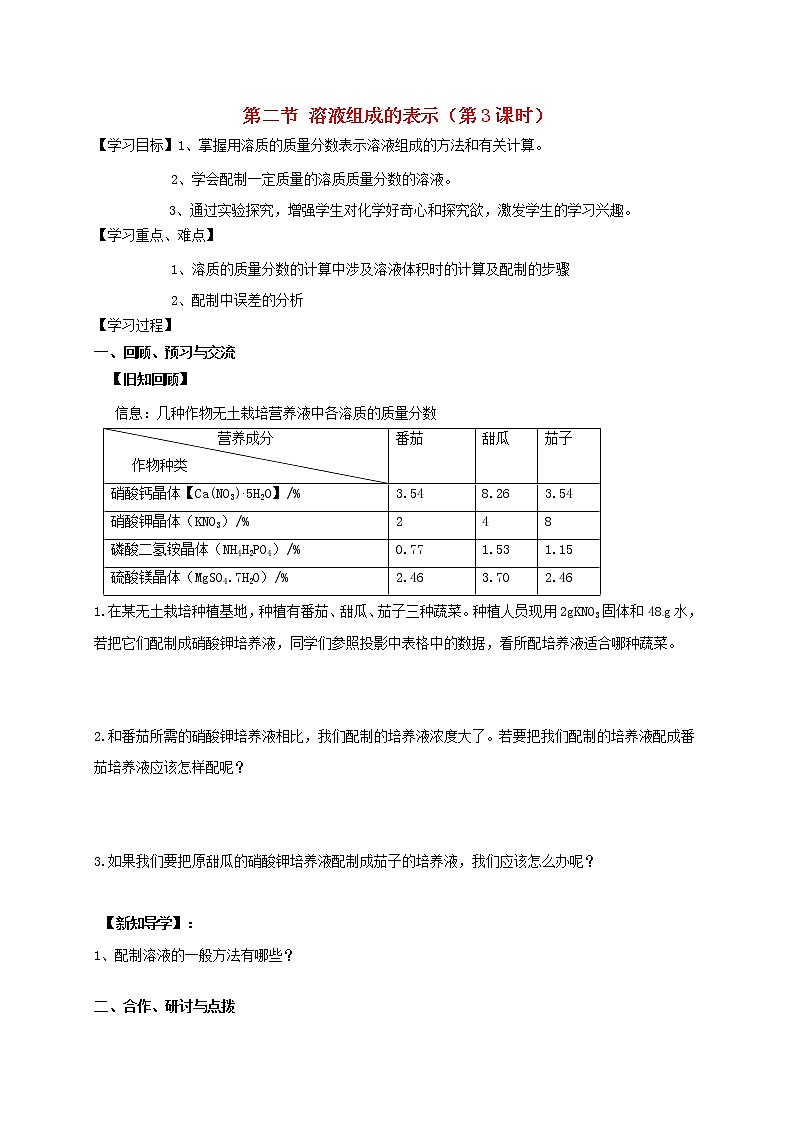
信息:几种作物无土栽培营养液中各溶质的质量分数
1.在某无土栽培种植基地,种植有番茄、甜瓜、茄子三种蔬菜。种植人员现用2gKNO3固体和48g水,若把它们配制成硝酸钾培养液,同学们参照投影中表格中的数据,看所配培养液适合哪种蔬菜。
2.和番茄所需的硝酸钾培养液相比,我们配制的培养液浓度大了。若要把我们配制的培养液配成番茄培养液应该怎样配呢?
3.如果我们要把原甜瓜的硝酸钾培养液配制成茄子的培养液,我们应该怎么办呢?
【新知导学】:
1、配制溶液的一般方法有哪些?
二、合作、研讨与点拨
活动一 配制一定质量的溶质质量分数的溶液
农业生产上,有时用质量分数为10%~20%食盐溶液来选种。现用食盐固体和水来配制50克15%食盐溶液,应该如何配制这样的溶液呢?
活动二:用15%食盐溶液配制55ml生理盐水(生理盐水的溶质质量分数为0.9%,密度为1.0g/ml,15%食盐溶液密度为1.1g/ml.)
三、总结、反思、提升
1 .总结:实验室配制溶液的一般步骤
固体物质配制: _______、_________、_________、_________、_________
浓溶液稀释配制:_______、________、_________、_________、__________
用足量的粗盐配制一定质量、一定质量分数的氯化钠溶液其步骤为:
。
2.请找出下图中的错误:① ;② ; ③ 。
3.提升:在NaCl固体配NaCl溶液时,下列操作会导致所配溶液的溶质质量分数(偏大、偏小、不变)
①未使用游码,物码倒置 ;②在使用游码情况下,物码倒置 ;
③使用了生锈的砝码(铁锈未脱落) ;④转移固体时,固体撒落 ;
⑤量筒内水倒入烧杯时洒落 ;有水未倒尽 ;
⑥用量筒量取水,俯视读数 ;仰视读数 ;
⑦所用量筒内有水 ; ⑧配好的溶液装瓶时洒落 ;
四、自检、反馈与巩固
【课堂作业】1.向l00g10%NaOH溶液中加入12.5gNaOH固体,完全溶解后.所得溶液中溶质质量分数为 ( )
A. 12. 5% B.20.0% C.22.5% D.25%
2.用氯化钠固体和蒸馏水配制100g10%的氯化钠溶液,不需要的实验仪器是 ( )
A.玻璃棒 B.蒸发皿 C.烧杯 D.天平
3.把400克质量分数为20%食盐水稀释成质量分数为10%的溶液,需加水 ( )
A 100克 B 200克 C 400克 D 800克
4. 配制溶质质量分数一定的氯化钠溶液常按以下操作顺序进行。
请回答下列问题:(1)计算配制100g溶质质量分数为5%的氯化钠溶液所需: 氯化钠 g,水 g,即用 的量筒量取 ml的水。
(2)用托盘天平称量所需的氯化钠时,发现托盘天平的指针偏向左盘,应 。
A.增加适量氯化钠固体 B.减少适量氯化钠固体 C.调节平衡螺母
(3)将氯化钠和水依次倒入烧杯中,用玻璃棒搅拌,其目的是 。
【课后作业】
1.实验室用密度为1.84g/cm3、质量分数为98%的浓硫酸和蒸馏水,配制500g 质量分数为20%的稀硫酸。需要用多少mL的量筒量取多少mL的浓硫酸? ( )
A.100mL、54.35mL B.100mL、55.5mL C.250mL、54.35mL D.250mL、55.5mL
2.把30克质量分数为20%的氢氧化钠溶液,加水稀释到100克,取出稀释后溶液20克,此溶液中NaOH的质量分数为 ( )
A .5% B .6% C. 3% D .2%
3.在实验室配制溶液时,常涉及以下过程:①溶解②称量③计算④装瓶存放。请按要求回答问题:
(1)现欲配制50g 5%氯化钠溶液,配制过程的先后顺序是 (填序号)。
(2)用已调节平衡的天平称取氯化钠固体时,发现指针偏右,接下来的操作是
(3)在量取蒸馏水体积时,若仰视读数,则会导致氯化钠溶液的溶质质量分数 (填“<”或“>”)5%。
(4)在称量步骤中需要的仪器有 。
4.“84消毒液”广泛应用于物体表面的消毒,其有效成分是次氯酸钠。
(1)50g溶质质量分数为12%的次氯酸钠溶液中,需要固体次氯酸钠 g,
水 mL
(2)将上述溶液稀释成0.2%的次氯酸钠溶液 g,加水 mL
5.农业上经常用16%的食盐溶液来选种,如果溶液太浓或太稀都会使优种筛出。小明准备配制500g这种食盐溶液帮家里选种,他应该称量________g食盐,在用量筒量取所需水的过程中,小明俯视读数,这样配得的溶液浓度会_____(填“偏高”、“偏低”、或“无影响”)。
为检验糖尿病患者的尿液,医院要配置8%的CuSO4溶液。现有16g CuSO4固体,可配置该CuSO4溶液_______g,需水________ml(水的密度为1.0g/ml)。配置CuSO4溶液的一般步骤为_____、_____、______。在此过程中需要用到的仪器有_________________________。
6.2010年4月14日,青海省玉树县发生大地震,某护士为在帐篷里的一位病人滴注500mL的生理盐水(NaCl的质量分数为0.9%,溶液的密度约为1g/mL)。计算500mL的生理盐水中NaCl的质量为 g,水的质量为 g,水的体积是 ml。
(选做)7. 某化学兴趣小组的同学做粗盐(含有难溶性杂质)提纯实验,并用所得的精盐配制50 g 5%的氯化钠溶液。
图10
② ③ ④ ⑤ ⑥
实验一:图10是同学们做粗盐提纯实验的操作示意图。
粗盐
粗盐
请回答下列问题:
(1)操作④中用玻璃棒搅拌的作用是 。
(2)操作⑥中的错误是 。
(3)粗盐提纯实验的操作顺序为(填操作序号) 、称量精盐并计算产率。
(4)操作④中,当观察到 时,停止加热。
实验二:用提纯得到的精盐配制了50 g 5%的氯化钠溶液。经检测,溶质质量分数偏小,其原因可能有 (填序号)。
①氯化钠固体仍然不纯 ②称量时砝码端忘垫质量相同的纸片
③量取水时,仰视读数④装瓶时,有少量溶液洒出
⑤溶解氯化钠的烧杯内壁是潮湿的 ⑥用2.5g氯化钠和50g水配制溶液营养成分
作物种类
番茄
甜瓜
茄子
硝酸钙晶体【Ca(NO3).5H2O】/%
3.54
8.26
3.54
硝酸钾晶体(KNO3)/%
2
4
8
磷酸二氢铵晶体(NH4H2PO4)/%
0.77
1.53
1.15
硫酸镁晶体(MgSO4.7H2O)/%
2.46
3.70
2.46
配制溶液基本步骤
所用仪器
1
2
3
4
5
配制溶液基本步骤
所用仪器
1
2
3
4
5
沪教版九年级下册第2节 溶液组成的表示优质导学案及答案: 这是一份沪教版九年级下册第2节 溶液组成的表示优质导学案及答案,共2页。学案主要包含了拓展提高等内容,欢迎下载使用。
沪教版九年级下册第6章 溶解现象第2节 溶液组成的表示优秀导学案: 这是一份沪教版九年级下册第6章 溶解现象第2节 溶液组成的表示优秀导学案,共3页。学案主要包含了课前预习,教学过程等内容,欢迎下载使用。
化学九年级下册第2节 溶液组成的表示优秀导学案: 这是一份化学九年级下册第2节 溶液组成的表示优秀导学案,共2页。













