


人教版九年级上册课题2 原子的结构优质ppt课件
展开1.(2020•云南模拟)“不经一番寒彻骨,怎得梅花扑鼻香”,从微观角度分析,诗人能闻到梅花香气的主要原因是( )A.分子的体积和质量都很小B.分子间有一定的间隔C.分子在不断地运动 D.分子可以再分
2.(2020•蒙自市一模)家庭用液化石油气是丙烷、丁烷等气体经加压后压缩到钢瓶中的,气体能被压缩的原因是( )A.分子质量和体积很小B.分子体积变小C.分子在不断运动 D.分子间有间隔
3.(2020春•平房区期末)下列事实用微粒的知识解释错误的是( )
4.(2020•莒县模拟)下列变化能证明分子可以再分的是( )A.水蒸发 B.电解水C.干冰升华D.硬水软化
5.(2019秋•西岗区期末)用微粒的观点回答下列问题:(1)干冰汽化体积变大,因为 。(2)杯中的水敞口不断减少,因为 。(3)一氧化碳和二氧化碳化学性质不同的原因是 。(4)金刚石和石墨的物理性质差异很大的原因是 。
二氧化碳分子间的间隔变大
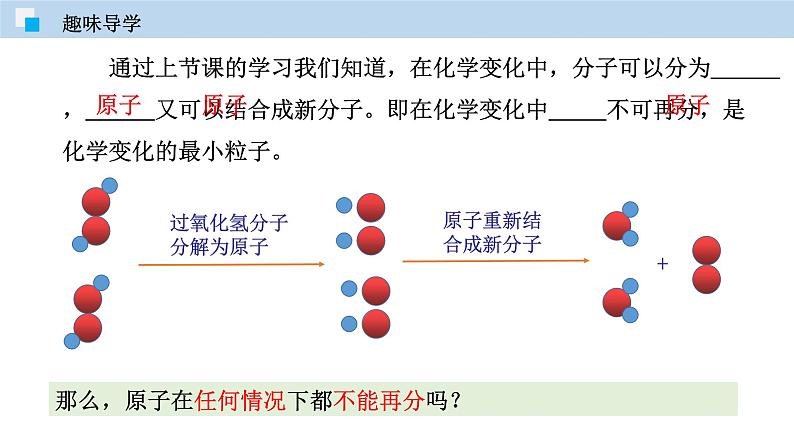
通过上节课的学习我们知道,在化学变化中,分子可以分为 , 又可以结合成新分子。即在化学变化中 不可再分,是化学变化的最小粒子。
过氧化氢分子分解为原子
那么,原子在任何情况下都不能再分吗?
1897年,汤姆森在原子内部发现了带负电的电子,摧毁了“原子不可再分”的观点,并建立了新的原子结构模型--“葡萄干布丁模型”。
远在公元前5世纪,希腊哲学家德谟克利特(约公元前460~前370)等,认为万物都是由大量不可再分的微粒构成的,并把这种微粒叫做原子。
到了19世纪前半叶,英国科学家道尔顿提出:构成物质的最小粒子是原子,原子是不可再分的实心球体。
“葡萄干布丁模型”认为,原子是一个平均分布着正电荷的圆球状粒子,而带负电荷的电子像一粒粒葡萄干一样镶嵌其中,中和了正电荷,从而形成了中性原子。
1911年,卢瑟福通过精密的实验证明在原子中心有一个带正电的极小的核,电子在一个很大的空间绕核做高速旋转。
即原子是由居于原子中心的原子核与核外电子构成。
1个质子带1个单位的正电荷
(1个电子带1个单位负电荷)
【练一练】下列关于原子的叙述中,正确的是( ) A.原子由电子和质子构成的 B.原子由电子和中子构成的 C.原子由质子和中子构成的 D.原子由原子核和核外电子构成的
【练一练】(2020•惠来县模拟)如图是某同学学习物质结构层次后以氧气为例进行的梳理,下列选项中与a、b、c相对应的是( )
A.原子、原子核、核外电子B.原子核、原子、核外电子C.原子、核外电子、原子核 D.核外电子、原子核、原子
通过下表,你能得出哪些结论?
结论1:在同一个原子中,核电荷数_____质子数。
结论2:在同一个原子中,质子数_____核外电子数。
结论3:在同一个原子中,质子数_____________中子数。
结论5:原子中不一定含有中子,如 。
结论4:不同的原子的质子数和核外电子数均 。
根据刚才的判断我们可以得到:1.在同一个原子中,核电荷数=__________=__________;2.在同一个原子中,质子数_____________中子数;
同一原子中,原子核中带正电的_____和核外带负电的________,所带的电量 且电性________,故整个原子不显电性。
4.原子中不一定含有中子,如氢原子;
3.不同种类的原子,其根本区别在于它们核内 的不同。
【练一练】下列叙述中错误的是( )。 ①原子是化学变化中的最小粒子 ②原子是不能再分的粒子 ③一切物质都是由原子直接构成的 ④一切原子核都是由质子和中子构成的 ⑤原子不显电性 ⑥原子之间有间隔A.①② B.②③④ C.③⑤ D.③⑥
【练一练】(2019秋•从化区期末)钛被称为“航空金属”,国产C919大飞机的钛合金用量达到9.3%.已知一种钛原子核内有22个质子和26个中子,该原子的核外电子数为( )A.22B.26 C.48D.4
原子的体积非常小,小到什么程度呢?
如果将一个原子与一个乒乓球相比,相当于将这个乒乓球与地球相比。
二、核外电子的分层排布
原子很小,原子核更小。
如果把原子看做一个体育场,那么它的原子核也就是一只蚂蚁这么大。因此,原子核外有一个很大
的空间,电子在这个空间里做高速运动。
电子在核外是怎样运动的呢?
(1)电子在核外是分层排布的。
电子从离核最近的一层开始排,这层为第一层,次之为第二层,依次类推为三、四、五、六、七层,离核最远的也叫最外层。
(2)各电子层上最多排2n2个电子; 其中第一层最多排2个电子,最外层最多排8个电子。
如何更简明、方便地表示电子的分层排布呢?
我们用原子结构示意图来表示。
【练一练】画出1-20号元素原子结构示意图,并观察它们的原子结构特点。
金属原子:最外层电子数一般少于4个
非金属原子:最外层电子数一般等于或多于4个
稀有气体原子:最外层电子数等于8个(氦原子除外,最外层电子数为2)
最外层电子为8(只有一个电子层时有2个电子)时的结构,不易与其它物质发生反应,属于相对稳定的结构,元素化学性质相对稳定。
想一想,下列这些结构是不是稳定结构?
·多数金属原子的最外层电子数少于4,容易 电子;·许多非金属原子的最外层电子数多于4,容易 电子;·氦、氛、氩等稀有气体的原子的最外层电子数为8(氦原子的最外层电子数为2),既不易失去电子,也不易得到电子。
最外层的电子数不为8的原子,在化学反应中容易得到或者失去电子,趋于变成稳定结构:
多数金属原子容易失去电子,那么失去电子之后变成了什么?
我们以氯化钠的形成为例:
在上述过程中,钠原子因失去l个电子而带上1个单位的正电荷;氯原子因得到1个电子而带上1个单位的负电荷。 像这种 叫做离子。其中 叫做阳离子,如钠离子(Na+); 叫做阴离子,如氯离子(CI-)。
原子不带电而离子带电,即离子的质子数≠电子数
【练一练】下列结构中属于原子结构的是 ,属于阳离子的是 ;属于阴离子的是 。
【练一练】右图为氯原子的结构示意图,下列有关说法错误的是( )A.氯原子的核电荷数为17B.氯原子最外层有7个电子C.氯原子的质子数为17D.在化学反应中氯原子容易失去电子
【练一练】(2020•青白江区模拟)某粒子的结构示意图是 ,当n=9时,该微粒是( )A.阳离子 B.分子C.阴离子 D.原子
离子和分子、原子一样,也是构成物质的一种粒子,如NaCl就是由Na+和CI-构成。
【练一练】下列各组物质中,都由离子构成的一组是( ) A.NaCl、MgCl2 B.H2O、HCl C.Si、CO2 D.Ar、Na
【练一练】下列物质由分子构成的是( )A.氦气 B.水 C.氯化钠 D.金刚石
【练一练】(2020•芝罘区一模)建立正确的微粒观有助于化学的学习,下列有关微粒的说法错误的是( )A.原子可以转化为离子B.原子的质量主要由质子和中子决定C.离子之间存在着相互作用,分子之间不存在相互作用D.原子得失电子后,原子核没有发生变化
【练一练】(2020•任城区三模)下列关于分子、原子、离子的说法正确的是( )A.NaCl由Cl﹣和Na+构成 B.原子中都含有中子C.Cl﹣的质子数比电子数多1 D.保持水化学性质的最小粒子是氢原子和氧原子
原子核虽然很小,但整个原子的质量几乎都集中在核上。每个质子和每个中子的质量几乎相等,都大约等于l个氢原子的质量,而电子的质量仅仅约等于质子质量的1/1836。那么,原子的质量又有多大呢?
一个氢原子的质量是:0.00000000000000000000000000167千克 即1.67×10-27千克一个碳原子的质量是:0.00000000000000000000000001993千克 即1.993×10-26千克一个氧原子的质量是:0.00000000000000000000000002657千克 即2.657×10-26千克
从上图中你能得出哪些信息?
如何让记忆、计算更方便呢?
为更方便地书写和使用原子的质量,国际上采用相对质量,即以一种碳原子质量的1/12为标准,其它原子的质量与它相比较得到的比值,作为这种原子的相对原子质量(符号为Ar)。
原子的质量很小,通常使用其相对质量
以碳-12原子的质量的1/12为标准,其它原子的质量跟它的比值。
例:氢原子的相对原子质量=
1.67×10-27kg
1.661×10-27kg
碳原子的相对原子质量=
1.992×10-26kg
氧原子的相对原子质量=
2.657×10-26kg
(1)相对原子质量不是原子的真实质量;
(2)相对原子质量是个比值,单位为1,一般不写;
(3)相对原子质量与原子的真实质量成正比。
结论:相对原子质量≈ + 。
【练一练】(2019秋•保山期末)下列有关原子结构的说法正确的是( )A.原子中的中子带负电荷 B.决定原子种类的是质子数C.原子中质子与中子的数目一定相同 D.原子的质量主要集中在质子和电子上
【练一练】(2019秋•龙口市校级月考)有两个原子,甲原子核内有6个质子和8个中子,乙原子核内有7个质子和7个中子,关于这两个原子的说法,不正确的是( )A.不属于同类原子B.核电荷数不相同C.相对原子质量相同D.核外电子数相同
(每个质子带1个单位正电荷)
(每个电子带1个单位负电荷)
核电荷数=质子数=核外电子数
质子数(核电荷数)
电子从离核最近的一层开始排。
(2)各电子层上最多排2n2个电子, 其中第一层最多排2个电子,最外层最多排8个电子。
3.相对原子质量=质子数+中子数
1.定义:以碳-12原子的质量的1/12为标准,其它原子的质量跟它的比值。
(1)定义:带电的原子。
阳离子(带正电荷)如:Na+
阴离子(带负电荷)如:Cl-
(3)判断:质子数≠电子数
(4)离子是构成物质的一种粒子。
1.(2019秋•龙口市校级月考)下列粒子中,带负电荷的是( )A.原子B.质子C.中子D.电子
2.(2020•江西模拟)铯原子钟是一种精密的计时器具,它的稳定程度很高,目前最好的铯原子钟达到2000万年才相差1秒。已知某种铯原子的相对原子质量为134,核外电子数为55,则该原子的中子数为( )A.34B.55 C.79D.134
3.(2019秋•南昌期末)关于Mg和Mg2+的叙述正确的是( )A.核电荷数相同 B.最外层电子数相同C.核外电子数相同D.电子层数相同
4.(2019•大丰区校级模拟)氦(He)核聚变会释放出巨大能量,给人类能源危机提供了途径,各国都对这一科技感兴趣,我国也取得了较大进展。如图是核聚变燃料氦的原子结构模型。下列说法正确的是( )
A.“ ”表示的是质子B.氦的相对原子质量为5C.氦原子核外有2个电子D.氦原子的核电荷数为3
5.(2020•章贡区模拟)下列结构示意图表示稀有气体原子的是( )
6.(2020•天桥区二模)下列对相应微粒的描述中,正确的是( )
A.微粒甲在化学反应中易失电子B.微粒乙示意图第三层有2个电子C.微粒丙为阳离子 D.微粒丁化学性质比较活泼
化学九年级上册课题2 原子的结构教案配套ppt课件: 这是一份化学九年级上册课题2 原子的结构教案配套ppt课件,共60页。
人教版九年级上册第三单元 物质构成的奥秘课题2 原子的结构多媒体教学课件ppt: 这是一份人教版九年级上册第三单元 物质构成的奥秘课题2 原子的结构多媒体教学课件ppt,共46页。PPT课件主要包含了核外电子的排布,原子结构示意图,离子的形成,基础练习,能力提高等内容,欢迎下载使用。
初中化学人教版九年级上册第三单元 物质构成的奥秘课题2 原子的结构教课ppt课件: 这是一份初中化学人教版九年级上册第三单元 物质构成的奥秘课题2 原子的结构教课ppt课件,共21页。PPT课件主要包含了课前导入,课堂探究,原子的质量测定值,碳原子质量,碳原子质量的112,Ar=,定义式,近似值,测定出来绝对的,比较得出相对的等内容,欢迎下载使用。