

安徽省蚌埠田家炳中学2019-2020学年高一下学期开学学业检测化学试题
展开蚌埠田家炳中学高一化学必修二检测卷
第Ⅰ卷 (选择题 共54分)
一、 单项选择题(每小题3分,共54分。在每小题所列的四个选项中,只有一项是符合题目要求的,请把答案的字母序号填涂在答题卡上。)
1.为纪念编制元素周期表的俄国化学家,人们把第101号元素(人工合成元素)命名为钔(元素符号为Md),这位科学家是( )
A.拉瓦锡 B.波尔 C.门捷列夫 D.道尔顿
2.通常用来衡量一个国家的石油化学工业发展水平的标志是 ( )
A.石油产量 B.乙烯的产量
C.合成纤维的产量 D.硫酸的产量
3. 决定元素种类的因素是( )
A.核外电子数 B.最外层电子数 C.核电荷数 D.中子数
4. 下列物质之间的相互关系错误的是( )
A.CH3CH2OH和CH3OCH3互为同分异构体
B.干冰和冰为同一种物质
C.CH3CH3和CH3CH2CH3互为同系物
D.O2和O3互为同素异形体
5. 相同状况下,在容积相同的三个烧瓶内分别充满干燥的NH3、HCl、NO2气体,做喷泉实验,所得三种溶液的物质的量浓度比为( )
A.3∶3∶2 B.2∶2∶3
C.1∶1∶1 D.无法确定
6.下列措施对增大反应速率明显有效的是( )
A.Na与无水乙醇反应时增大无水乙醇的用量
B.Zn与25%的稀硫酸反应制取H2时,改用98%的浓硫酸
C.在K2SO4与BaCl2两溶液反应时,增大压强
D.将炭块磨成炭粉用于燃烧
7.已知某反应aA(g)+bB(g)==cC(g)的各物质浓度数据如下:
| A | B | C |
起始浓度(mol·L-1) | 3.0 | 1.0 | 0 |
2 s末浓度(mol·L-1) | 1.8 | 0.6 | 0.8 |
据此可推算出a∶b∶c是( )
A.9∶3∶4 B.3∶1∶2 C.2∶1∶3 D.3∶2∶1
8.下列反应中生成物总能量高于反应物总能量的是( )
A.碳酸钙受热分解 B.乙醇燃烧
C.铝粉与氧化铁粉末反应 D.氧化钙溶于水
9.下列物质属于同分异构体的一组是 ( )
A.淀粉和纤维素
B.CH3-CH2-CH2-CH3 与
C.1H 和2H
D.O2与O3
10.下列微粒中: 其核外电子数相同的 是( )
A.①②③ B.②③④
C.①②④ D.①③④
11.有关化学用语正确的是( )
A.乙烯的结构简式CH2CH2 B.乙醇的结构简式C2H6O
C.四氯化碳的结构式CCl4 D.乙酸的分子式C2H4O2
12.下列物质中,只含有离子键,不含有共价键的是 ( )
A.HCl B.KOH C.CaCl2 D.NH4 NO3
13.下列反应中,属于取代反应的是 ( )
A. 乙烯在空气中燃烧 B. 乙烷在空气中燃烧
C. 乙烯使氯水褪色 D. 乙烷与氯气在光照下颜色变浅
14、下列化合物中既含有离子键又含有共价键的是 ( )
A.HNO3 B.CaCl2 C. NH4Cl D.H2SO4
15.可逆反应达到化学平衡的标志是( )。
A.正、逆反应不再进行 B.反应物的浓度为零
C.正、逆反应都还在继续进行 D.正、逆反应的速率相等
16.将铜棒和锌棒用导线连接后插入稀硫酸溶液中,下列叙述中正确的是( )。
A.该装置能形成原电池,其中锌是负极
B.该装置能形成原电池,其中铜是负极
C.该装置不能形成原电池 D.以上说法均不正确
17.某阳离子X2+有m个电子,其质量数为a,则核内中子数为( )。
A.m+2 B.m+5 C.a-m+2 D.a-m-2
18.把a、b、c、d四种金属片浸泡在稀H2SO4中,用导线两两相连可以组成各种原电池。若a、b相连时,a为负极;c、d相连时,c为负极;a、c相连时,c为正极;b、d相连时,b为正极,则这四种金属活动性顺序由大到小为( )
A.a>b>c>d B.a>c>d>b C.c>a>b>d D.b>d>c>a
第Ⅱ卷 (非选择题 共46分)
二、填空题:(方程式每空3分,其余每空2分)
19.(6分)微粒2311Na+ 中的质子数是 ,
中子数是 ,核外电子数是 .
20.(8分)有下列四种微粒:①168O、②2311Na、③2412Mg、④14 7N
(1)按原子半径由大到小顺序排列的是________________________
(用序号回答,下同)
(2)微粒中质子数小于中子数的是______________________________
(3)在化合物中呈现的化合价的数值最多的是____________________
(4)能形成X2Y2型化合物的是___________。
21.(8分)请写出下列微粒的电子式
N2: CO2:
MgCl2: NaOH :
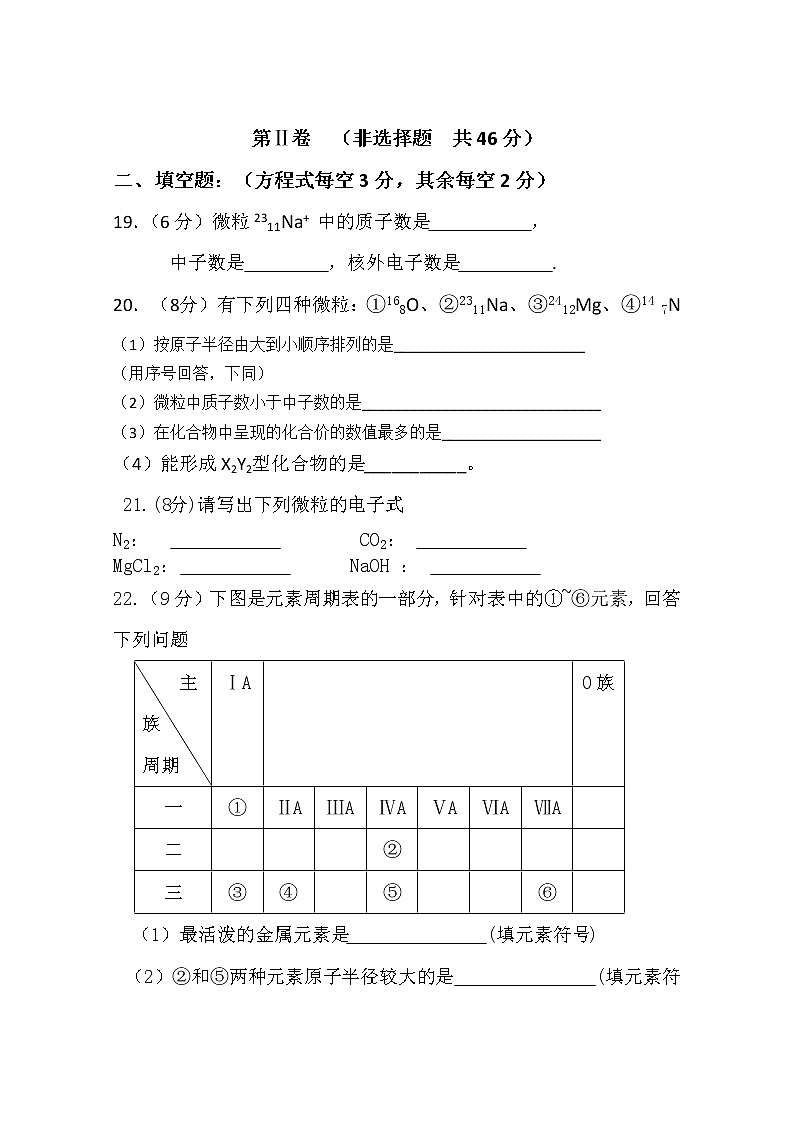
22.(9分)下图是元素周期表的一部分,针对表中的①~⑥元素,回答下列问题
主族 周期 | ⅠA |
| 0族 | |||||
一 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
|
二 |
|
|
| ② |
|
|
|
|
三 | ③ | ④ |
| ⑤ |
|
| ⑥ |
|
(1)最活泼的金属元素是 (填元素符号)
(2)②和⑤两种元素原子半径较大的是 (填元素符号),⑤和⑥两种元素最高价氧化物对应的水合物酸性较强的是 (填元素符号);
(3)写出①的单质在⑥的单质中燃烧的化学方程式 。
23.(9分)气体A的产量可以用来衡量一个国家石油化工发展水平。下图是由A为原料生产B的转化关系图,B是一种有香味的液体。
(1)将A通入滇水中,观察到的实验现象是__________,A分子中的官能团是______。
(2)写出CH3CH2OH与CH3COOH反应生成B的化学方程式_____________________。
(3)写出乙醇的一种用途____________________________________。
三、计算题(6分)( 原子量 H:1 Fe:56 )
24.非物质文化遗产“芜湖铁画”的某些产品中含有铁、金和碳等成分(其他成分忽略不计)。某同学取一定质量的铁画废弃样品,加入100mL稀盐酸中,恰好完全反应,放出0.3gH2,剩余固体质量为0.1g。请计算:
(1)样品中铁的质量分数。
(2)稀盐酸的物质的量浓度。
答案
一、选择题(每题3分,共54分)
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
C | B | C | B | C | D | B | A | B |
10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
C | D | C | D | C | D | A | D | B |
二、填空题(方程式每空3分,其余每空2分)
19、(1)11 (2)12 (3)10
20、(1)②③④① (2)② (3)④ (4)②①
21、(1) (2)
(3) (4)
22、(1)Na (2)Si (3)Cl (3)H2+Cl22HCl
23、(1)溴水褪色(或溶液褪色,合理答案均可得分) 碳碳双键(或)
(2)CH3COOH+CH3CH2OHCH3COOCH2CH3+H2O
(3)燃料(或化工原料等,合理答案均可得分)
三、计算题(6分)
24、(1)98.8% (2)3mol·L-1
(方程式1分,答案一个一分,过程3分)








