

所属成套资源:高一化学必修第二册(2019人教版)课件全套+课时作业全套(含详细解析)
人教版 (2019)必修 第二册化学反应与能量变化课后测评
展开 这是一份人教版 (2019)必修 第二册化学反应与能量变化课后测评,共8页。
[学业达标]
1.下列对化学反应的认识错误的是( )
A.会引起化学键的变化
B.会产生新的物质
C.必然引起物质状态的变化
D.必然伴随着能量的变化
2.如图表示化学反应过程中的能量变化,据图判断下列说法中合理的是( )
A.CaO、浓硫酸分别加入水中时的能量变化符合图1
B.500 mL 2.0 ml·L-1 H2SO4溶液和500 mL 2.0 ml·L-1 Ba(OH)2溶液的反应符合图1
C.发生图1能量变化的任何反应,一定不需要加热即可发生
D.500 mL 2.0 ml·L-1盐酸和500 mL 2.0 ml·L-1 NaOH溶液的反应符合图2
3.下列变化中属于吸热反应的是( )
①液态水汽化 ②将胆矾加热变成白色粉末
③浓硫酸稀释 ④氯酸钾分解制氧气
⑤生石灰跟水反应生成熟石灰
A.①④ B.②③
C.①④⑤ D.②④
4.下图是一个一次性加热杯的示意图。当水袋破裂时,水与固体碎块混合,杯内食物温度逐渐上升。制造此加热杯可选用的固体碎块是( )
A.硝酸铵 B.生石灰
C.氯化镁 D.食盐
5.参照反应Br+H2―→HBr+H的能量随反应过程变化的示意图(如下图所示),下列叙述中正确的是( )
A.反应物具有的总能量大于生成物具有的总能量
B.正反应为吸热反应
C.该反应的逆反应是吸热过程
D.从图中可以看出,HBr的能量一定高于H2的能量
6.已知化学反应A2(g)+B2(g)===2AB(g)的能量变化如图所示,判断下列叙述中正确的是( )
A.每生成2分子AB(g)吸收b kJ热量
B.该反应热ΔH=+(a-b) kJ/ml
C.该反应中反应物的总能量高于生成物的总能量
D.断裂1 ml A—A和1 ml B—B键,放出a kJ能量
7.[2022·邢台高一检测]我国空间站预计建成后可承载试验能力大幅提高,而且长期连续运行。为此,需要提前造好飞船,根据空间站航天员乘组更换要求和货物运输需求,按需发射,“有点像航空公司的航班”。航天飞船可用肼(N2H4)作动力源。
已知1 g液态肼和足量的液态过氧化氢反应生成N2和水蒸气时放出20.05 kJ热量,化学方程式如下:N2H4+2H2O2===N2↑+4H2O。下列说法中错误的是( )
A.该反应中肼作还原剂
B.此情况下,液态肼燃烧生成1 ml N2时放出的热量为641.6 kJ
C.肼(N2H4)分子中只存在极性共价键
D.该反应的反应物总能量高于生成物的总能量
8.化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的。如图表示N2(g)与O2(g)反应生成NO(g)过程中的能量变化:
下列说法中正确的是( )
A.1 ml N2(g)与1 ml O2(g)反应放出的能量为180 kJ
B.1 ml N2(g)和1 ml O2(g)具有的总能量小于2 ml NO(g)具有的总能量
C.通常情况下,N2(g)与O2(g)混合能直接生成NO(g)
D.NO是一种酸性氧化物,能与NaOH溶液反应生成盐和水
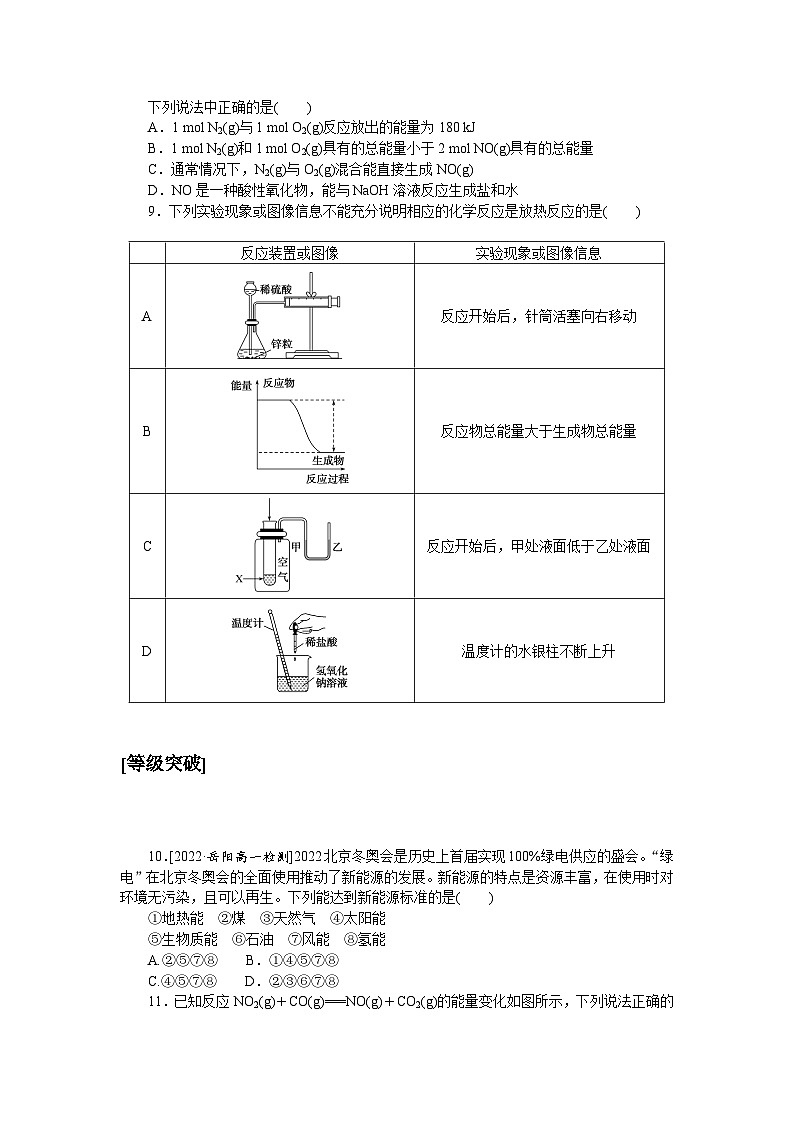
9.下列实验现象或图像信息不能充分说明相应的化学反应是放热反应的是( )
[等级突破]
10.[2022·岳阳高一检测]2022北京冬奥会是历史上首届实现100%绿电供应的盛会。“绿电”在北京冬奥会的全面使用推动了新能源的发展。新能源的特点是资源丰富,在使用时对环境无污染,且可以再生。下列能达到新能源标准的是( )
①地热能 ②煤 ③天然气 ④太阳能
⑤生物质能 ⑥石油 ⑦风能 ⑧氢能
A.②⑤⑦⑧ B.①④⑤⑦⑧
C.④⑤⑦⑧ D.②③⑥⑦⑧
11.已知反应NO2(g)+CO(g)===NO(g)+CO2(g)的能量变化如图所示,下列说法正确的是( )
A.图中A→B的过程为放热过程
B.1 ml NO2和1 ml CO的键能总和大于1 ml NO和1 ml CO2的键能总和
C.该反应为氧化还原反应
D.1 ml NO2(g)和1 ml CO(g)的总能量低于1 ml NO(g)和1 ml CO2(g)的总能量
12.为消除目前燃料燃烧时产生的环境污染,同时缓解能源危机,有关专家提出了利用太阳能制取氢能的构想。下列说法正确的是( )
A.H2O的分解反应是放热反应
B.氢能源已被普遍使用
C.氢气不易贮存和运输,无开发利用价值
D.2 ml H2O具有的总能量低于2 ml H2和1 ml O2具有的总能量
13.用Cl2生产某些含氯有机物时会产生副产物HCl。利用反应A,可实现氯的循环利用。
反应A:4HCl+O2 eq \(,\s\up7(CuO、CuCl2),\s\d5(400℃)) 2Cl2+2H2O
已知:反应A中,4 ml HCl被氧化,放出115.6 kJ的热量。
(1)H2O的电子式是________。
(2)断开1 ml H—O键与断开1 ml H—Cl键所需能量相差约为________kJ;H2O中H—O键比HCl中H—Cl键________(填“强”或“弱”)。
14.为了探究化学能与热能的转化,某实验小组设计了如下三套实验装置:
(1)上述三套装置中,不能证明“铜与浓硝酸反应是吸热反应还是放热反应”的是________。
(2)某同学选用装置Ⅰ进行实验(实验前U形管里液面左右相平),在甲试管里加入适量氢氧化钡溶液与稀硫酸,U形管中可观察到的现象是________________________________________________________________________
________________________________________________________________________,
说明该反应属于________(填“吸热”或“放热”)反应。
(3)为探究固体M溶于水的热效应,选择装置Ⅱ进行实验(反应在甲中进行)。
①若M为钠,则实验过程中烧杯中可观察到的现象是________________________________________________________________________。
②若观察到烧杯里产生气泡,则说明M溶于水________________(填“一定是放热反应”“一定是吸热反应”或“可能是放热反应”),理由是________________________________________________________________________
________________________________________________________________________。
③若观察到烧杯里的玻璃管内形成一段水柱,则M可能是________________________________________________________________________。
(4)至少有两种实验方法能证明超氧化钾与水的反应(4KO2+2H2O===4KOH+3O2↑)是放热反应还是吸热反应。方法①:选择上述装置________(填“Ⅰ”“Ⅱ”或“Ⅲ”)进行实验。方法②:取适量超氧化钾粉末用脱脂棉包裹并放在石棉网上,向脱脂棉上滴加几滴蒸馏水,片刻后,若观察到棉花燃烧,则说明该反应是________反应。
课时作业8 化学反应与热能
1.解析:化学反应的本质是化学键的断裂和形成,表现为有新物质生成,并伴随着能量的变化,而化学变化中的反应物和生成物的状态在反应前后可能相同,也可能不相同,C错误。
答案:C
2.解析:浓硫酸稀释时没有发生化学反应,只是放热过程,A错误;H2SO4和Ba(OH)2的反应为放热反应,反应物的总能量大于生成物的总能量,B正确;图1表示放热反应,有些放热反应需要加热,如铝热反应属于放热反应,但需要高温条件才能发生,C错误;酸碱中和反应为放热反应,反应物的总能量高于生成物的总能量,符合图1的能量变化曲线,D错误。
答案:B
3.解析:放热反应和吸热反应都是化学反应。放热反应为⑤,吸热反应为②④,液态水汽化是吸热过程,浓H2SO4稀释是放热过程,二者均为物理变化。
答案:D
4.解析:生石灰与水反应放出大量的热。
答案:B
5.解析:从示意图中可以看出,反应物Br+H2先吸收117 kJ·ml-1能量,然后放出42 kJ·ml-1能量。由于总能量是守恒的,因此反应物具有的总能量低于生成物具有的总能量,则正反应是吸热反应,逆反应是放热反应,故A、C两项错误,B项正确。根据图中信息,不能看出HBr与H2的能量谁高谁低,D项错误。
答案:B
6.解析:形成化学键放出热量,每生成2 ml AB放出b kJ热量,A项错误;该反应焓变=断裂化学键吸收热量-形成化学键所放出热量,所以焓变为ΔH=+(a-b) kJ/ml;B项正确;反应是吸热反应,依据能量守恒可知,反应中反应物的总能量低于生成物的总能量,故C项错误;断裂1 ml A—A键和1 ml B—B键,吸收a kJ能量,D项错误。
答案:B
7.解析:反应中N2H4中-2价N元素被氧化成N2,N2H4在反应中作还原剂,A项正确;生成1 ml N2需要1 ml N2H4,即32 g N2H4,此时共放热20.05 kJ×32=641.6 kJ,B项正确;在N2H4中既存在N—H极性键又存在N—N非极性键,C项不正确;该反应为放热反应,说明反应物总能量高于生成物总能量,D项正确。
答案:C
8.解析:1 ml N2(g)与1 ml O2(g)反应吸收的能量为946 kJ+498 kJ-2×632 kJ=180 kJ,A错误;1 ml N2(g)和1 ml O2(g)具有的总能量小于2 ml NO(g)具有的总能量,B正确;在放电条件下,N2(g)与O2(g)混合能直接生成NO(g),C错误;NO不是酸性氧化物,与NaOH溶液不反应,D错误。
答案:B
9.解析:稀硫酸和锌反应生成氢气,反应开始后,能使针筒活塞向右移动,不能说明反应放热,A项符合题意;从能量守恒的角度分析,反应物总能量大于生成物总能量,为放热反应,B项不符合题意;反应开始后,甲处液面低于乙处液面,说明装置内温度升高,压强增大,反应为放热反应,C项不符合题意;稀盐酸和氢氧化钠溶液发生中和反应,可观察到温度计的水银柱不断上升,说明为放热反应,D项不符合题意。
答案:A
10.解析:煤、石油、天然气是化石能源,不可再生,不属于新能源;新能源有太阳能、地热能、海洋能、风能、氢能、生物质能等,这些新能源对环境污染小,属于环境友好型能源,即符合条件的是①④⑤⑦⑧,故选B。
答案:B
11.解析:图中A→B的过程为吸热过程,A项错误;反应物总能量高于生成物总能量,则1 ml NO2和1 ml CO的键能总和小于1 ml NO和1 ml CO2的键能总和,B项错误;反应中C和N元素的化合价发生变化,则该反应为氧化还原反应,C项正确;该反应为放热反应,则1 ml NO2(g)和1 ml CO(g)的总能量高于1 ml NO(g)和1 ml CO2(g)的总能量,D项错误。
答案:C
12.解析:水的分解是吸热反应,A错误;氢能源由于受贮存和运输等因素的限制,还未普遍使用,但有巨大的开发利用价值,B、C错误;2 ml H2在1 ml O2中完全燃烧生成2 ml H2O,并放出大量的热,D正确。
答案:D
13.解析:由题给条件可知,4 ml HCl被氧化,放出的热量为115.6 kJ,则4E(H—Cl)+E(O===O)-2E(Cl—Cl)-4E(H—O)=-115.6 kJ,即E(H—Cl)-E(H—O)= eq \f(-115.6 kJ-498 kJ+2×243 kJ,4) =-31.9 kJ。键能越大的化学键越强,所以H—O键比H—Cl键强。
答案:(1) (2)31.9 强
14.解析:(1)装置Ⅰ可通过U形管中红墨水液面的变化判断铜与浓硝酸的反应是放热还是吸热;装置Ⅱ可通过烧杯中是否产生气泡判断铜与浓硝酸的反应是放热还是吸热;装置Ⅲ只是铜与浓硝酸反应并将生成的气体用水吸收的装置,不能证明该反应是放热反应还是吸热反应。(2)氢氧化钡与稀硫酸反应属于中和反应,中和反应都是放热反应。(3)浓硫酸、硝酸铵溶于水有热效应,但不属于化学反应,故不是放热或吸热反应。
答案:(1)Ⅲ (2)左端液柱降低,右端液柱升高 放热 (3)①产生气泡,反应完毕后,冷却至室温,烧杯里的导管内形成一段液柱 ②可能是放热反应 某些物质(如浓硫酸)溶于水放热,但不是放热反应 ③硝酸铵(或其他合理答案) (4)Ⅰ(或Ⅱ) 放热
反应装置或图像
实验现象或图像信息
A
反应开始后,针筒活塞向右移动
B
反应物总能量大于生成物总能量
C
反应开始后,甲处液面低于乙处液面
D
温度计的水银柱不断上升
相关试卷
这是一份人教版 (2019)必修 第二册化学反应与能量变化课后测评,共8页。
这是一份高中化学人教版 (2019)必修 第二册化学反应与能量变化达标测试,共7页。
这是一份人教版 (2019)必修 第二册第六章 化学反应与能量第一节 化学反应与能量变化同步练习题,共7页。试卷主要包含了选择题,填空题等内容,欢迎下载使用。
相关试卷 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 






.png)




