




所属成套资源:2025-2026学年化学九年级上册课件(2024人教版)
初中化学人教版(2024)九年级上册(2024)分子和原子背景图ppt课件
展开 这是一份初中化学人教版(2024)九年级上册(2024)分子和原子背景图ppt课件,共48页。PPT课件主要包含了新课导入,原子核外电子的排布,Li+,Al3+,S2-,Ca2+,Mg2+,课堂总结,课堂小节等内容,欢迎下载使用。
3.2.2 原子核外电子的排布 离子一、原子核外电子的排布(一)分层排布规律引入:在了解原子由原子核和核外电子构成的基础上,指出核外电子在核外空间做高速运动,且是分层排布的。科学家把能量最低、离核最近的电子层称为第一层,由里往外依次为第二层、第三层…… ,目前发现最多有七个电子层。规律讲解:电子总是优先排布在能量低的电子层,排满一层后再排下一层。例如,第一层最多能容纳 2 个电子,当第一层排满 2 个电子后,电子才会排布到第二层 。第二层最多容纳 8 个电子,最外层电子数不超过 8 个(只有 1 个电子层时,最多容纳 2 个电子) 。以钠原子(核电荷数为 11)为例,其核外 11 个电子的排布为:第一层 2 个电子,第二层 8 个电子,第三层 1 个电子 。图示辅助:通过绘制钠原子、氧原子等常见原子的核外电子分层排布示意图,标注各电子层的电子数,让学生直观理解电子的分层排布方式。(二)原子结构示意图结构解析:以氧原子结构示意图为例,讲解原子结构示意图的组成。小圈表示原子核,圈内数字表示核内质子数;弧线表示电子层,弧线上的数字表示该层上的电子数 。氧原子结构示意图中,小圈表示氧原子核,圈内数字 “8” 表示氧原子核内有 8 个质子,两条弧线分别代表第一层和第二层电子层,弧线上的数字 “2” 和 “6” 分别表示第一层有 2 个电子,第二层有 6 个电子 。绘制练习:给出几种元素的原子(如镁原子、氯原子),让学生尝试绘制其原子结构示意图,巩固对原子结构示意图的理解和绘制方法。(三)最外层电子数与元素化学性质的关系金属元素:以钠、镁等金属原子为例,它们的最外层电子数一般少于 4 个。在化学反应中,金属原子容易失去最外层电子,使次外层变为最外层,达到相对稳定结构(一般认为最外层电子数为 8 个,只有 1 个电子层时为 2 个是相对稳定结构) 。失去电子后,金属元素的化合价通常显正价,如钠原子最外层 1 个电子,在化学反应中易失去 1 个电子,形成钠离子,钠元素在化合物中通常显 +1 价 。非金属元素:以氧、氯等非金属原子为例,其最外层电子数一般多于 4 个。在化学反应中,非金属原子容易得到电子,使最外层达到 8 个电子的相对稳定结构 。得到电子后,非金属元素的化合价通常显负价,如氧原子最外层 6 个电子,在化学反应中易得到 2 个电子,形成氧离子,氧元素在化合物中通常显 -2 价 。稀有气体元素:氦、氖、氩等稀有气体元素的原子,最外层电子数为 8 个(氦为 2 个),是相对稳定结构。在通常情况下,稀有气体元素的化学性质稳定,不易与其他物质发生化学反应 。由此得出结论:元素的化学性质与原子的最外层电子数密切相关。二、离子(一)离子的形成以钠与氯气反应生成氯化钠为例,讲解离子的形成过程。钠原子最外层 1 个电子,容易失去 1 个电子,使核外电子排布变为 2、8 的稳定结构,此时钠原子带上 1 个单位的正电荷,形成钠离子,符号为\(Na^{+}\);氯原子最外层 7 个电子,容易得到 1 个电子,使核外电子排布变为 2、8、8 的稳定结构,此时氯原子带上 1 个单位的负电荷,形成氯离子,符号为\(Cl^{-}\) 。带相反电荷的钠离子和氯离子相互作用,形成稳定的化合物氯化钠,这种带电的原子或原子团叫做离子 。动画演示:通过动画动态展示钠原子失电子、氯原子得电子以及阴阳离子相互结合形成化合物的过程,帮助学生更清晰地理解离子的形成机制。(二)离子的分类阳离子:带正电荷的离子叫做阳离子,如钠离子(\(Na^{+}\))、镁离子(\(Mg^{2+}\))、铵根离子(\(NH_{4}^{+}\))等 。阳离子是原子失去电子形成的,失去电子的数目就是离子所带正电荷的数目,如镁原子失去 2 个电子形成带 2 个单位正电荷的镁离子 。阴离子:带负电荷的离子叫做阴离子,如氯离子(\(Cl^{-}\))、氧离子(\(O^{2 - }\))、硫酸根离子(\(SO_{4}^{2 - }\))等 。阴离子是原子得到电子形成的,得到电子的数目就是离子所带负电荷的数目,如氧原子得到 2 个电子形成带 2 个单位负电荷的氧离子 。(三)离子符号的书写与意义书写方法:离子符号的书写是在元素符号(或原子团)的右上角标明离子所带的电荷,数字在前,正负号在后。当离子所带电荷数为 1 时,“1” 省略不写 。例如,钠离子写成\(Na^{+}\),氢离子写成\(H^{+}\),硫酸根离子写成\(SO_{4}^{2 - }\) 。意义讲解:以\(Mg^{2+}\)为例,“\(Mg\)” 表示镁元素或镁原子,“\(2 +\)” 表示每个镁离子带 2 个单位的正电荷;\(2Mg^{2+}\)表示 2 个镁离子,前面的数字 “2” 表示离子的个数 。通过多个例子,如\(3Cl^{-}\)、\(4O^{2 - }\)等,让学生准确理解离子符号及其表示的意义。三、课堂小结(一)知识总结回顾原子核外电子分层排布的规律、原子结构示意图的含义以及最外层电子数与元素化学性质的关系。梳理离子的形成过程、分类、离子符号的书写和意义,强调离子与原子的联系和区别 。(二)巩固提升布置思考问题:一种元素的原子变成离子后,其质子数、电子数、化学性质是否发生变化?为什么?通过思考和解答,加深学生对本节知识的理解和应用能力,同时为后续学习物质的组成和化学式的书写打下基础 。
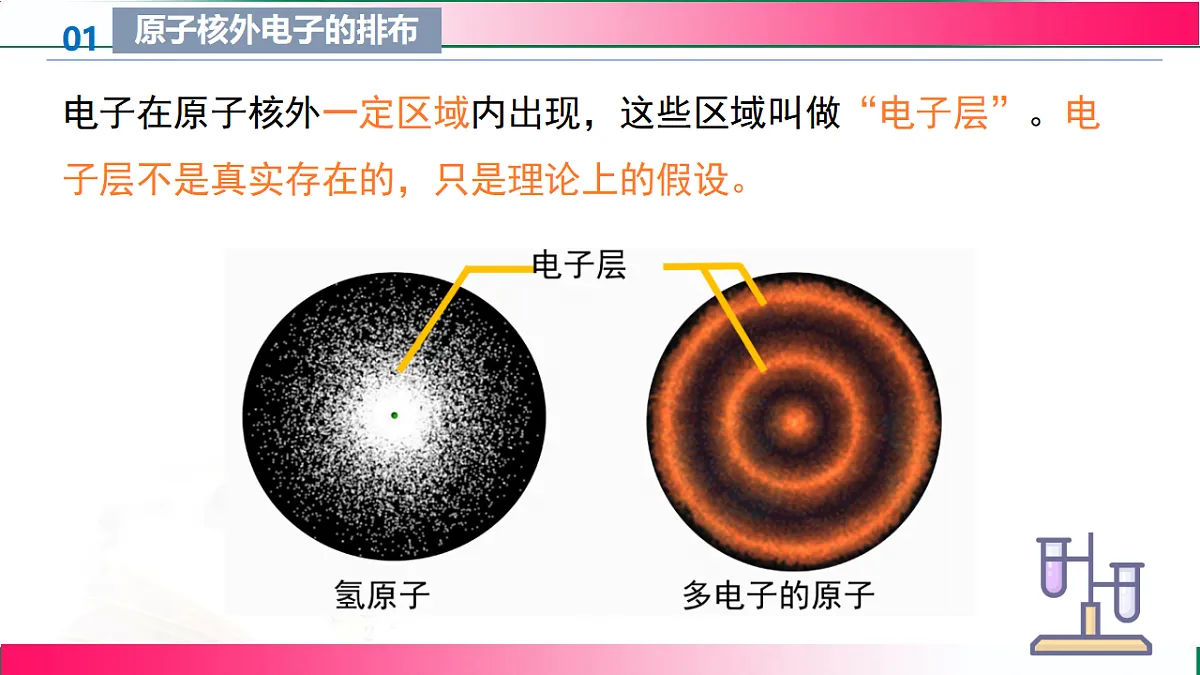
电子在原子核外一定区域内出现,这些区域叫做“电子层”。电子层不是真实存在的,只是理论上的假设。
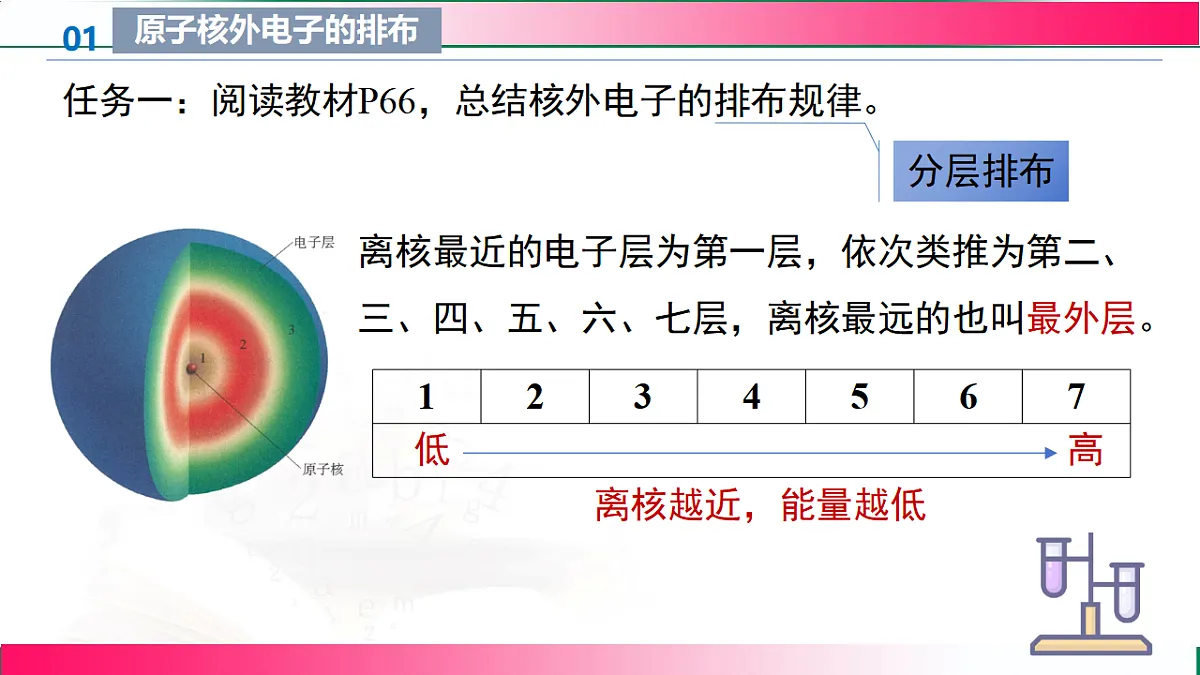
任务一:阅读教材P66,总结核外电子的排布规律。
离核最近的电子层为第一层,依次类推为第二、三、四、五、六、七层,离核最远的也叫最外层。
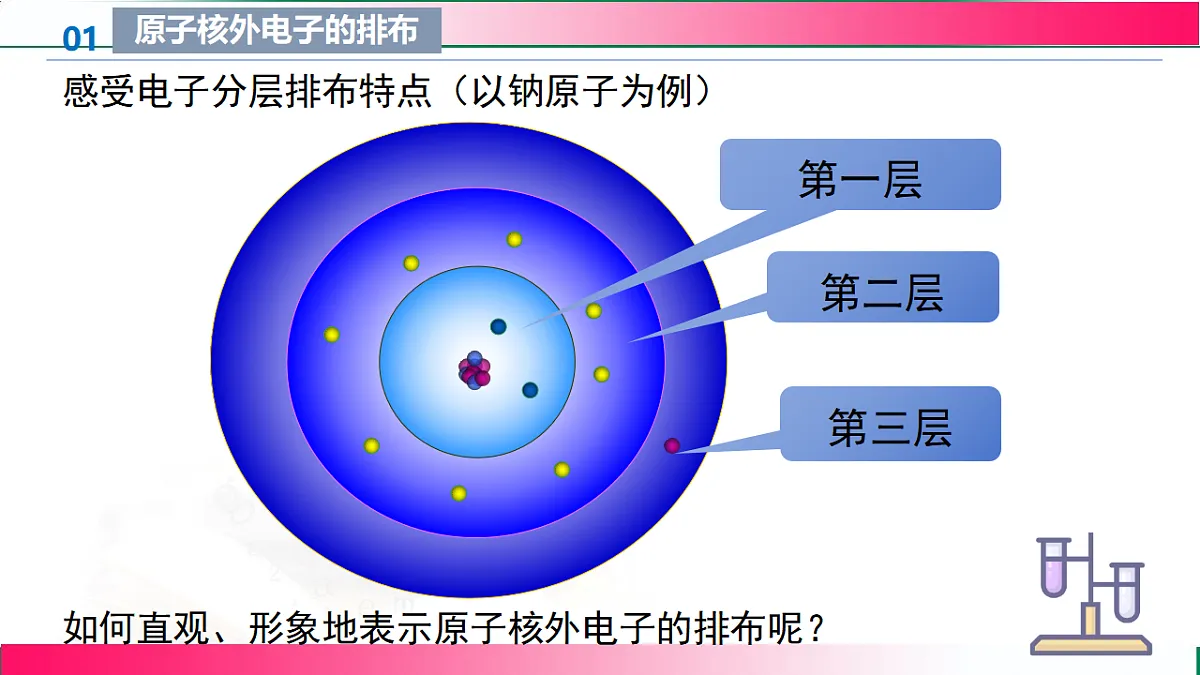
感受电子分层排布特点(以钠原子为例)
如何直观、形象地表示原子核外电子的排布呢?
简明表示原子核外电子的排布——原子结构示意图
任务二:观察下列原子的结构示意图,总结电子分层排布的规律。
1.第一层最多排__个电子,第二层最多排___个电子
2.最外层一般不超过 个电子(只有1层的,不超过 个电子)
1.试试画出下列原子的结构示意图。
任务三:阅读教材P67,结合原子结构示意图填写下表。
既不得电子,也不失电子
原子的最外层电子数决定原子的化学性质。
通常,最外层电子数相同,化学性质相似。
2.如图为某粒子的结构示意图,下列说法正确的是( )A.该粒子有12个质子 B.该粒子有2个电子层 C.该粒子属于非金属原子 D.该粒子已达到相对稳定结构
3.根据下列原子的结构示意图,回答下列问题:
(2)易失电子的原子的是 ;易得电子的原子的是 ;
(1)具有相对稳定结构的是 (填序号,下同);
(3)化学性质相似的是 。
任务四:分别画出钠原子和氯原子的结构示意图。
分析:钠原子和氯原子在反应中的得失电子趋势。
如果一个钠原子和一个氯原子相遇,会发生什么呢?
质子数= 电子数=
质子数= 电子数=
1.定义:带电荷的原子叫作离子。
离子也是构成物质的微观粒子
氯化钠(NaCl)是由____和____构成的。
2.书写:在原子(或原子团)符号的右上角标出离子所带的电荷数及电性,数值在前,正负号在后,当离子所带电荷数为1个单位时, 1 可以不写。
1.试试写出下列离子的离子符号。
1个氯离子带1个单位负电荷
表示一种离子及一个离子所带的电荷数
离子符号周围数字的意义:
表示每个镁离子带2个单位的正电荷
4.原子与离子的区别与联系
原子是化学变化中的最小微粒而离子是带电的原子
大多数原子是不稳定结构,而离子是稳定结构
2.下列关于离子的说法中不正确的是( )A.离子是构成物质的一种粒子B.氯化钠是由钠离子和氯离子构成的C.离子是一种不显电性的粒子D.在化学反应中离子和原子可以相互转化
3.“结构决定性质”是化学的核心观念。如图是硫原子结构示意图,下列说法正确的是( )A. X的值为8B.硫原子的核电荷数为16C.硫原子在化学反中易得到电子,变成阳离子D.硫原子和硫离子的性质完全相同
4. 根据下图所示的粒子结构示意图,回答问题:
① ② ③ ④ ⑤ ⑥
(1)属于相对稳定结构的是_________(2)核电荷数相同的的是______;(3)在反应中易失电子的是_____,易得电子的是_____;(4)属于原子的是_________,属于阳离子的是___;属于阴离子的是____;(5)属于稀有气体原子的是____,属于金属原子的是___,属于非金属原子的是______;(6)与①化学性质相似的是____。
1. 学习完“原子核外电子的排布”之后, 小明同学得到下列结论,其中不正确的是 ( )A. 与原子相比,原子核的体积更小B. 原子核外的电子按固定轨道围绕原子核作高速运动C. 离原子核近的电子能量较低D. 原子核外电子是分层排布的
2. [2025·威海模拟] 如图为铝原子结构示意图。下列有关铝原子的说法正确的是 ( )A. 图中“+”表示铝原子带正电B. 铝原子的中子数为13C. 铝原子的核外电子数为3D. 铝原子核外有3 个电子层
【点拨】图中“+”表示铝原子核带正电,原子不显电性,A 错误;圆圈内的“13”表示质子数,而不是中子数,B 错误;铝原子最外层电子数为3,核外电子数为13,C 错误;弧线表示电子层,由图可知,铝原子核外有3 个电子层,D 正确。
3. [2024·宿迁改编] 氯原子、碘原子结构示意图如图所示。下列说法正确的是 ( )A. 氯原子和碘原子的化学性质相似B. 氯原子最外电子层已达到稳定结构C. 氯原子为金属原子D. 碘原子在化学反应中易失去电子
【点拨】与元素化学性质关系最密切的是原子的最外层电子数,氯原子和碘原子的最外层电子数相同,都是7 个电子,化学性质相似,A 正确;最外层电子数为8(只有1 个电子层时,电子数为2)的结构,属于相对稳定结构,B 错误;氯原子属于非金属原子,C 错误;碘原子的最外层电子数是7,多于4,在化学反应中易得到1 个电子,D 错误。
4. [2025·张家口模拟] 根据下列各组原子的结构示意图进行判断,其中化学性质相似的一组是 ( )
【点拨】A 项,两种原子的最外层均为6 个电子,在反应中都易得到2 个电子形成8 个电子的稳定结构,化学性质相似,符合题意;B 项,钠原子最外层只有1 个电子,在反应中易失去1 个电子形成钠离子,钠离子性质较稳定,因此钠原子与钠离子的化学性质不相似,不符合题意;C 项,两种原子的最外层电子数均为2,但氦原子化学性质稳定,而镁原子在反应中易失去最外层的2 个电子形成相对稳定结构,化学性质不相似,不符合题意;D 项,两种原子的最外层电子数分别为1 和7,化学性质不相似,不符合题意。
【点易错】认识粒子结构示意图的常见误区:(1)最外层电子数为8 的结构是相对稳定结构,但注意氦原子的最外层电子数为2,也是相对稳定结构(它原子核外只有一个电子层)。(2)原子的化学性质与最外层电子数关系密切,但是最外层电子数相同的原子化学性质不一定相似,如氦与镁;化学性质相似的原子最外层电子数也不一定相同,如氦与氖。
5. [2024·苏州改编] 构成物质的微粒有分子、原子、离子等。下列物质由离子构成的是 ( )A. 水 B. 铜 C. 氯化钠 D. 金刚石
【点拨】水由水分子构成,铜由铜原子构成,氯化钠由钠离子和氯离子构成,金刚石由碳原子构成,故选C。
6. 下列微粒中,核电荷数少于核外电子数的是( )A. Na+ B. OH- C. O2 D. Mg
【点拨】OH- 为阴离子,带负电荷,其核电荷数少于核外电子数,B 正确。
7. 下列四种粒子的结构示意图中,表示阳离子的是 ( )
8. 如图为金属钠与氯气反应生成氯化钠的示意图,下列说法错误的是( )A. 每个氯离子带一个单位负电荷B. 钠原子在该反应中形成了阳离子C. 氯离子核外有2 个电子层D. 钠离子和氯离子的结构都相对稳定
9. 科学家研制的一种以铯原子做钟摆的钟是目前世界上最精确的钟。铯原子的结构示意图如图1 所示。(1)铯原子的核内质子数为________,原子核外有________个电子层,在化学反应中容易__________ (填“得到”或“失去”)电子。
10. [2024·深圳期末]X、Y、Z、Q 四种原子的核外电子数分别为a、b、c、d(均小于18),若它们的离子Xm+、Yn+、Zm-、Qn- 的核外电子排布相同,则下列关系中,正确的是( )A. a-b=n-m B. b-d=2nC. c-d=m+n D. a-c=0
原子失去电子形成阳离子,带正电原子得到电子形成阴离子,带负电
mXn+ mXn-
(2)决定原子化学性质的粒子是原子的( )。 A. 核内中子数 B. 核内质子数 C. 最外层电子数 D. 核外电子数(3)核电荷数少于核外电子数的一定是( )。 A. 分子 B. 原子 C. 阳离子 D. 阴离子
(1)B所表示的原子在化学反应中容易 (填 “得到”或“失去”)电子,形成 (填“阳” 或“阴”)离子,离子符号为 。(2)表示原子的是 (填字母,下同)。
3.如图是几种粒子的结构示意图:
(3)表示阴离子的是 ,表示阳离子的是 。(4)具有相对稳定结构的是 。(5)化学性质相似的原子是 。
相关课件 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 


.png)




