


所属成套资源:化学鲁科版 2019 必修第一册 全章专项训练 + 题型突破资源包(含答案)
化学铁的多样性综合训练题
展开 这是一份化学铁的多样性综合训练题,文件包含第1节铁的多样性专项训练原卷版docx、第1节铁的多样性专项训练解析版docx等2份试卷配套教学资源,其中试卷共52页, 欢迎下载使用。
\l "_Tc17993" 题型01 铁的氧化物性质及应用
题型02 亚铁盐的化学性质
题型03 铁盐的化学性质
题型04 Fe2+与Fe3+的检验
题型05 氢氧化亚铁的制备
题型06 铁与水蒸气反应
题型07 铁及其化合物的性质及转化关系
题型08 铁及其化合物综合实验探究
题型01 铁的氧化物性质及用途
【典例1】化学品在造纸工业中有着重要的应用。下列说法错误的是
A.碳酸钠用作纸浆抗氧化剂 B.双氧水用作纸浆漂白剂
C.氢氧化钠用于脱除木质素 D.氧化铁红用作纸张染色剂
【变式1-1】性质决定用途,下列物质的性质、用途描述均正确且有关联的是
A.是红棕色粉末,可用作油漆的红色涂料
B.金属铝表面有致密的氧化膜,铝制餐具可用于蒸煮酸性或碱性食物
C.是淡黄色固体,可用作潜水艇供氧剂
D.不锈钢的抗腐蚀能力强,可用作医疗器材
【变式1-2】建筑用的红砖和青砖,其颜色是由其中含有的不同价态的铁的氧化物所致。我国古代砖瓦建筑能够保持到现在的,几乎无一例外是由青砖建成的。有人提出以下可能的原因:你认为合理的是:
①青砖中含的是FeO;②青砖中含的是Fe2O3;③Fe2O3遇长期酸雨侵蚀会风化溶解使砖瓦强度降低;④ Fe2O3性质稳定;⑤FeO性质稳定
A.①③⑤B.②③④C.③⑤D.①②③④
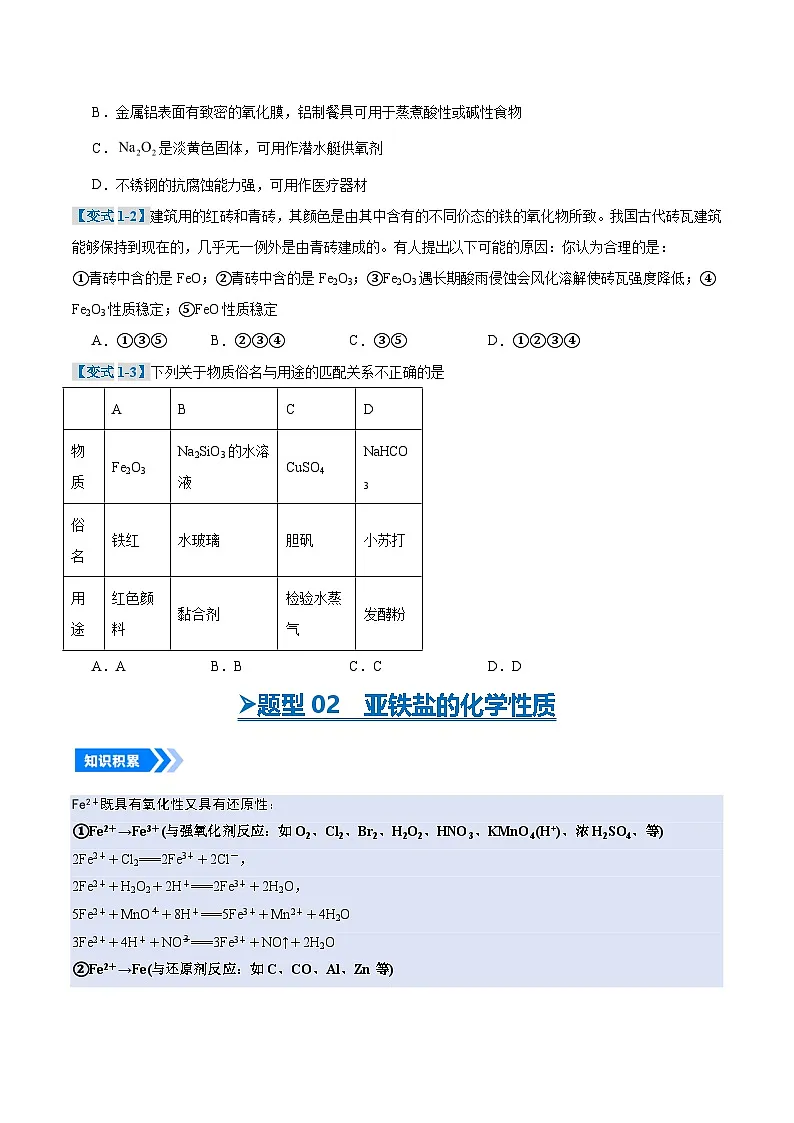
【变式1-3】下列关于物质俗名与用途的匹配关系不正确的是
A.AB.BC.CD.D
题型02 亚铁盐的化学性质
Fe2+既具有氧化性又具有还原性:
①Fe2+→Fe3+(与强氧化剂反应:如O2、Cl2、Br2、H2O2、HNO3、KMnO4(H+)、浓H2SO4、等)
2Fe2++Cl2===2Fe3++2Cl-,
2Fe2++H2O2+2H+===2Fe3++2H2O,
5Fe2++MnOeq \\al(-,4)+8H+===5Fe3++Mn2++4H2O
3Fe2++4H++NOeq \\al(-,3)===3Fe3++NO↑+2H2O
②Fe2+→Fe(与还原剂反应:如C、CO、Al、Zn等)
Zn+Fe2+===Zn2++Fe FeO+COeq \(=====,\s\up7(△))Fe+CO2。
亚铁盐是补铁保健品的主要成分,其铁元素处于+2价,易被氧化,需密封保存;与维生素C同服能增强补铁功效。
【典例2】下列物质的保存方法不正确的是
A.漂白液需避光保存B.干燥的液氯保存在铁质容器中
C.保存溶液时可加适量铁粉D.锂和钠均可保存在煤油中
【变式2-1】下列离子方程式书写正确的是
A.向溶液中滴加少量盐酸:
B.向溶液中通入少量:
C.将Na投入溶液中:
D.向溶液中加入少量溶液:
【变式2-2】某小组验证的性质,进行如下实验。
(1)画出Fe的离子结构示意图 。
(2)实验①中的试剂X是 (填序号)。
a. b. c.₃ d.
(3)实验②中的现象是 ,用化学用语解释该现象,能写离子方程式的写离子方程式 。
(4)实验③体现了的 性。
(5)实验④还能证明溶液中无三价铁,实验操作及现象是 ,发生的离子方程式 。
【变式2-3】用KSCN溶液和溶液探究的还原性时出现异常现象,实验如下:
下列说法不正确的是
A.对比①③,可判定酸性条件下可氧化
B.实验②中发生的氧化还原反应有两种
C.②中红色溶液中含有胶体
D.③中发生的氧化还原反应为:
题型03 铁盐的化学性质
Fe3+具有较强氧化性,可被还原为Fe2+或Fe。
①Fe3+→Fe2+(与还原剂反应:如Fe、Cu、I-、S2-等)
2Fe3++Cu===2Fe2++Cu2+,
2Fe3++H2S===2Fe2++S↓+2H+。
2Fe3++2I-===I2+2Fe2+
②Fe3+→Fe(与还原剂反应:如C、CO、Al等)
Fe2O3+3COeq \(=====,\s\up7(高温))2Fe+3CO2 Fe2O3+2Aleq \(=====,\s\up7(高温))2Fe+Al2O3。
【典例3】下列有关物质的性质或应用的描述错误的是
A.AB.BC.CD.D
【变式3-1】某同学探究镁条与FeCl3溶液的反应。操作与现象如下:
① 向盛有过量镁条的试管中加入0.5 ml·L-1 FeCl3溶液,立即产生大量气泡,一段时间后,出现大量红褐色沉淀,镁条表面有固体附着。
② 取少量上层清液于试管中,滴加K3[Fe(CN)6]溶液,有蓝色沉淀产生。
③ 取反应后的镁条于试管中,加入盐酸,产生气泡,取与盐酸反应后的溶液于试管中,滴加K3[Fe(CN)6]溶液,有蓝色沉淀产生。
下列说法不正确的是:
A.①中产生大量气泡的原因:镁条与溶液中H+反应产生H2
B.①中产生红褐色沉淀的原因:c(H+)减小,Fe3+ +3H2OFe(OH)3 +3H+正向移动
C.②中现象说明镁条与Fe3+发生反应:Mg + 2Fe3+ = Mg2+ + 2Fe2+
D.③中的实验现象说明镁条表面附着的固体有铁单质
【变式3-2】常温下,下列各组离子在指定溶液中能大量共存的是
A.氨水中:
B.稀硫酸中:
C.溶液中:
D.无色溶液中:
【变式3-3】下列关于和两种溶液的说法错误的是(双选)
A.保存时均需加入少量铁粉
B.可利用与铜粉的反应比较的氧化性强弱
C.分别加入溶液,久置后均能观察到红褐色沉淀
D.可用酸性溶液鉴别和溶液
题型04 Fe2+与Fe3+的检验
1.Fe2+的检验
2.Fe3+的检验
若无其它还原性物质干扰,可用酸性KMnO4溶液区别Fe2+、Fe3+:Fe2+能使紫色褪去,Fe3+无明显现象。
【典例4】下列离子的检验方法合理的是
A.向某溶液中滴入KSCN溶液显红色,说明不含Fe2+
B.向某溶液中通入Cl2,然后再加入KSCN溶液变红色,说明原溶液中含有Fe2+
C.向某溶液中加入NaOH溶液,得到红褐色沉淀,说明溶液中含有Fe3+
D.向某溶液中加入NaOH溶液得白色沉淀,又观察到颜色逐渐变为红褐色,说明溶液中含有Fe2+,不含有Mg2+
【变式4-1】氯化铁是常用的金属刻蚀剂。从刻蚀电路板后的废液(含)中回收铜,并重获溶液的流程图如下:
下列说法正确的是
A.检验“废液”中含有的方法:先加KSCN溶液,再滴加氯水
B.若①为铁粉,则滤渣③中只含铜
C.以上涉及反应均属于氧化还原反应
D.④、⑥可分别选用盐酸和硝酸
【变式4-2】从某含有,、的工业废液中回收铜并制备晶体的流程如下:
下列说法错误的是
A.试剂a是铁,试剂b是盐酸
B.操作Ⅰ、操作Ⅱ、操作Ⅲ所用仪器都相同
C.试剂c是氯气,反应的离子方程式为
D.用KSCN溶液可以检验滤液Z中是否含有
【变式4-3】和FeO的热化学循环可以利用太阳能,其转化关系如图所示。
已知:反应可用来检验。下列叙述错误的是
A.分析过程I和Ⅱ,是该循环过程中的催化剂
B.过程Ⅱ的化学方程式为
C.用盐酸、溶液检验和FeO混合物中的FeO
D.可利用该循环过程降低环境中的含量,减缓温室效应
题型05 氢氧化亚铁的制备
原理:Fe2++2OH-=Fe(OH)2↓
现象:白色沉淀
试剂:FeSO4或FeCl2、NaOH(均须采用煮沸并冷却的水配制溶液)
仪器:装有NaOH溶液的长试管,伸入液面下,以防生成的Fe(OH)2被氧化;
可以加少量煤油,以隔绝空气,能够长时间观察到白色沉淀。
【典例5】如图所示,为了制得较纯净的Fe(OH)2,以下操作错误的是
A.煮沸并冷却NaOH溶液B.煮沸并冷却FeSO4溶液
C.胶头滴管末端伸进液面下D.使用煤油进行液封
【变式5-1】实验室用和烧碱制备,为使生成的产物不被氧化,下列说法不正确的是
A.配制溶液和烧碱溶液所用的蒸馏水要煮沸
B.产生沉淀后,不能振荡试管
C.可在溶液的上面加一层植物油,以隔绝空气
D.向溶液中滴加烧碱溶液时,胶头滴管尖嘴不能伸入试管中
【变式5-2】下列各图示中能较长时间看到Fe(OH)2白色沉淀的是
A.①②④B.①②③C.①②D.②③④
【变式5-3】用下列实验装置进行相应实验(夹持装置略),不能达到实验目的的是
A.用装置甲制备Fe(OH)2白色沉淀
B.用装置乙蒸发NaCl溶液制备NaCl晶体
C.用装置丙检验溶液中是否含K+
D.用装置丁除去苯中溶解的Br2
题型06 铁与水蒸气反应
铁元素的存在:有游离态,如陨铁;有化合态,如氧化物、盐等。自然界的铁矿石主要有:黄铁矿(FeS2)、赤铁矿(Fe2O3)、磁铁矿(Fe3O4)等。
铁单质的物理性质:光亮的银白色金属,密度为 7.86 g·cm-3 ,熔点为1538 ℃。 纯铁的抗腐蚀能力很强,具有良好的延展性和导热性,导电性比铜、铝差,能被磁铁吸引。
铁的化学性质:
与酸反应
现象:生成无色气体,放热。
离子方程式: Fe + 2H+ =Fe2+ + H2↑
与某些盐溶液反应(置换)
离子方程式:Fe + Cu2+ =Fe2+ + Cu
与水蒸气反应
化学方程式:3Fe + 4H2O(g) Fe3O4 +4H2
【典例6】实验室中利用下图装置验证铁与水蒸气的反应。下列说法错误的是
A.酒精灯点燃的顺序:先①后②
B.用火柴点燃肥皂泡检验生成的
C.反应为
D.由此可知炽热的铁水注入模具之前,模具须干燥
【变式6-1】用如图所示装置研究铁粉与水蒸气的反应。观察到肥皂液中有气泡产生,点燃肥皂泡听到爆鸣声;实验结束后,试管中残留的黑色固体能被磁体吸引。下列分析正确的是(双选)
A.仅由“肥皂液中有气泡产生”,不能推断铁与水蒸气发生了反应
B.铁粉与水蒸气的反应需要加热,推断该反应为吸热反应
C.由“点燃肥皂泡听到爆鸣声”,推断有氢气生成
D.残留的黑色固体是
【变式6-2】下列图示实验中,操作规范的是
A.AB.BC.CD.D
【变式6-3】下列与铁及其化合物相关的实验不能达到目的的是
A.AB.BC.CD.D
\l "_Tc30563" 题型07 铁及其化合物的性质及转化关系
Fe3+、Fe2+的相互转化
【典例7】关于铁及其化合物的性质,下列说法不正确的是
A.可用足量的还原为
B.,说明氧化性:
C.足量的在氯气中燃烧生成
D.与足量酸性溶液反应,转移电子
【变式7-1】黔南州铁矿储量有限,为了减少资源浪费;加强废旧金属回收再利用,某工厂以废铁屑为原料制备铁红的工艺流程如图所示。下列说法不正确的是
A.铁红常作颜料,用于油漆、橡胶、塑料等的着色
B.“碱洗”的目的是除去废铁屑表面的油污
C.用KSCN溶液检验氧化后的溶液中是否含有Fe2+
D.氧化时可以选用H2O2溶液
【变式7-2】铁及其化合物在工业上有广泛的用途。回答下列问题:
(1)氯化铁的用途之一是五金蚀刻,蚀刻产品有眼镜架、钟表、电子元件和标牌等。
①实验室鉴别饱和溶液与胶体的方法是 。
②写出用氯化铁溶液蚀刻不锈钢时发生的主要反应的离子方程式: 。
③将1 溶液和1 溶液等体积混合(假设混合溶液的体积等于混合前两种溶液的体积之和),再向其中加入足量铁粉,经过足够长的时间后,铁粉有剩余(不考虑溶液体积的变化)。此时溶液中的物质的量浓度是 。
(2)高铁酸钠()是一种新型绿色净水剂,主要用于饮用水处理。工业上常用硫酸铁与次氯酸钠在碱性条件下反应制备高铁酸钠。
①写出工业制备高铁酸钠时发生反应的离子方程式: 。每生成1ml ,转移电子的数目是 。
②高铁酸钠可用作净水剂的原因是 。
③如果用单位质量的氧化剂所得到的电子数来表示消毒效率,那么,、、三种消毒杀菌剂的消毒效率最高的是 (填化学式)。
(3)草酸亚铁可作为制备电池正极材料磷酸铁锂的原料。称取3.60g ,用热重法对其进行热分解,得到剩余固体的质量随温度变化的曲线如图所示。
300℃时剩余固体只有一种且是铁的氧化物,则其化学式为 。
【变式7-3】铁及其化合物的相互转化
(1)亚铁盐
①氧化性和还原性
含有的溶液呈浅绿色,处于铁元素的中间价态,既有氧化性,又有还原性,其中以 为主,如遇等均表现 。
的酸性溶液与反应的离子方程式为 。
溶液与稀反应的离子方程式为 。
②易水解
是弱碱,含的盐(如硫酸亚铁)溶液呈酸性。配制硫酸亚铁溶液时常加少量 抑制的水解,加少量 防止被氧化。
(2)铁盐
①氧化性:含有的溶液呈棕黄色,处于铁元素的高价态,遇等均表现 。
可腐蚀印刷电路板上的铜箔,反应的离子方程式为 。
向溶液中滴入淀粉KI溶液,溶液变蓝,离子方程式为 。
②易水解:是很弱的碱,且溶度积很小,因而极易水解,只能存在于酸性较强的溶液中。
a.利用易水解的性质,实验室可将饱和溶液滴入沸水中制取氢氧化铁胶体,反应的化学方程式为。
b.利用易水解的性质,工业上常用调节pH的方法除去溶液中的铁离子。
c.利用易水解的性质,实验室配制氯化铁溶液,通常将氯化铁固体先溶于较浓的盐酸中,然后再稀释至所需浓度。
d.与 等水解呈碱性的离子不能大量共存。
题型08 铁及其化合物综合实验探究
【典例8】某种催化剂为铁的氧化物。化学兴趣小组在实验室对该催化剂中铁元素的价态进行探究:将适量稀硝酸加入少量样品中,加热溶解;取少量溶液,滴加KSCN溶液后出现红色。一位同学由此得出该催化剂中铁元素价态为+3的结论。
(1)请指出该结论是否合理并说明理由 。
(2)配制实验试剂:
实验需要配制0.01溶液250mL,需要选择的玻璃仪器有 (填编号);
(3)完成对铁元素价态的探究:
提供的实验仪器:烧杯、试管、玻璃棒、药匙、滴管、酒精灯、试管夹;
提供的实验试剂:3、3% 、6、0.01、NaOH稀溶液、0.1KI、20% KSCN、蒸馏水。
①提出合理假设
假设1:催化剂中铁元素的化合价全部为+2;
假设2:催化剂中铁元素全部为+3价;
假设3: 。
②设计实验证明你的假设
请在答题卡上按下表格式完成实验操作步骤、预期现象与结论。
。
(4)定量检测铁的氧化物组成
取0.99g铁的氧化物样品,用足量硝酸充分溶解后,加入过量氢氧化钠,过滤并洗涤沉淀,高温灼烧后冷却,称量得1.1g固体,实验数据证明假设 (填数字)正确。
【变式8-1】某化学兴趣小组为探究铁及其化合物的性质,进行了如下实验:
(1)实验一:铁与稀硫酸反应
取一定量的铁粉加入到稀硫酸中,观察到的现象是 ,反应的化学方程式为 。反应结束后,向溶液中滴加KSCN溶液,溶液 (填“变红”或“不变红”)。
(2)实验二:与的转化
①向实验一所得溶液中滴加双氧水,溶液颜色由浅绿色变为棕黄色,反应的离子方程式为 ,该反应中双氧水作 (填“氧化剂”或“还原剂”)。
②向上述棕黄色溶液中加入过量铁粉,溶液颜色又变为浅绿色,反应的离子方程式为 ,该反应中表现出 性。
(3)实验三:胶体的制备与性质
①向沸水中滴加饱和溶液,继续煮沸至溶液呈 色,停止加热,制得胶体。
②向胶体中逐滴加入稀硫酸,观察到的现象是 ,原因是 。
(4)实验四:检验某未知溶液中是否含有
可选用的试剂是 ,若含有,观察到的现象是 。
【变式8-2】兴趣小组的同学将生锈铁钉浸泡在过量10%稀盐酸中,观察到铁锈逐渐消失,同时伴有气泡产生,溶液呈黄色,一段时间后黄色变为浅绿色。
I.探究黄色溶液变为浅绿色的原因
(1)铁的锈蚀是铁跟 反应的结果。
(2)铁锈和盐酸反应的化学方程式为 。
(3)溶液由黄色变为浅绿色可能是氯化铁和某些物质反应,现进行3个实验进行探究(已知氢气不影响该反应),持续时间大约6个小时。
结合实验1~3
①实验1中x的数值是
②黄色溶液变为浅绿色的原因:在酸性环境中, (写出化学反应方程式)。
Ⅱ.应用和理解
(4)已知Fe2+在空气中易被氧化为Fe3+,你认为实验室保存氯化亚铁溶液时,可以加入 。
(5)印刷铜制电路板的“腐蚀液”为FeCl3溶液,反应原理为。现向溶液中加入一定量的铁粉和铜粉,充分反应后,发现有固体剩余。下列有关说法正确的是_____(填序号)。
A.向剩余的固体中加入稀盐酸,若无气体放出,说明反应后的溶液中没有Cu2+
B.向反应后的溶液中加入氢氧化钠可能有红褐色沉淀[Fe(OH)3]生成
C.若反应后的溶液呈蓝色,说明铁粉已经完全反应
D.剩余固体中如果有铁,一定也有铜
【变式8-3】乳酸亚铁晶体(CH3CH(OH)COO)2Fe·2H2O是一种很好的食品铁强化剂,可由乳酸钙与FeCl2反应制得,反应装置如下:
已知:潮湿的乳酸亚铁易被氧化
(1)仪器A的名称是 。
(2)装置B的主要作用是 。
(3)试写出制备乳酸亚铁晶体的化学方程式 。
(4)部分实验操作过程如下,其正确的操作顺序是: 。
检查气密性加入试剂将三颈烧瓶置于水浴中_____________________
a.关闭K1,盖上分液漏斗上口玻璃塞
b.关闭K3,打开K2
c.关闭K2,打开K3
d.打开分液漏斗上口玻璃塞,打开K1
(5)下列说法不正确的是_______。
A.本实验采用较大铁片而不是铁粉,主要原因是避免反应速率过快
B.关闭K1、K2、K3,往分液漏斗中加水,打开K1和分液漏斗活塞,若刚开始水能滴下,一段时间之后不再下滴,则虚线框内装置气密性良好
C.粗产品经洗涤后,再用小火烘干
D.控制反应温度,有利于得到大颗粒沉淀,吸附杂质的量少
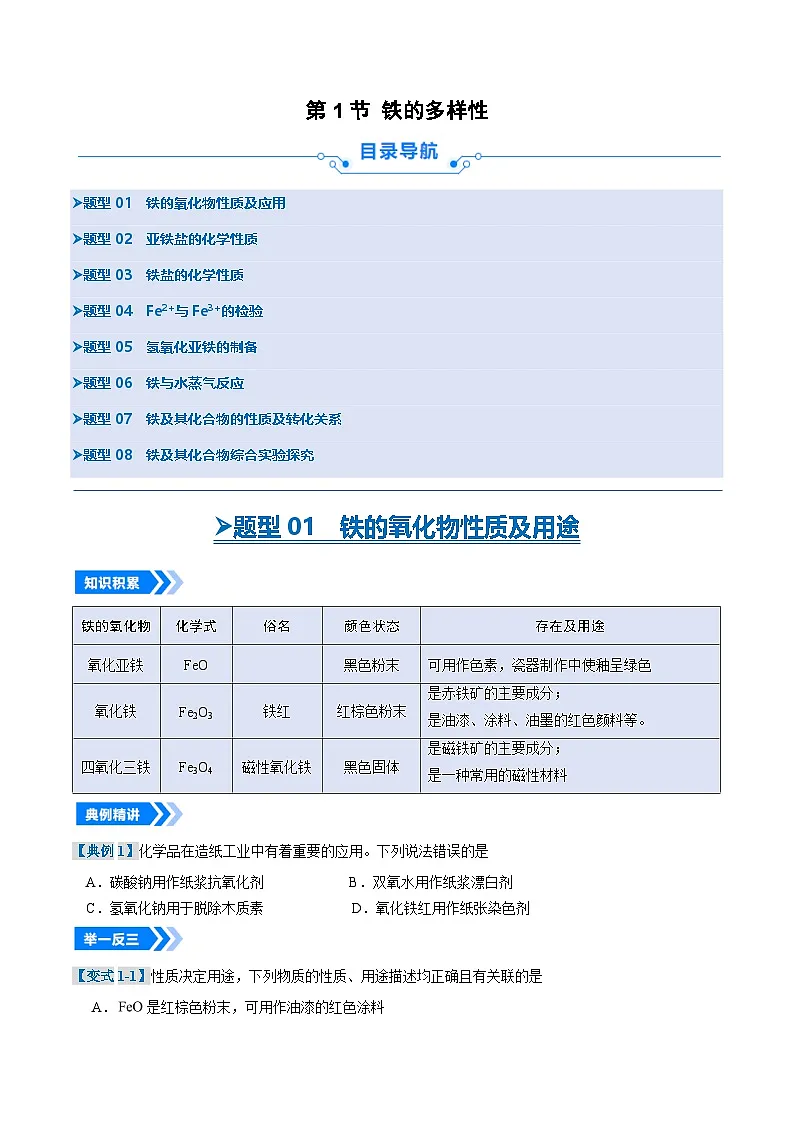
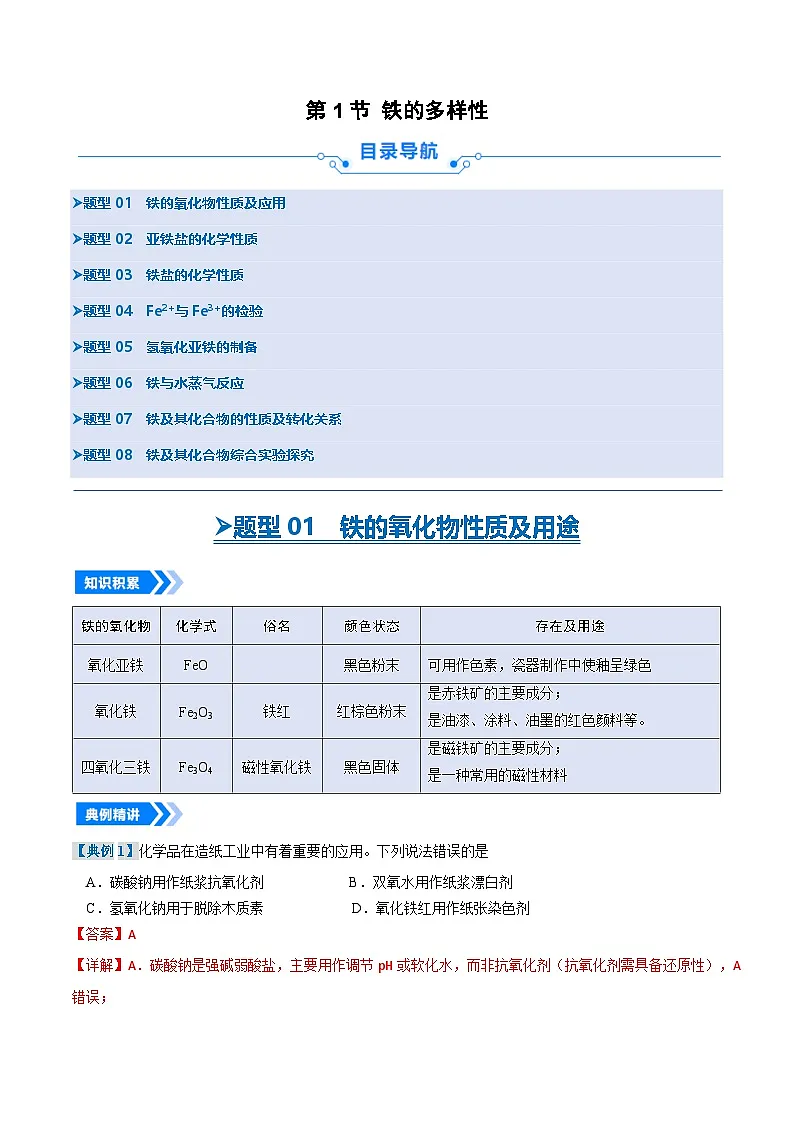
铁的氧化物
化学式
俗名
颜色状态
存在及用途
氧化亚铁
FeO
黑色粉末
可用作色素,瓷器制作中使釉呈绿色
氧化铁
Fe2O3
铁红
红棕色粉末
是赤铁矿的主要成分;
是油漆、涂料、油墨的红色颜料等。
四氧化三铁
Fe3O4
磁性氧化铁
黑色固体
是磁铁矿的主要成分;
是一种常用的磁性材料
A
B
C
D
物质
Fe2O3
Na2SiO3的水溶液
CuSO4
NaHCO3
俗名
铁红
水玻璃
胆矾
小苏打
用途
红色颜料
黏合剂
检验水蒸气
发酵粉
实验序号
验证性质
实验装置
试剂X
实验现象
①
能与盐溶液反应
_____溶液
产生白色沉淀
②
能与碱溶液反应
氨水
_____。
③
具有_____性
锌粒
锌粒表面变黑,溶液浅绿色褪去
④
具有还原性
KSCN溶液氯水
_____。
实验
①
②
③
操作和试剂
现象
溶液变红,大约10秒左右红色褪去,有气体生成(经检验为)。取褪色后溶液,滴加盐酸和溶液,产生白色沉淀。
溶液变红且不褪色,有气体生成(经检验为),经检验有丁达尔效应。
溶液变红且不褪色,滴加盐酸和溶液,无白色沉淀,经检验无丁达尔效应。
选项
物质
性质或应用
A
氯化铁溶液
可用于腐蚀铜电路板
B
石灰乳
利用石灰乳的还原性除去废气中的
C
小苏打
焙制糕点时用作膨松剂
D
食盐
运动后饮用适量食盐水可补充电解质
方法1
观察法:浅绿色
方法2
eq \a\vs4\al(样品溶液)eq \(―――――――→,\s\up7(滴加KSCN溶液))无现象eq \(―――――――→,\s\up11(滴加氯水),\s\d4(或双氧水))溶液变红色,证明含有Fe2+
方法3
eq \a\vs4\al(样品溶液)eq \(――――――――→,\s\up7(加入NaOH溶液))产生白色絮状沉淀,迅速变成灰绿色,最终变为红褐色,证明含有Fe2+
方法4
eq \a\vs4\al(样品溶液)eq \(―――――――――→,\s\up7(加入K3[Fe(CN)6]溶液))生成蓝色沉淀,证明含有Fe2+
方法1
观察法:棕黄色
方法2
eq \a\vs4\al(样品溶液)eq \(――――――――→,\s\up7(滴加KSCN溶液))溶液变红色,证明含有Fe3+
方法3
eq \a\vs4\al(样品溶液)eq \(―――――――→,\s\up7(加入NaOH溶液))产生红褐色沉淀,证明含有Fe3+
A.测量气体体积时,除去其中的HCl
B.单质铁与水蒸气的反应
C.吸收尾气
D.打开干燥器盖子
A.制备并观察沉淀
B.检验溶液中是否含有
C.检验未知溶液中是否存在
D.验证与的反应并收集气体
实验操作
实验现象
加少量铁粉振荡后,溶液变成浅绿色,
再加KSCN溶液,溶液颜色无变化
向上层清液中滴加新制氯水,
溶液变成红色
离子方程式
2Fe3++Fe=3Fe2+
2Fe2++Cl2=2Fe3++2Cl-
Fe3++3SCN-=Fe(SCN)3
实验结论
Fe3+遇到较强的还原剂时,会被还原成Fe2+
Fe2+在较强氧化剂的作用下会被氧化成Fe3+
实验操作
预期现象与结论
步骤1:取一定量3于试管中,加热煮沸数分钟以除去溶于其中的氧气。
步骤2:用药匙取少量样品于试管中,用滴管加入适量上述并加热,充分反应后得A溶液
固体溶解,溶液颜色有变化
步骤3:
……
序号
实验1
实验2
实验3
实验内容
现象
溶液颜色始终呈黄色
产生红褐色沉淀[Fe(OH)3沉淀]
溶液逐渐由黄色变浅绿色
相关试卷
这是一份化学铁的多样性综合训练题,文件包含第1节铁的多样性专项训练原卷版docx、第1节铁的多样性专项训练解析版docx等2份试卷配套教学资源,其中试卷共52页, 欢迎下载使用。
这是一份鲁科版 (2019)必修 第一册第1节 铁的多样性复习练习题,共19页。试卷主要包含了北宋沈括《梦溪笔谈》中记载,下列说法正确的是,博物馆修复出土铁器的过程如下,5 ml/L Na2SO3、0等内容,欢迎下载使用。
这是一份高中化学鲁科版 (2019)必修 第一册第1节 铁的多样性课后练习题,共13页。试卷主要包含了单选题,实验探究题等内容,欢迎下载使用。
相关试卷 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 






.png)
.png)



