



所属成套资源:沪教版(2024)化学九年级下册同步教学课件
九年级下册(2024)中和反应背景图ppt课件
展开 这是一份九年级下册(2024)中和反应背景图ppt课件,文件包含第1课时中和反应pptx、中和反应的应用mp4、导入视频mp4、酸碱中和反应实验mp4等4份课件配套教学资源,其中PPT共31页, 欢迎下载使用。
认识酸碱中和反应的概念及实质
能描述中和反应中物质和能量的变化
能举例说明酸碱中和反应在生产生活中的重要应用
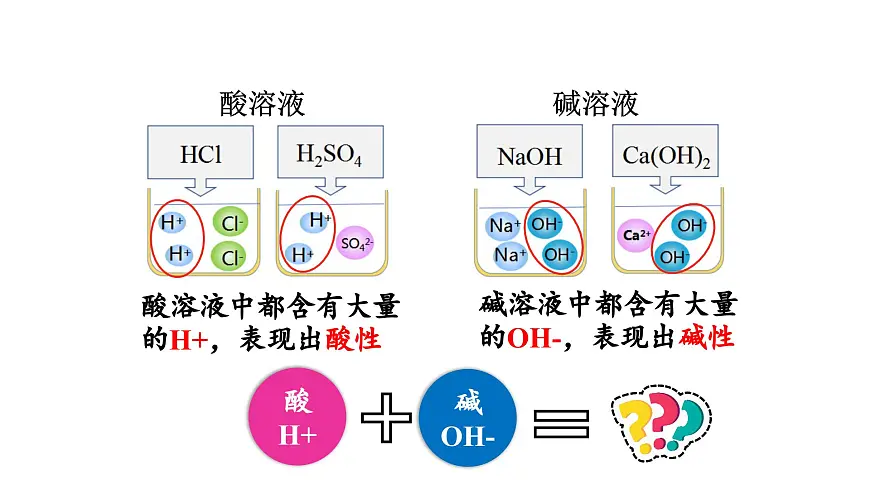
酸溶液中都含有大量的H+,表现出酸性
碱溶液中都含有大量的OH-,表现出碱性
观察浓盐酸和浓硫酸的状态、颜色,比较它们与同体积水的质量大小。打开瓶塞,观察发生的现象;闻一闻是否有气味。
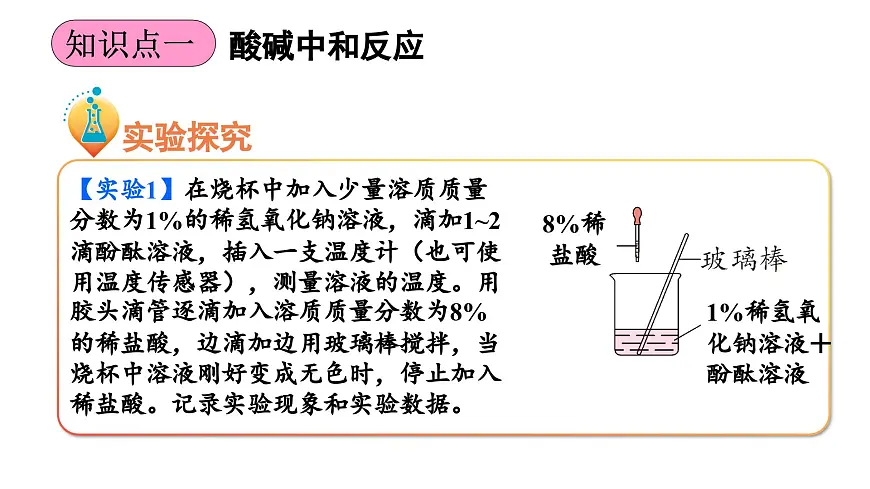
【实验1】在烧杯中加入少量溶质质量分数为1%的稀氢氧化钠溶液,滴加1~2滴酚酞溶液,插入一支温度计(也可使用温度传感器),测量溶液的温度。用胶头滴管逐滴加入溶质质量分数为8%的稀盐酸,边滴加边用玻璃棒搅拌,当烧杯中溶液刚好变成无色时,停止加入稀盐酸。记录实验现象和实验数据。
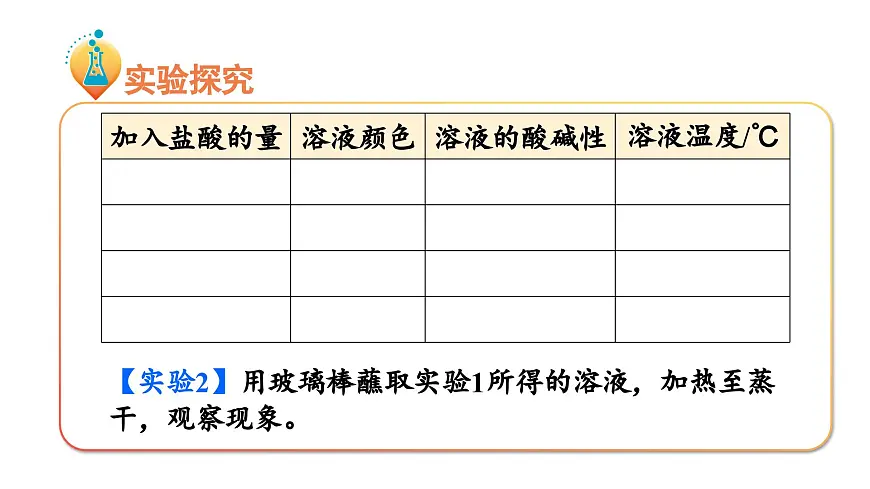
【实验2】用玻璃棒蘸取实验1所得的溶液,加热至蒸干,观察现象。
氢氧化钠溶液中滴入酚酞溶液后,溶液变成红色,当用胶头滴管逐滴加入盐酸时,红色逐渐变浅,最后变为无色,且溶液温度不断升高
玻璃棒上有白色固体析出
(2)为什么操作中必须逐滴滴入稀盐酸?
(1)酚酞在实验中起什么作用?
(3)玻璃棒搅拌的目的是什么?
指示作用。根据指示剂颜色变化,可判断反应的发生和反应的终点。
使溶液充分接触,反应迅速完全。
HCl + NaOH ══ NaCl + H2O
酸与碱作用生成盐和水的反应称为中和反应。
酸 + 碱 → 盐 + 水
例如:H2SO4 + 2NaOH ══ Na2SO4 + 2H2O
是复分解反应的一种,但不是基本反应类型
酸溶液中的H+和碱溶液中的OH-结合生成 H2O,即
H++ OH- ══ H2O
①中和反应是放热反应,这可以作为判断中和反应发生的依据之一。
②中和反应一定生成盐和水,但有盐和水生成的反应不一定是中和反应。如
CO2 + 2NaOH ══ Na2CO3 + H2O
Fe2O3 + 6HCl ══ 2FeCl3 + 3H2O
都有盐和水生成,但都不是中和反应
③中和反应不一定都无明显现象,有些中和反应伴有固体消失、溶液颜色改变及生成沉淀等现象。例如:
Fe(OH)3+3HCl══FeCl3+3H2O
红褐色固体溶解,生成黄色溶液
Cu(OH)2+H2SO4══ CuSO4+2H2O
Ba(OH)2+H2SO4══ BaSO4↓+2H2O
蓝色固体溶解,生成蓝色溶液
酸碱中和反应pH变化图像
NaCl、NaOH(酸不足、碱过量)
NaCl(酸碱刚好完全反应)
NaCl、HCl(酸过量)
NaCl、HCl(碱不足、酸过量)
NaCl、NaOH(碱过量)
例1 室温下,将NaOH溶液滴加到一定量的稀盐酸中,用数字化仪器测得溶液pH随加入NaOH溶液的质量的变化如图所示。下列叙述错误的是( )
A.反应的化学方程式为HCl + NaOH ══ NaCl + H2OB.a 点所示溶液的pH<7 ,呈酸性C.b 点表示HCl与NaOH恰好完全反应D.c 点所示溶液中的溶质是NaCl和HCl
1.科学研究中调控溶液pH
向酸性溶液中加碱中和溶液的酸性
使用稀盐酸、稀硫酸或醋酸中和溶液的碱性
在硫酸厂的酸性废水中加入熟石灰
加入酸溶液中和造纸厂、炼油厂的碱性废水
利用酸和碱反应并通过化学沉淀、分离提纯等方法回收废水
含碱的药物(如氢氧化铝)可中和过多的胃酸
使用食醋或洁厕灵(主要成分是盐酸)可清理下水道水垢(含氢氧化镁等难溶物)
Al(OH)3 + 3HCl ══ AlCl3 + 3H2O
Mg(OH)2+2HCl ══ MgCl2 +2H2O
例2 中和反应在生活生产中有广泛的应用,下列做法不是利用中和反应原理的是( )A.用醋酸清理烧水壶中的水垢B.用含碱性物质的药物治疗胃酸过多C.用盐酸除去铁锈D.用熟石灰处理工厂污水中的硫酸
1.下列反应中,属于中和反应的是( )。CO2+2NaOH══Na2CO3+H2OCuO + H2SO4 ══ CuSO4 +H2ONaOH + HNO3══ NaNO3+H2OZn+2HCl ══ ZnCl2+H2↑
【教材P64 练习与实践 第1题】
2.下列物质中,有一种物质与其他三种物质都能发生反应,它是( )。A. 铁 B.稀盐酸 C.碳酸钙 D.氢氧化钠
【教材P64 练习与实践 第2题】
3.下列反应,要借助酸碱指示剂才能判断两者是否发生反应的是( )。A.大理石和稀盐酸B.澄清石灰水和稀盐酸C.铁锈和稀硫酸D.镁和稀硫酸
【教材P65 练习与实践 第3题】
【教材P65 练习与实践 第4题】
4.下列应用与中和反应原理无关的是( )。A.服用含有Al(OH)3的药物,缓解胃酸过多症状B.用稀硫酸除去铁钉表面的铁锈C.用NaOH溶液洗涤石油产品中的残余硫酸D.用熟石灰改良酸性土壤
【教材P65 练习与实践 第5题】
5.同学们借助pH传感器研究氢氧化钠溶液与稀硫酸的中和反应,测得实验过程中溶液pH的变化如右图所示。下列分析正确的是( )。A.该实验是将氢氧化钠溶液滴入稀硫酸中B.P点时的溶液能与镁条发生反应C.M点对应溶液中的溶质是硫酸钠和硫酸D.N→P过程中生成的硫酸钠的量不断增加
【教材P65 练习与实践 第6题】
6.向氢氧化钠溶液中滴加稀盐酸没有明显现象。为了判断两者是否恰好完全反应,取少量反应后的溶液加入试管中,滴加几滴酚酞溶液,振荡后观察到酚酞溶液不变色。(1)根据上述现象,能否得出“两种物质恰好完全反应”的结论?(2)再利用pH试纸测定反应后溶液的pH,以确定两者是否恰好完全反应。请你选用其他试剂再设计一个实验,以验证氢氧化钠和盐酸是否恰好完全反应(写出选用的试剂、可能的现象和相应的结论)。
(1)不能。(2)向反应后的溶液中加入紫色石蕊溶液,若溶液呈紫色,说明氢氧化钠与盐酸恰好完全反应;若溶液呈红色,说明盐酸过量,氢氧化钠反应完全。
【教材P65 练习与实践 第7题】
7.室温下,在一定体积10%的氢氧化钠溶液中滴加10%的盐酸,测得反应中溶液温度的变化如下页表所示(△t为溶液实时温度与初始温度差)。试绘制溶液温度变化与加入盐酸体积之间的关系图,并根据曲线讨论溶液温度发生变化的原因。
溶液温度变化与加入盐酸体积之间的关系图如图所示:
温度发生变化的原因:开始加入盐酸时,盐酸与氢氧化钠溶液发生中和反应,放出热量,溶液温度升高;当加入的盐酸与氢氧化钠溶液恰好完全反应时,放出热量最多,溶液温度升高到最大;反应结束,继续加入盐酸,溶液温度逐渐降低。
相关课件
这是一份九年级下册(2024)中和反应背景图ppt课件,文件包含第1课时中和反应pptx、中和反应的应用mp4、导入视频mp4、酸碱中和反应实验mp4等4份课件配套教学资源,其中PPT共31页, 欢迎下载使用。
这是一份初中化学沪教版(2024)九年级下册(2024)第3节 中和反应授课ppt课件,共36页。PPT课件主要包含了第3节中和反应,第2节常见的酸和碱,常见的酸,酸的性质,常见的碱,碱的性质,化学性质腐蚀性,酸碱中和反应,复分解反应,有水生成等内容,欢迎下载使用。
这是一份沪教版(2024)九年级下册(2024)中和反应精品课件ppt,共29页。PPT课件主要包含了3中和反应的实质,氢氧化钠溶液,SO42-,2温度变化的图像等内容,欢迎下载使用。
相关课件 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 






.png)





