

湖南省岳阳市汨罗市第一中学2024-2025学年高三下学期4月月考 化学试题(含答案)
展开 这是一份湖南省岳阳市汨罗市第一中学2024-2025学年高三下学期4月月考 化学试题(含答案),共17页。试卷主要包含了单选题,解答题等内容,欢迎下载使用。
1.对于贵州这座城市的初印象,往往从地标建筑开始,不仅逼真地传递城市形象,也蕴藏着很多“黑科技”,下列说法正确的是
A.贵阳奥体中心场馆膜顶采用了耐腐蚀性能更好的PTFE(聚四氟乙烯)膜,该膜是一种合成有机高分子材料,也能使溴水褪色
B.石阡武陵山区崛起的新地标大顶山发电场,采用光伏发电技术绿色供电,这有利于实现低碳管理目标
C.黔南州平塘县的中国天眼FAST,制造大型抛物面天线的铝合金、玻璃钢均属于金属材料
D.铜仁大峡谷玻璃栈道依山势而造,是目前贵州最长的峡谷玻璃栈道,生产普通玻璃的主要原料是黏土和石灰石
2.已知反应,为阿伏加德罗常数的值。下列说法正确的是
A.的溶液中含有数目为
B.该反应中每生成转移电子数为
C.中含有孤电子对数目为
D.中含有的电子总数为
3.设为阿伏加德罗常数的值。下列说法正确的是
A.常温下,的溶液中,的数目为
B.常温常压下, 和混合气体中含有的氧原子数目为
C.电解精炼铜时,电路中每通过个电子时阳极溶解
D.重水比水多个质子
4.已知相关数据如下表:
下列离子方程式书写正确的是
A.与少量反应:
B.足量通入饱和溶液中:
C.氢氧化钙溶液与氢氟酸混合的离子方程式:
D.向溶液通入过量:
5.W、X、Y、Z是原子序数依次增大的短周期主族元素。已知W原子的最外层电子数是电子层数的2倍,X元素存在两种气态同素异形体,其中一种可吸收大气中的紫外线,Y原子最外层电子数等于电子层数,Z离子在同周期稳定的最简单阴离子中,半径最小。下列说法正确的是
A.简单离子半径:
B.可用于污水的杀菌消毒
C.X的氢化物常温常压下处于气态
D.的水溶液能导电,故为离子化合物
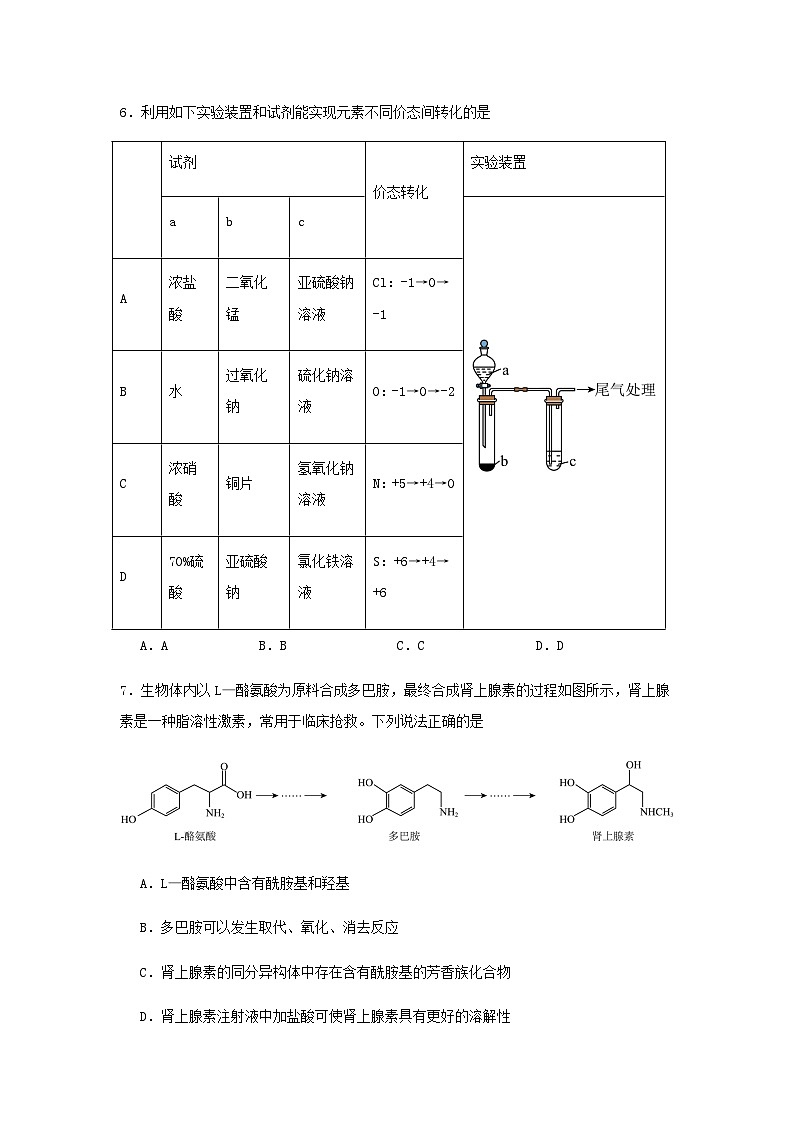
6.利用如下实验装置和试剂能实现元素不同价态间转化的是
A.AB.BC.CD.D
7.生物体内以L—酪氨酸为原料合成多巴胺,最终合成肾上腺素的过程如图所示,肾上腺素是一种脂溶性激素,常用于临床抢救。下列说法正确的是
A.L—酪氨酸中含有酰胺基和羟基
B.多巴胺可以发生取代、氧化、消去反应
C.肾上腺素的同分异构体中存在含有酰胺基的芳香族化合物
D.肾上腺素注射液中加盐酸可使肾上腺素具有更好的溶解性
8.室温下,用的二甲胺溶液(二甲胺在水中的电离与一水合氨相似)滴定盐酸溶液。溶液随加入二甲胺溶液体积变化曲线如图所示(忽略溶液混合时的体积变化)。下列说法正确的是
A.x=1,y=7
B.a、b两点的溶液中,不相等
C.本实验应该选择酚酞作指示剂
D.b点溶液中存在:
9.药物吲哚美辛结构如图所示,下列说法正确的是
A.分子式为
B.分子中所有碳原子均为杂化
C.分子中有种含氧官能团
D.该有机物能与过量反应,最多消耗
10.根据下列实验操作和现象,得出的相应结论正确的是
A.AB.BC.CD.D
11.将一定量的固体置于容积不变的密闭容器中,在一定温度下加入催化剂后发生下列反应:①;②。反应经过后达到了平衡状态,测得,,下列说法正确的是
A.的分解率为
B.此温度下反应①平衡常数
C.在上述平衡体系中再加入少量的,再次达到平衡后将减小
D.若温度不变,体积缩小为原来的一半,不变
12.盐酸羟胺()是一种常见的还原剂和显像剂,其结构和性质类似。工业上利用电化学方法制备盐酸羟胺时,Fe电极的反应机理如图所示(电解质溶液是HCl溶液):
下列说法错误的是
A.该催化循环中N元素的化合价没有发生变化
B.Fe起催化和导电作用
C.物质A为,物质B为
D.反应过程中有极性键的断裂和生成
13.甲胺()水溶液中存在以下平衡:。已知:25℃时,的,的。下列说法不正确的是
A.的
B.溶液中存在
C.25℃时, 溶液与 溶液相比,溶液的小
D. 溶液与相同浓度的溶液以任意比例混合,混合液中存在
14.常温下,、分别在溶液中达到沉淀溶解平衡后,改变溶液pH,金属阳离子浓度的变化如图所示。据图分析,下列判断正确的是
A.
B.e点对应的含的分散系很稳定
C.加适量固体可使溶液由a点变到b点
D.c、d两点代表的溶液中与乘积相等
15.25℃时,向 溶液中不断通入气体(忽略溶液体积变化),浴液中、与的关系如图所示。下列说法不正确的是
A.该温度下,的
B.点所表示的溶液中:
C.向原溶液中不断通入 气体:
D.的溶液中:
二、解答题(共55分)
16.(本题12分)锰是生产各种合金的重要元素,工业上以菱锰矿(主要成分为,还含有铁、钴、铜等的碳酸盐杂质)为原料生产金属锰的工艺流程如图所示:
已知:①25℃时,部分金属离子开始沉淀与完全沉淀的如表所示:
②25℃时,、、;
③“除铜”时,溶液中。
回答下列问题:
(1)菱锰矿经过富集、粉碎再进行酸浸,粉碎的目的是 ,“氧化”步骤发生反应的离子方程式为 。
(2)滤渣1的成分是 ,“除铜”时,当时,认为已完全沉淀,此时溶液中 (填“是”或“否”)开始沉淀。
(3)试剂是下列试剂中的一种,其中最合适的是 (填选项字母)。
A. B. C.
(4)“电解”时阴极上的电极反应式为 ,电解废液中有某种成分可循环应用,该成分是 (填化学式)。
17.(本题11分)铬酸铅[常温下,]又称铬黄,常用于染料或颜料,某同学在实验室以为原料制备,实验步骤如下:
步骤1:称取于的烧杯中,加入蒸馏水,搅拌使其溶解,逐滴滴入稍微过量的的溶液;
步骤2:向上述溶液中逐滴滴入溶液,溶液由绿色变为黄色。加热煮沸,将多余的赶尽,此时溶液变为亮黄色。再逐滴滴入的硝酸溶液,亮黄色溶液又变为橙红色,此时溶液的为4.6;
步骤3:在煮沸条件下逐滴滴入的溶液,加入第一滴后先搅拌再加第2滴,每滴加一滴可以看到有黄色沉淀产生,滴加到不再有新的黄色沉淀产生时停止加入溶液。继续煮沸,取下静置片刻,检验是否沉淀完全,过滤,产品用蒸馏水洗涤2~3次;
步骤4:将沉淀放入烘箱中干燥、称重、计算产率。
已知:元素铬()在溶液中主要以(蓝紫色)、(绿色)、(橙红色)、(黄色)等形式存在,为难溶于水的灰蓝色固体。回答下列问题:
(1)实验室在配制溶液时,下列仪器一定不需要的是___________(填字母)。
A.B.C.D.
(2)步骤1中加入稍微过量的的溶液过程中的现象是 ,溶液不能过量太多,其原因是 。
(3)步骤2溶液中逐滴滴入溶液,溶液由绿色变为黄色。发生反应的离子方程式为 。
(4)步骤2用硝酸调节,存在如下平衡:。已知随的变化如图所示。
①由图可知,溶液酸性增大,的平衡转化率 (填“增大”“减小”或“不变”)。
②升高温度,溶液中的平衡转化率减小,则该反应的 (填“>”或“
相关试卷 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 





