





初中化学人教版(2024)九年级下册(2024)溶质的质量分数图文ppt课件
展开 这是一份初中化学人教版(2024)九年级下册(2024)溶质的质量分数图文ppt课件,共28页。PPT课件主要包含了核心素养目标,课前导入,溶质的质量分数,实验现象及结论,溶质质量分数,溶质质量分数的计算,课堂小结,课堂练习等内容,欢迎下载使用。
科学态度与责任:通过溶质质量分数计算,养成严谨、细致的实验操作态度和科学思维习惯。化学观念:建立 “溶质质量分数是衡量溶液组成的重要定量指标” 的化学观念,理解溶液稀释前后溶质质量不变等相关化学原理。科学思维:借助溶液浓稀判断、溶质质量分数计算,培养逻辑推理、数据分析和实验操作能力,提升将化学知识应用于实际的思维素养
重点溶质质量分数的概念及计算公式;有关溶质质量分数的基本计算(包括配制溶液、溶液稀释等);难点理解溶质质量分数概念的内涵及应用;灵活运用溶质质量分数公式解决实际问题,如溶液稀释、浓缩等计算;
生活中我们会用到各种溶液,比如给农作物喷洒的农药溶液、医院里给病人输液的药水。如果农药溶液太浓,会伤害农作物;太稀,又起不到杀虫灭菌的效果。输液药水的浓度不合适,甚至会危及生命。那么,如何准确表示溶液的浓稀程度呢?今天,我们就一起来学习 “溶质的质量分数”,掌握定量描述溶液组成的方法,为生活和生产中的溶液使用保驾护航!
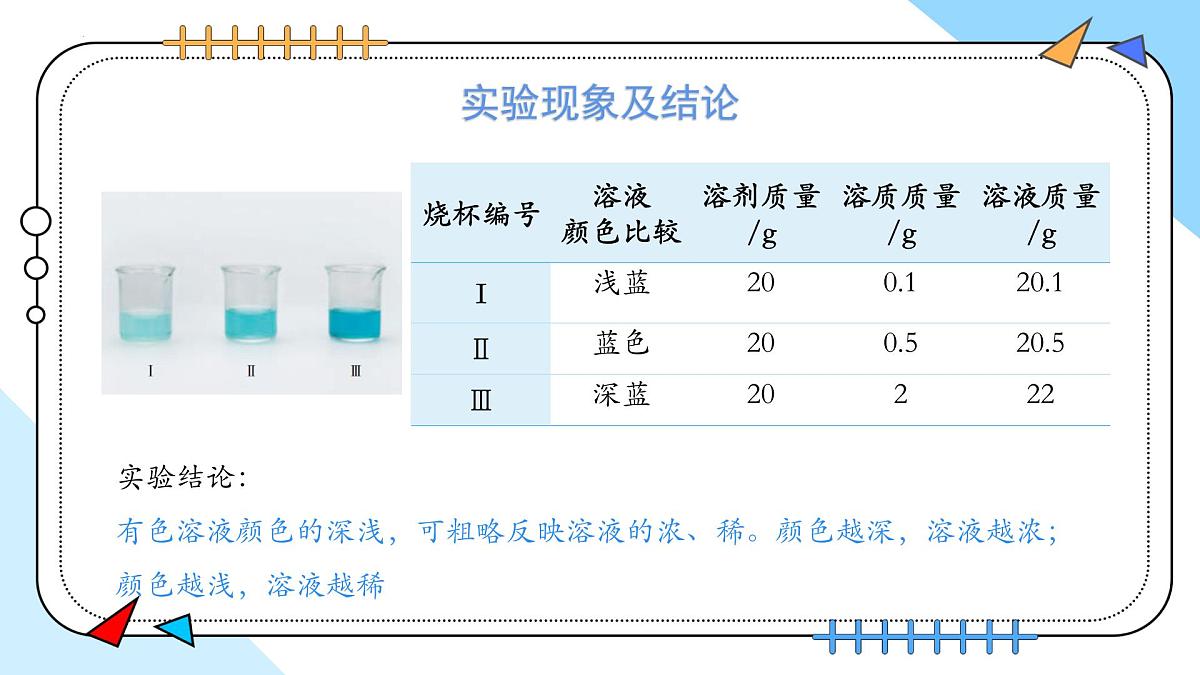
溶液浓度的粗略表示——溶液的稀、浓
实验结论:有色溶液颜色的深浅,可粗略反映溶液的浓、稀。颜色越深,溶液越浓;颜色越浅,溶液越稀
为什么要使用溶质质量分数
一般情况下,对于有色溶液来说,根据颜色的深浅可以判断溶液的浓稀程度。这种方法比较粗略,不能准确地表明一定量的溶液里究竟含有多少溶质。在实际应用中,常常要准确知道一定量的溶液里所含溶质的量,即浓度。例如:在施用农药时,如果药液过浓,会毒害农作物;如果药液过稀,则不能有效地杀虫灭菌。因此,我们需要准确地知道一定量的药液里所含农药有效成分的量。
对溶液中溶质的质量分数的理解
(1)溶质的质量分数是溶液浓度的一种表示方法,适用于任何溶液。(2)一定温度下,某一溶质的不同质量分数的溶液中,饱和溶液的溶质质量分数最大且固定。向饱和溶液中添加原溶质,原溶质不会溶解,故溶质质量分数不会改变。(3)溶液具有均一性,故溶液中各部分溶质的质量分数相等;溶液具有稳定性,一种溶液长期放置,只要外界条件不变,其溶质的质量分数不变。
配制两种不同质量分数的氯化钠溶液
溶质的质量分数与溶质质量的相对大小有关。对于不饱和溶液,溶质质量相对越多,即溶质质量分数越大。
不饱和溶液中的数量关系
有关溶质的质量分数、溶质质量和溶剂质量的基本计算
(2)饱和溶液的溶质质量分数的计算
【例题 1】在农业生产中,可利用质量分数为16%的氯化钠溶液选种。现要配制150 kg这种溶液,需要氯化钠和水的质量各是多少
溶液稀释(无晶体析出)的计算
m ×a%=[m +m(水)]×b%
m×a% +m(稀)×c%(稀)=[m+m(稀)]×b%
溶液增浓(无晶体析出)的计算
m×a% +m(浓)×c%(浓)=[m +m(浓)]×b%
m ×a% =[m -m(水)]×b%
m×a%+m(质)=[m+m(质)]×b%
m×(1-a%)=[m+m(质)]×(1-b%)
【例题2】化学实验室有质量分数为98%的浓硫酸,现需要用较稀的硫酸进行实验。要把50 g上述浓硫酸稀释为质量分数为20%的硫酸,需要水的质量是多少?
体积分数 除了质量分数,人们有时也用体积分数来表示浓度。例如,用作消毒剂的医用酒精中乙醇的体积分数为 75%,就是指每100体积的医用酒精中含 75 体积的乙醇。
1.将50℃的硝酸钠饱和溶液降温到20℃,有晶体析出(晶体中不含水)。下列有关量中没有发生改变的是( )A.溶液的质量B.溶液中溶质的质量C.溶液中溶剂的质量D.溶液中溶质的质量分数
2.下列关于100g溶质质量分数为10%的氯化钠溶液的理解,正确的是( )A.100g氯化钠溶液中溶解了10g氯化钠B.溶液中氯化钠与水的质量比为1:10C.溶液中氯化钠与溶液的质量比为1:9D.将10g氯化钠溶解于100g水中配成的溶液
3.某温度时,将20g KNO3溶解在100g水中恰好饱和。关于该饱和溶液的叙述正确的是( )A.m(溶质)∶m(溶剂)=20∶120B.溶质的质量分数为20%C.升温后,溶质的质量分数增大D.降温后,溶质质量分数减小
4.有一瓶t℃某溶质的饱和溶液中,加入一些该溶质的晶体,则( )A.晶体质量减少B.溶质的质量分数增大C.晶体质量不变D.溶质的溶解度变化
相关课件 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 

.png)




