




湖北省华中师范大学第一附属中学2024届高三上学期第一次调研测试化学试题(Word版附解析)
展开
这是一份湖北省华中师范大学第一附属中学2024届高三上学期第一次调研测试化学试题(Word版附解析),文件包含湖北省华中师范大学第一附属中学2024届高三上学期第一次调研测试化学试卷原卷版docx、湖北省华中师范大学第一附属中学2024届高三上学期第一次调研测试化学试卷解析版docx等2份试卷配套教学资源,其中试卷共31页, 欢迎下载使用。
请考生注意:
1. 请用2B 铅笔将选择题答案涂填在答题纸相应位置上,请用0.5毫米及以上黑色字迹的钢笔或签字笔将主观题的答案写在答题纸相应的答题区内。写在试题卷、草稿纸上均无效。
2. 答题前,认真阅读答题纸上的《注意事项》,按规定答题。
一、选择题(每题只有一个选项符合题意)
1. 下列诗句、谚语或与化学现象有关,说法不正确的是
A. “水乳交融,火上浇油”前者包含物理变化,而后者包含化学变化
B. “落汤螃蟹着红袍”肯定发生了化学变化
C. “滴水石穿、绳锯木断”不包含化学变化
D. “看似风平浪静,实则暗流涌动”形象地描述了溶解平衡的状态
2. 下列说法正确的是
A 离子晶体中可能含有共价键,但不一定含有金属元素
B. 分子晶体中一定含有共价键
C. 非极性分子中一定存在非极性键
D. 对于组成结构相似的分子晶体,一定是相对分子质量越大,熔沸点越高
3. 已知X、Y、Z、W为原子序数依次增大的短周期元素,Y、W为同一周期元素且W原子的最外层电子数等于Y原子的核外电子总数,其形成的一种化合物结构如图所示,下列叙述正确的是
A. 原子半径:W>Z>Y>X
B. 该化合物中各元素的原子最外层均满足8电子结构
C. X与Y形成的二元化合物常温下一定为气态
D. X、Y、Z、W可形成原子个数比8:1:2:3的化合物
4. pH=0的某X溶液中,除H+外,还可能存在Al3+、Fe2+、NH4+、Ba2+、Cl-、CO32-、SO42-、NO3-中的若干种,现取适量X溶液进行如下一系列实验:
下列有关判断不正确是
A. 生成气体A的离子方程式为:3Fe2++4H++NO3-=3Fe3++NO↑+2H2O
B. 生成沉淀H 离子方程式为:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-
C. 溶液X中一定没有的离子仅为:CO32-、Ba2+
D. 溶液X中一定含有离子是: H+、Fe2+、SO42-、NH4+、 Al3+
5. 化学与生产、生活息息相关。下列说法正确的是( )
A. 可用钢瓶储存液氯或浓硫酸
B. 二氧化碳气体可用作镁燃烧的灭火剂
C. 鸡蛋清溶液中加入CuSO4溶液,有沉淀析出,该性质可用于蛋白质的分离与提纯
D. 炒菜时加碘食盐要在菜准备出锅时添加,是为了防止食盐中的碘受热升华
6. 下列解释事实或实验现象的化学用语正确的是
A. 硫酸酸化的KI淀粉溶液久置后变蓝:4I-+O2+4H+=2I2+2H2O
B. 铁和稀硝酸反应制得浅绿色溶液:Fe+4H++NO=Fe3++NO↑+2H2O
C. 水垢上滴入CH3COOH溶液有气泡产生:CaCO3+2H+=Ca2++CO2↑+H2O
D. SO2通入漂白粉溶液中产生白色浑浊:SO2+Ca2++2ClO-+H2O=CaSO3↓+2HClO
7. 异丙烯苯和异丙苯是重要的化工原料,二者存在如图转化关系:
下列说法正确的是
A. 异丙烯苯分子中所有碳原子一定共平面
B. 异丙烯苯和乙苯是同系物
C. 异丙苯与足量氢气完全加成所得产物的一氯代物有6种
D. 0.05ml异丙苯完全燃烧消耗氧气13.44L
8. 下列说法中正确的是( )
A. 气体单质中,一定有σ键,可能有π键
B. PCl3分子是非极性分子
C. 邻羟基苯甲醛的熔、沸点比对羟基苯甲醛的熔、沸点高
D. ClO4-的VSEPR模型与离子的空间立体构型一致
9. 已知对二烯苯的结构简式如图所示 ,下列说法正确的是( )
A. 对二烯苯苯环上的一氯取代物有2种
B. 对二烯苯与苯乙烯互为同系物
C. 对二烯苯分子中所有碳原子一定处于同一平面
D. 1ml对二烯苯最多可与5ml氢气发生加成反应
10. 氮及其化合物的性质是了解工农业生产的重要基础。NA为阿伏加 德罗常数的值,下列有关说法错误的是
A. 22.4 L(标准状况)15NH3含有的质子数为10 NA
B. 密闭容器中,2 ml NO与1 ml O2充分反应,产物的分子数为2 NA
C. 13.8 g NO2与足量水反应,转移的电子数为0.2 NA
D. 常温下,1 L 0.1 ml·L1 NH4NO3溶液中含有的氮原子数为0.2 NA
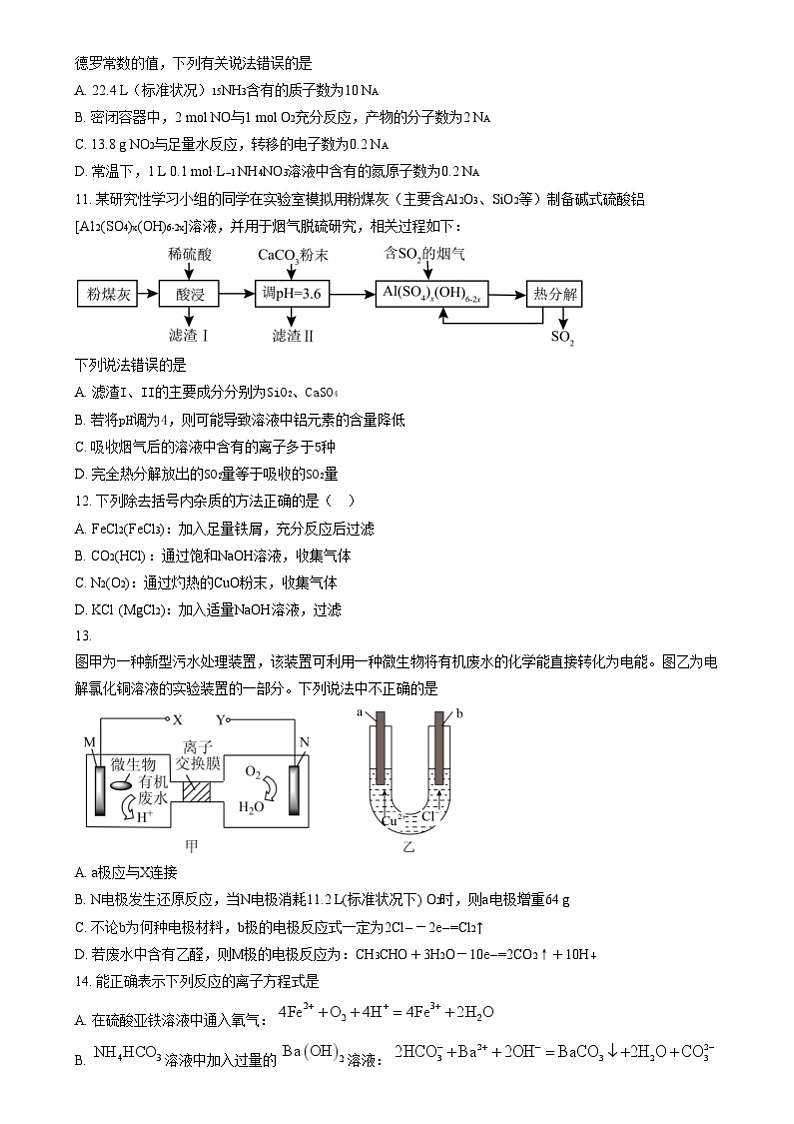
11. 某研究性学习小组的同学在实验室模拟用粉煤灰(主要含Al2O3、SiO2等)制备碱式硫酸铝 [A12(SO4)x(OH)6-2x]溶液,并用于烟气脱硫研究,相关过程如下:
下列说法错误的是
A. 滤渣I、II的主要成分分别为SiO2、CaSO4
B. 若将pH调为4,则可能导致溶液中铝元素的含量降低
C. 吸收烟气后的溶液中含有的离子多于5种
D. 完全热分解放出的SO2量等于吸收的SO2量
12. 下列除去括号内杂质的方法正确的是( )
A. FeCl2(FeCl3):加入足量铁屑,充分反应后过滤
B. CO2(HCl):通过饱和NaOH溶液,收集气体
C. N2(O2):通过灼热的CuO粉末,收集气体
D. KCl (MgCl2):加入适量NaOH溶液,过滤
13. 图甲为一种新型污水处理装置,该装置可利用一种微生物将有机废水的化学能直接转化为电能。图乙为电解氯化铜溶液的实验装置的一部分。下列说法中不正确的是
A. a极应与X连接
B. N电极发生还原反应,当N电极消耗11.2 L(标准状况下) O2时,则a电极增重64 g
C. 不论b为何种电极材料,b极的电极反应式一定为2Cl--2e-=Cl2↑
D. 若废水中含有乙醛,则M极的电极反应为:CH3CHO+3H2O-10e-=2CO2↑+10H+
14. 能正确表示下列反应的离子方程式是
A. 在硫酸亚铁溶液中通入氧气:
B. 溶液中加入过量的 溶液:
C. 氢氧化亚铁溶于稀硝酸中:
D. 澄清石灰水与过量小苏打溶液混合:
15. 下列说法正确的是( )
A. 氢键、分子间作用力、离子键、共价键都是微粒间的作用力。其中分子间作用力只影响物质的熔沸点而不影响物质的溶解性。
B. 石墨烯是一种从石墨材料中用“撕裂”方法剥离出的单层碳原子平面材料,用这种方法可以从C60、金刚石等中获得“只有一层碳原子厚的碳薄片”也必将成为研究方向。
C. 由“同温度下等浓度的Na2CO3溶液比Na2SO3溶液的pH大”,可推知C比S的非金属性弱。
D. H、S、O三种元素组成的物质的水溶液与Na、S、O三种元素组成的物质的水溶液混合可能会观察到浑浊现象。
16. 我国自主研发的对二甲苯绿色合成项目取得新进展,其合成过程如图所示。
下列说法不正确的是
A. 异戊二烯所有碳原子可能共平面
B. 可用溴水鉴别M和对二甲苯
C. 对二甲苯的一氯代物有2种
D. M的某种同分异构体含有苯环且能与钠反应放出氢气
二、非选择题(本题包括5小题)
17. 化合物 I( )是治疗心脏病的一种重要药物,可由简单有机物 A、B 和萘( )合成,路线如下:
(1)C的结构简式为_________,E的化学名称_______。
(2)由萘生成C、B生成E的反应类型分别为_________、_________ 。
(3)I中含氧官能团的名称为_______。
(4)D可使溴水褪色,由D生成G的反应实现了原子利用率100%,则该反应的化学方程式为_______________。
(5)同位素标记可用来分析有机反应中的断键情况,若用超重氢(T)标记的
G( )与F反应,所得H的结构简式为 则反应中G( )断裂的化学键为 _______(填编号)
(6)Y为H的同分异构体,满足以下条件的共有______种,请写出其中任意一种的结构简式_________。
①含有萘环,且环上只有一个取代基。
②可发生水解反应,但不能发生银镜反应。
18. 白藜芦醇(结构简式:)属二苯乙烯类多酚化合物,具有抗氧化、抗癌和预防心血管疾病的作用。某课题组提出了如下合成路线:
根据以上信息回答下列问题:
(1)白藜芦醇的分子式是_________
(2)C→D的反应类型是:__________;E→F的反应类型是______。
(3)化合物A不与FeCl3溶液发生显色反应,能与NaHCO3溶液反应放出CO2,推测其核磁共振谱(1H-NMR)中显示不同化学环境的氢原子个数比为_______(从小到大)。
(4)写出A→B反应的化学方程式:_____________;
(5)写出结构简式;D________、E___________;
(6)化合物符合下列条件的所有同分异构体共________种,
①能发生银镜反应;②含苯环且苯环上只有两种不同化学环境的氢原子。
写出其中不与碱反应的同分异构体的结构简式:_______。
19. Fe(OH)3广泛应用于医药制剂、颜料制造等领域,其制备步骤及装置如下:在三颈烧瓶中加入16.7gFeSO4·7H2O和40.0ml蒸馏水。边搅拌边缓慢加入3.0mL浓H2SO4,再加入2.0gNaClO3固体。水浴加热至80℃,搅拌一段时间后,加入NaOH溶液,充分反应。经过滤、洗涤、干燥得产品。
(1)NaClO3氧化FeSO4·7H2O的离子方程式为_____________。
(2)加入浓硫酸的作用为_________(填标号)。
a.提供酸性环境,增强NaClO3氧化性 b.脱去FeSO4·7H2O的结晶水
c.抑制Fe3+水解 d.作为氧化剂
(3)检验Fe2+已经完全被氧化需使用的试剂是_________。
(4)研究相同时间内温度与NaClO3用量对Fe2+氧化效果的影响,设计对比实验如下表
①m=______;n=______。
②若c>87.8>a,则a、b、c的大小关系为___________。
(5)加入NaOH溶液制备Fe(OH)3的过程中,若降低水浴温度,Fe(OH)3的产率下降,其原因是___
(6)判断Fe(OH)3沉淀洗涤干净的实验操作为_________________;
(7)设计实验证明制得的产品含FeOOH(假设不含其他杂质)。___________。
20. 碱式碳酸钴[ Cx(OH)y(CO3)z ]常用作电子材料,磁性材料的添加剂,受热时可分解生成三种氧化物。为了确定其组成,某化学兴趣小组同学设计了如图所示装置进行实验。
(1)请完成下列实验步骤:
①称取3.65g样品置于硬质玻璃管内,称量乙、丙装置的质量;
②按如图所示装置组装好仪器,并检验装置气密性;
③加热甲中玻璃管,当乙装置中____________(填实验现象),停止加热;
④打开活塞a,缓缓通入空气数分钟后,称量乙、丙装置的质量;
⑤计算。
(2)步骤④中缓缓通入空气数分钟的目的是_____________________
(3)某同学认为上述实验装置中存在一个明显缺陷,为解决这一问题,可选用下列装置中的______(填字母)连接在_________(填装置连接位置)。
编号
T/℃
FeSO4·7H2O/g
NaClO3/g
氧化效果/%
i
70
25
1.6
a
ii
70
25
m
b
iii
80
n
2.0
c
iv
80
25
1.6
87.8
(4)若按正确装置进行实验,测得如下数据:
则该碱式碳酸钴的化学式为_________________。
(5)含有C(AlO2)2的玻璃常用作实验室观察钾元素的焰色反应,该玻璃的颜色为___________。
(6)CCl2·6H2O常用作多彩水泥的添加剂,以含钴废料(含少量Fe、Al等杂质)制取CCl2·6H2O的一种工艺如下:
已知:
①净除杂质时,加入H2O2 发生反应的离子方程式为______________。
②加入CCO3调PH为5.2~7.6,则操作Ⅰ获得的滤渣成分为_____________。
③加盐酸调整PH为2~3的目的为__________________________________。
乙装置的质量/g
丙装置的质量/g
加热前
80.00
62.00
加热后
80.36
6288
沉淀物
Fe(OH)3
Fe(OH)2
CO(OH)2
Al(OH)2
开始沉淀(PH)
2.3
7.5
7.6
3.4
完全沉淀(PH)
4.1
9.7
9.2
5.2
④操作Ⅱ过程为___________(填操作名称)、过滤。
21. 氯吡格雷是一种用于抑制血小板聚集的药物,合成线路如图:
(1)C→D的反应类型____,X的化学式是(C6H7BrS),X的结构简式___。
(2)写出C聚合成高分子化合物的结构简式___。
(3)E合成氯吡格雷的反应中,另一个有机产物的结构简式___。
(4)物质A的同系物G,比A多一个碳原子且苯环上一溴代物只有两种的可能结构有___种。
(5)已知①同一个碳原子上连有两个羟基是不稳定的,极易脱水转变为,②中氯原子在水溶液中不水解,写出2-氯甲苯()经两步反应合成A的化学方程式。____,合成A时产生的有机副产物可能是____。
相关试卷
这是一份湖北省武汉市华中师范大学第一附属中学2024-2025学年高三上学期第一次测评(一模)化学试题(Word版附解析),文件包含湖北省武汉市华中师范大学第一附属中学2024-2025学年高三上学期第一次测评一模+化学试题+评分参考docx、湖北省武汉市华中师范大学第一附属中学2024-2025学年高三上学期第一次测评一模+化学试题+docx等2份试卷配套教学资源,其中试卷共16页, 欢迎下载使用。
这是一份湖北省华中师范大学第一附属中学2024-2025学年高三上学期期中检测化学试卷(Word版附答案),共11页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
这是一份湖北省武汉市华中师范大学第一附属中学2024-2025学年高三上学期10月月考化学试题(Word版附解析),文件包含湖北省武汉市华中师范大学第一附属中学2024-2025学年高三上学期10月阶段性检查化学试卷Word版含解析docx、湖北省武汉市华中师范大学第一附属中学2024-2025学年高三上学期10月阶段性检查化学试卷Word版无答案docx等2份试卷配套教学资源,其中试卷共33页, 欢迎下载使用。








