



所属成套资源:2025年高考化学 热点 重点 难点 专练(西北四省专用)(陕西、山西、宁夏、青海)
热点题型05 实验方案设计与评价-2025年高考化学 热点 重点 难点 专练(西北四省专用)
展开
这是一份热点题型05 实验方案设计与评价-2025年高考化学 热点 重点 难点 专练(西北四省专用),文件包含热点题型05实验方案设计与评价-2025年高考化学热点重点难点专练西北四省专用原卷版docx、热点题型05实验方案设计与评价-2025年高考化学热点重点难点专练西北四省专用解析版docx等2份试卷配套教学资源,其中试卷共44页, 欢迎下载使用。
探究性实验以其创新、灵活的特点成为每年高考的热点题型,试题将元素化合物知识与化学实验知识巧妙地融合在一起,增加了题目的新颖度和难度,能充分考查学生的发散思维能力和分析问题的能力。实验往往通过对物质化学性质的实验探究、反应产物成分的实验探究、化学反应原理的实验探究,揭示反应原理、解释产生某些现象的原因等。
1.性质、原理探究类实验的设计角度分析
(1)酸性强弱比较:可通过强酸制弱酸、对应盐溶液的碱性、同浓度溶液导电能力或pH等方法来比较
(2)金属性强弱比较:可通过与水或酸反应置换氢的能力、最高价氧化物对应水化物的碱性、置换反应、原电池的正负极、电解池中阴极阳离子的放电顺序等方法来比较
(3)非金属性强弱比较:可通过最高价氧化物对应水化物的酸性、气态氢化物的稳定性、与H2化合的难易程度、相互之间的置换、对应阴离子的还原性等方法来比较
(4)弱酸酸式盐的电离程度与水解程度比较:可通过测定溶液的酸碱性的方法来比较
(5)Ksp的大小比较
(6)一元酸、二元酸判断:可用NaOH溶液进行中和滴定测定消耗V(NaOH)来确定
(7)羟基的数目判断:可通过取一定量试剂与足量Na反应测定放出氢气的量来确定
(8)羧基的数目判断:可通过取一定量试剂与足量NaHCO3反应测定放出CO2的量来确定
2.探究物质成分或反应产物的设计角度分析
通过化学反应原理猜测可能生成哪些物质,对这些物质一一的检验来推测出究竟含有哪些物质
(1)钢铁发生电化学腐蚀的规律探究:可以通过控制钢铁是否与空气接触、所接触的电解质溶液的酸碱度、钢铁在腐蚀过程中体系内的气压变化等设计实验,找出规律
(2)常见物质的热分解反应规律
= 1 \* GB3 \* MERGEFORMAT ①难溶性碳酸盐氧化物+CO2↑
= 2 \* GB3 \* MERGEFORMAT ②碳酸的酸式盐碳酸的正盐+CO2↑+H2O
= 3 \* GB3 \* MERGEFORMAT ③铵盐NH3+相应的酸(或酸性氧化物+H2O)(NH4NO3除外)
= 4 \* GB3 \* MERGEFORMAT ④草酸晶体CO2↑+CO↑+H2O
= 5 \* GB3 \* MERGEFORMAT ⑤硝酸盐的分解规律
3.根据特殊现象进行成分确定
根据物质性质,使被检验物质与加入的试剂作用,转变为某种已知物质,或产生某种特殊现象,从而确定该物质的存在(物质性质也是帮助检验的重要依据)。常见的特殊现象有:
(建议用时:40分钟)
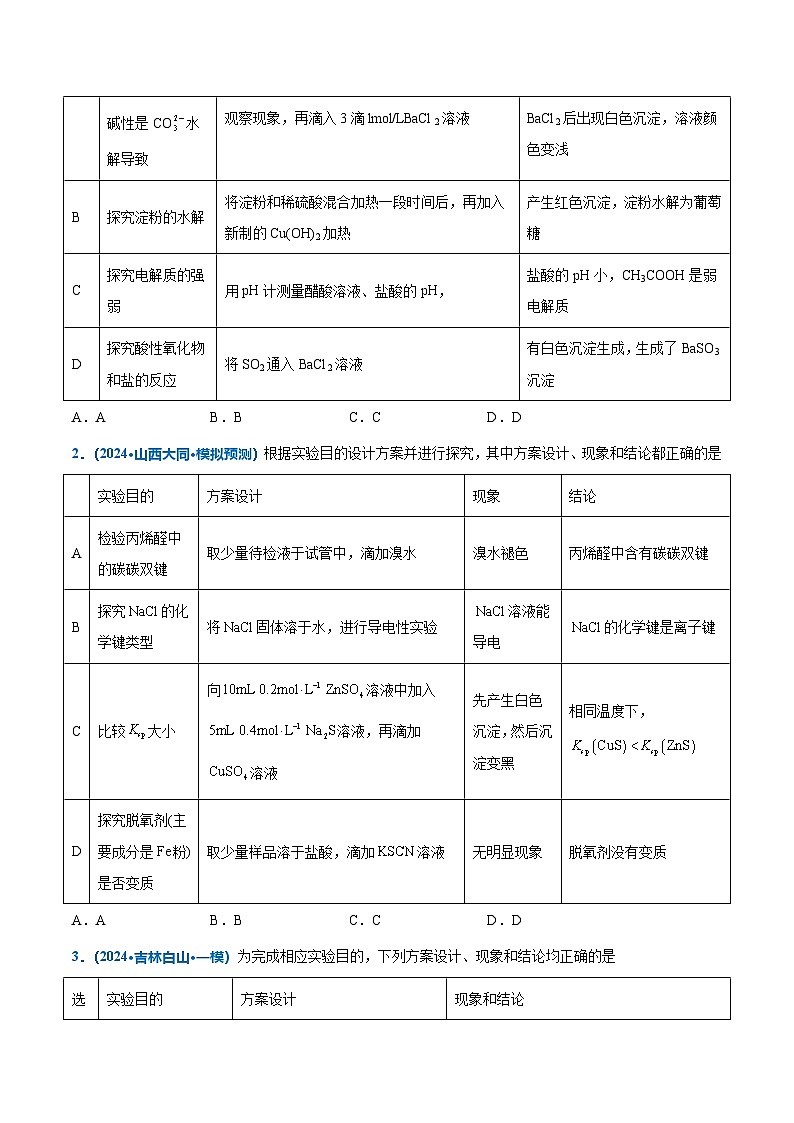
1.(2024·宁夏银川·一模)下列方案设计、现象和结论均正确的是
A.AB.BC.CD.D
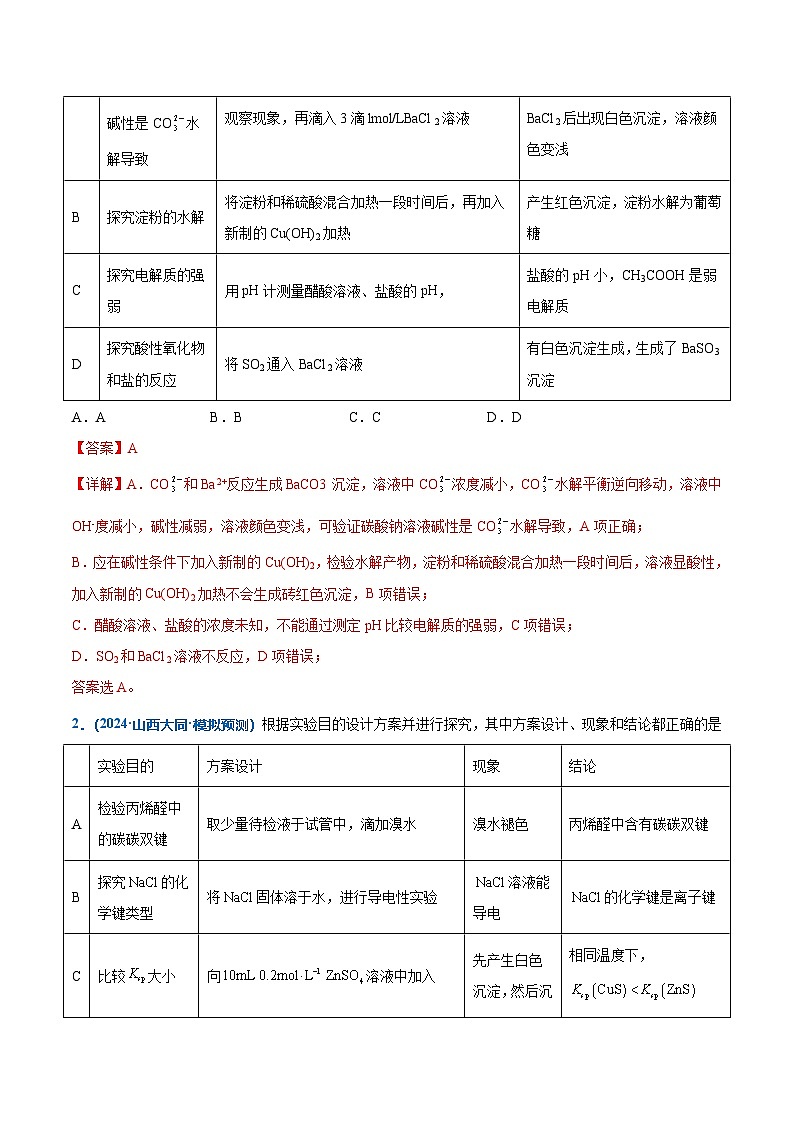
2.(2024·山西大同·模拟预测)根据实验目的设计方案并进行探究,其中方案设计、现象和结论都正确的是
A.AB.BC.CD.D
3.(2024·吉林白山·一模)为完成相应实验目的,下列方案设计、现象和结论均正确的是
A.AB.BC.CD.D
4.(2024·陕西·模拟预测)下列实验方案的设计不能达到实验目的的是
A.AB.BC.CD.D
5.(2024·陕西咸阳·联考)下列实验的方案设计、现象和结论都正确的是
A.AB.BC.CD.D
6.(2024·陕西安康·联考)化学实验源于生活。下列实验方案设计、现象与结论均正确的是
A.AB.BC.CD.D
7.(2024·山西运城·联考)下列实验方案设计、现象和结论都正确的是
A.AB.BC.CD.D
8.(2024·山西吕梁·联考)下列方案设计、现象和结论正确的是
A.AB.BC.CD.D
9.(2024·山西·联考)下列方案设计、现象和结论都正确的是
A.AB.BC.CD.D
10.(2024·陕西安康·联考)下列方案设计、现象和结论都正确的是
A.AB.BC.CD.D
11.(2024·山西·联考)下列方案设计、现象和结论都正确的是
A.AB.BC.CD.D
12.(2024·陕西咸阳·三模)为达到相应目的,下列方案设计、现象与结论均正确的是
A.AB.BC.CD.D
13.(2024·浙江·模拟预测)下列方案设计和结论都正确的是
A.AB.BC.CD.D
14.(2024·全国·模拟预测)下列实验方案设计、现象和结论都正确的是
A.AB.BC.CD.D
15.(2025·河南·联考)下列实验目的、方案设计和现象以及结论都正确的是
A.AB.BC.CD.D
16.(2025·江苏苏州·联考)下列方案设计、现象和结论都正确的是
A.AB.BC.CD.D
17.(2025·四川成都·联考)下列方案设计、现象和结论正确的是
A.AB.BC.CD.D
18.(2025·四川攀枝花·联考)根据下列实验方案设计、现象得出的结论正确的是
A.AB.BC.CD.D
1.(2025高三·福建福州·联考)探究铁及其化合物的性质,下列方案设计、现象和结论都正确的是
A.AB.BC.CD.D
2.(2025高三·河北邯郸·阶段练习)亚硝酸钠(NaNO2)俗称“工业盐”,其外观、口感与食盐相似,若误服会中毒。现将适量某样品(成分为NaNO2或NaCl)溶于水配成溶液,分别取少量该溶液于试管中进行下列实验,其中方案设计、现象和结论均正确的是
A.AB.BC.CD.D
3.(2025高三·浙江·联考)根据实验目的设计方案并进行实验,观察到相关现象,下列方案设计、结论均正确的是
A.AB.BC.CD.D
4.(2024·河北·联考)根据实验目的设计方案并进行实验,观察到相关现象,其中方案设计与结论都正确的是
A.AB.BC.CD.D
5.(2024·浙江丽水·联考)下列实验方案设计、现象和结论不正确的是
A.AB.BC.CD.D
6.(2025高三·山东济宁·开学考试)下列实验方案设计、现象和结论都正确的是
A.AB.BC.CD.D
7.(2025·海南海口·联考)下列方案设计、现象和结论都正确的是
A.AB.BC.CD.D
8.(2025·广东广州·联考)下列方案设计能达到实验目的的是
A.甲装置可以定量测定化学反应速率
B.乙装置可以由球中气体颜色的深浅判断温度对反应速率的影响
C.丙装置可以由褪色快慢研究反应物浓度对反应速率的影响
D.丁装置可以验证增大反应物浓度对化学平衡的影响
9.(2025·浙江·联考)下列方案设计、现象和结论正确的是
A.AB.BC.CD.D
10.(2025·河北石家庄·联考)下列方案设计、现象和结论都正确的是
A.AB.BC.CD.D
探究盐酸、碳酸、硅酸的酸性强弱
利用“强酸制弱酸”的原理探究:盐酸与碳酸盐反应制取CO2,气体净化后通入硅酸钠溶液中生成硅酸沉淀
利用盐的水解原理探究:用pH试纸(或pH计)测定同浓度的NaCl溶液、NaHCO3溶液、Na2SiO3溶液的pH,pH越大,则对应酸的酸性越弱
探究HCOOH、CH3COOH电离能力的强弱
用pH试纸(或pH计)分别测定同浓度的HCOOH溶液、CH3COOH溶液的pH
用pH试纸(或pH计)分别测定同浓度的HCOONa溶液、CH3COONa溶液的pH,盐溶液的pH越大,则对应酸的酸性越弱
探究Cl2、Fe3+、I2的氧化性强弱
利用“氧化剂的氧化性强于氧化产物的氧化性”原理探究:将氯气通入FeCl2溶液中,氯气将Fe2+氧化成Fe3+,将FeCl3溶液滴入淀粉-KI溶液中,Fe3+将I-氧化成I2
探究AgCl、AgI的溶度积大小
向少量的AgNO3溶液中滴加NaCl溶液至不再有白色沉淀生成,再向其中滴加KI溶液,产生黄色沉淀
向浓度均为0.1 ml·L-1的NaCl、NaI混合溶液中滴加0.1 ml·L-1 AgNO3溶液,先产生黄色沉淀
探究CuS、ZnS的溶度积大小
向浓度相同的CuSO4、ZnSO4的混合液中滴入Na2S溶液,若先生成黑色沉淀CuS、后生成白色沉淀ZnS,则说明Ksp(ZnS)>Ksp(CuS)
生成
气体
能够生成气体的离子很多,生成的气体的性质也常有相似之处,判断时要注意排除干扰离子
生成
沉淀
许多金属阳离子或酸根阴离子都可生成具有特殊颜色、特殊性质的沉淀,但同时也应注意排除干扰离子
呈现特殊颜色
特殊颜色的出现或消失并配合特殊试剂,是鉴别物质的常见方法,如KSCN检验Fe3+、淀粉检验I2等
选项
实验目的
方案设计
现象和结论
A
探究碳酸钠溶液碱性是CO水解导致
取溶液,滴入3滴酚酞,观察现象,再滴入3滴lml/LBaCl2溶液
滴入酚酞溶液变红,再滴入BaCl2后出现白色沉淀,溶液颜色变浅
B
探究淀粉的水解
将淀粉和稀硫酸混合加热一段时间后,再加入新制的Cu(OH)2加热
产生红色沉淀,淀粉水解为葡萄糖
C
探究电解质的强弱
用pH计测量醋酸溶液、盐酸的pH,
盐酸的pH小,CH3COOH是弱电解质
D
探究酸性氧化物和盐的反应
将SO2通入BaCl2溶液
有白色沉淀生成,生成了BaSO3沉淀
实验目的
方案设计
现象
结论
A
检验丙烯醛中的碳碳双键
取少量待检液于试管中,滴加溴水
溴水褪色
丙烯醛中含有碳碳双键
B
探究的化学键类型
将固体溶于水,进行导电性实验
溶液能导电
的化学键是离子键
C
比较大小
向溶液中加入溶液,再滴加溶液
先产生白色沉淀,然后沉淀变黑
相同温度下,
D
探究脱氧剂(主要成分是Fe粉)是否变质
取少量样品溶于盐酸,滴加溶液
无明显现象
脱氧剂没有变质
选项
实验目的
方案设计
现象和结论
A
探究铁粉在中燃烧所得固体粉末的成分
取少量固体粉末,加入蒸馏水,振荡,迅速滴入几滴溶液
溶液不显红色,说明该固体粉末中不存在
B
探究和的酸性强弱
将气体通入溶液中
产生白色沉淀,说明酸性:
C
探究温度对化学平衡的影响
加热盛有溶液的试管
加热,溶液变为黄色,冷却后变为蓝色,说明转化为的反应为吸热反应
D
检验溴乙烷中含溴元素
加热溴乙烷与的混合液,然后滴加溶液
有沉淀生成,说明溴乙烷中含溴元素
方案设计
实验目的
A
取少量久置溶液,滴加溶液,观察溶液颜色变化
检验溶液是否被氧化
B
分别测定等物质的量浓度的与溶液的pH
比较HF与的酸性
C
用饱和溶液浸泡一段时间后过滤、洗涤,向所得滤渣上滴加盐酸,产生无色气体
D
用铂丝蘸取少量溶液,做焰色实验,观察到火焰呈黄色
证明该溶液中存在
选项
实验目的
方案设计
现象和结论
A
检验固体中是否含有单质Cu
取样,加入足量稀盐酸,观察现象
若有红色固体剩余,则说明样品中有单质Cu
B
检验某固体试样中是否存在三价铁
取少量固体试样完全溶于盐酸,再滴加KSCN溶液
没有出现血红色,说明该固体试样中不存在三价铁
C
检验铜与浓硫酸反应是否有酸剩余
取少量反应冷却液加入盛有水的烧杯中,再逐滴滴加稀NaOH溶液
若不立即产生蓝色沉淀,则硫酸有剩余
D
比较镁与铝元素的金属性强弱
取与溶液于试管中,加入足量浓氨水
溶液出现白色沉淀,溶液先出现白色沉淀,后溶解,证明镁元素的金属性更强
选项
目的
方案设计
现象与结论
A
检验淀粉是否水解
向淀粉溶液中加入稀硫酸,加热几分钟,冷却后再加入新制悬浊液,加热
溶液中未观察到砖红色沉淀产生
B
检验火柴头中是否含有氯元素
将几根未燃过的火柴头浸入水中,稍后取少量溶液于试管中,加入稀和溶液
若有白色沉淀产生,说明火柴头中含有氯元素
C
检验菠菜中是否含有铁元素
取少量菠菜叶剪碎研磨后加水搅拌,取上层清液于试管中,加入稀硝酸后再加入KSCN溶液
若溶液变红,说明菠菜中含有铁元素
D
检验鸡皮中是否含有脂肪
取一小块鸡皮于表面皿上,将几滴浓硝酸滴到鸡皮上
一段时间后鸡皮变黄说明鸡皮中含有脂肪
选项
方案设计
现象
结论
A
将装满和的试管倒立在饱和食盐水中,光照
试管中气体颜色逐渐变浅,最终试管内充满液体
和发生了取代反应
B
取2mL鸡蛋清溶液于试管中,加入适量醋酸铅溶液,再加入足量水
产生白色沉淀且加水后沉淀不溶解
蛋白质发生变性
C
取未知溶液于试管中,加入溶液,有白色沉淀生成,再加足量稀盐酸
沉淀不溶解
溶液中一定含有
D
向溶液中滴加稀盐酸,再加入几滴KSCN溶液
溶液变为红色
稀盐酸可以将氧化为
目的
方案设计
现象和结论
A
检验海带中是否含有碘元素
将海带灰溶解过滤后,取适量滤液于试管中,酸化后加入少量新制氯水,充分反应后加入1~2滴淀粉溶液
溶液变蓝,则证明海带中含有碘元素
B
探究和HClO的酸性强弱
将气体通入溶液中
若产生白色沉淀,则说明酸性:
C
检验CO还原的生成物中是否含有
将适量反应后的固体溶于稀盐酸中,取少量溶解液于试管中,滴加硫氰化钾溶液
溶液变血红色,则证明还原产物中含有
D
验证某红棕色气体是否为
将气体通入淀粉碘化钾溶液
若溶液变蓝,则说明气体为
选项
实验方案
现象
结论
A
将新制饱和氯水慢慢滴入紫色石蕊溶液中
溶液先变红,当滴到一定量时,红色褪去
氯气具有酸性和漂白性
B
向盛有浓硝酸的两支试管中分别加入除去氧化膜的镁带和铝片
加入镁带的试管中迅速产生红棕色气体,加入铝片的试管中无明显现象
金属活泼性:
C
向溶液中先通入过量氯气,后滴加淀粉溶液
溶液先变橙,后变蓝
氧化性:
D
向溶液中,逐滴滴入的氨水
先产生沉淀,后沉淀溶解
结合银离子能力:氨分子>氢氧根离子
选项
目的
方案设计
现象和结论
A
乙烯的还原性
向盛有高锰酸钾酸性溶液的试管中通入足量的乙烯后静置
溶液的紫色逐渐褪去,静置后溶液分层
B
探究KI与反应的限度
取溶液于试管中,加入溶液,充分反应后滴入5滴溶液
若溶液变血红色,则KI与的反应有一定限度
C
检验乙醇中是否含有水
向乙醇中加入一小粒金属钠,产生无色气体
乙醇中含有水
D
探究蔗糖在酸性水溶液中的水解程度
取的蔗糖溶液于试管中,加入适量稀后水浴加热5min,再加入适量新制悬浊液并加热
若没有生成砖红色沉淀,则蔗糖没有水解
选项
目的
方案设计
现象和结论
A
确定苯中是否有乙醇
取少量待测液于试管中,加入适量金属钠
若有气泡产生,则样品中含有乙醇
B
探究某卤代烃中
的卤素原子
将少量样品与NaOH水溶液共热几分钟,待冷却后再加入AgNO3溶液
若有白色沉淀生成,则该卤代烃中含有氯原子的
C
确定某有机分子
中是否含有醛基
向待测液中加入新制银氨溶液,并用酒精灯加热
若出现明亮的银镜,则分子中含有醛基
D
探究乙醇消去反
应的产物
取4mL乙醇,加入12mL浓硫酸、少量沸石,迅速升温至140℃,将产生的气体通入2mL溴水中
若溴水褪色,则乙醇消去反应的产物为乙烯
选项
目的
方案设计
现象与结论
A
检验食盐中是否含有碘元素
向某品牌的食盐水溶液中滴加淀粉溶液
溶液颜色不变,说明该食盐为无碘盐
B
检验葡萄酒中是否含有SO2
向葡萄酒中滴加几滴酸性高锰酸钾溶液
高锰酸钾溶液紫色褪去,证明葡萄酒中含SO2
C
检验菠菜中的铁元素
取少量菠菜叶,剪碎研磨后加水搅拌,取上层清液于试管中,加入新制氯水后再滴入KSCN溶液
若溶液变红,说明菠菜中含有铁元素
D
检验鸡皮中是否含有脂肪
取一小块鸡皮于表面皿上,滴几滴浓硝酸于鸡皮上
一段时间后鸡皮变黄,说明鸡皮中含有脂肪
选项
目的
方案设计
现象和结论
A
判断固体化合物是否是铵盐
取少量样品加水溶解,加足量NaOH溶液并加热,在试管口放一张湿润的红色石蕊试纸,观察现象
若试纸变蓝,说明该化合物属于铵盐
B
检验铁粉与水蒸气反应产物中铁元素的价态
取反应后的固体溶于足量稀硫酸,并滴加KSCN溶液,观察现象
若溶液未显红色,说明产物中铁元素为二价铁
C
研究淀粉的水解程度
取0.5g淀粉于试管中,加适量20%的硫酸溶液,沸水浴加热5min,再滴加足量NaOH溶液,加入适量碘水,观察现象
若溶液未显蓝色,说明淀粉已经水解完全
D
验证反应物浓度增大可加快反应速率
在甲、乙两支试管中均加入1mL0.01 ml∙L-1高锰酸钾溶液,再分别同时加入0.1 ml∙L-1和0.05 ml∙L-1的草酸溶液各1mL,观察现象
若甲试管中溶液紫色先褪去,说明反应物浓度增大时,反应速率加快
选项
方案设计
现象
结论
A
25℃时,用pH试纸分别测定饱和溶液和饱和溶液的pH
pH:
的
B
将灼热的木炭投入浓硝酸中
有红棕色气体产生
浓硝酸能氧化木炭
C
向白葡萄酒中滴加几滴酸性高锰酸钾溶液
溶液紫色褪去
葡萄酒中含
D
向2mL 0.1溶液中滴加2~4滴2NaOH溶液,继续滴加4滴0.1溶液
先出现白色沉淀,之后转化为红褐色
选项
实验目的
方案设计和现象
结论
A
判断AlCl3的化学键类型
将AlCl3固体溶于水,进行导电性实验,AlCl3溶液可导电
AlCl3中含有离子键
B
验证某固体是Na2CO3还是NaHCO3
室温下取少量固体于试管中,插入温度计,加几滴水,温度降低
该固体是Na2CO3
C
验证Cl-能加速破坏铝片表面的氧化膜
将一块未经打磨的铝片剪成相同的两小片,相同温度下分别投入5.0mL浓度均为2.0ml/L的CuSO4溶液和CuCl2溶液中,CuSO4溶液中无明显现象;CuCl2溶液中反应剧烈,铝片表面有红色物质生成
说明Cl-能加速破坏铝片表面的氧化膜
D
探究钠在空气中久置后所得固体成分
把一块绿豆大的久置后的钠固体放入蒸馏水中,有气体产生
固体中一定含有Na2O2
选项
方案设计
现象
结论
A
往2支试管中各加入1mL乙酸乙酯,再分别加入等体积等浓度的稀硫酸和NaOH溶液,置于同温度水浴加热
NaOH溶液中酯层消失的快
碱催化酯水解的效果比酸的催化效果好
B
向等浓度、等体积的H2O2中分别加入等浓度、等体积的KMnO4溶液和CuSO4溶液
前者产生气泡速率快
过氧化氢分解催化效果KMnO4>CuSO4
C
在4mL0.1ml/LK2Cr2O7溶液中加入数滴1ml/LNaOH溶液
溶液由橙色变为黄色
(橙色)+H2O(黄色)+2H+反应平衡正向移动
D
取少量“Fe粉与HNO3”反应后的溶液于试管中,依次加入H2SO4和Fe粉
有有色气体产生
HNO3过量
目的
方案设计
现象和结论
A
比较Na2CO3和NaHCO3溶液碱性强弱
相同温度下,向等浓度的两份溶液中分别滴入3滴酚酞,观察现象
观察到红色较深的是NaHCO3,说明碱性NaHCO3>Na2CO3
B
鉴别Na2CO3和NaHCO3固体
分别在两支试管中加入少量待检固体,再加入几滴水,用温度计测定变化
温度升高的是Na2CO3固体,温度略有下降的是NaHCO3固体
C
鉴别Na2O和Na2O2固体
将两种固体分别加入有水的试管中,观察现象
两支试管均有气泡产生,气体产生较快的是Na2O2
D
比较碳酸和盐酸的酸性强弱
适量二氧化碳通入氯化钡溶液中,观察现象
产生沉淀,碳酸的酸性比盐酸弱
选项
方案设计
现象
结论
A
取淀粉与稀硫酸的水解液加入过量NaOH,再加入碘水
溶液不变蓝
淀粉已完全水解
B
向白葡萄酒中滴加几滴酸性高锰酸钾溶液
溶液紫色褪去
葡萄酒中含SO2
C
将液态钠与液态四氯化钛加热至810℃(Na、Ti、NaCl的熔点分别为97℃、1668℃、801℃)
有银白色固体产生
不能说明还原性Na>Ti
D
取少量菠菜叶研磨后加水搅拌,静置,取上层清液于试管中,加入氯水,再滴加KSCN溶液
溶液变红
菠菜叶中含铁元素
实验方案
现象
结论
A
往溶液中加入片
溶液颜色由浅绿色变为无色
的氧化能力比强
B
往溶液中滴加溶液再加入少量固体
溶液先变成血红色后无明显变化
与的反应不可逆
C
将食品脱氧剂样品和还原铁粉溶于盐酸滴加溶液
溶液呈浅绿色
食品脱氧剂样品中没有价铁
D
向沸水中逐滴加5~6滴饱和溶液持续煮沸
溶液先变成红褐色再析出沉淀
此操作最终可制得胶体
选项
方案设计
现象和结论
A
先加入少量溶液,再加入稀硝酸酸化,振荡
若溶液变黄色,则样品为NaNO2
B
先加入少量溶液,再加硫酸酸化,振荡
若溶液褪色,则样品为NaNO2
C
先加入少量溶液,再加入溶液和稀盐酸,振荡
若产生白色沉淀,则样品为NaNO2
D
先加入少量KClO3溶液,再加AgNO3溶液和足量稀硝酸,振荡
若产生白色沉淀,则样品为NaNO2
选项
实验目的
方案设计
现象
结论
A
探究铜和浓硫酸反应的产物
将铜丝放入浓硫酸中,加热
开始时铜丝表面变黑,产生无色气体,后黑色固体溶解
由氧化还原反应规律可知黑色固体一定是CuO
B
判断的化学键类型
将固体溶于水,进行导电性实验
溶液可导电
中含有离子键
C
探究浓硝酸与碳在加热条件下能否反应
将红热的木炭投入浓硝酸中
产生红棕色气体
碳与浓硝酸在加热条件下反应生成
D
探究和的反应{已知含的溶液呈红棕色}
将气体通入溶液中
溶液先变为红棕色,过一段时间又变成浅绿色
与络合反应速率比氧化还原反应速率大,但氧化还原反应的平衡常数更大
实验目的
方案设计
现象
结论
A
检验固体样品中是否含有
将固体样品加少量水溶解,滴入浓溶液,试管口放一张湿润的红色石茲试纸
湿润的红色石蕊试纸变蓝
样品中含有
B
探究铝与浓硝的钝化现象
室温下,将铝片直接放入浓硝酸中,一段时间后取出并用水洗净,放入溶液中
铝片表面未见紫红色固体生成
室温下浓硝酸能将铝片钝化
C
探究C、元素非金属性的强弱
向溶液中加入过量的盐酸
有气泡生成
非金属性:
D
检验固体是否变质
取少量固体溶于蒸馏水,然后滴加少量稀硫酸,再滴入溶液
溶液变红
固体已变质
选项
方案设计
现象
结论
A
取溶液于试管中,加入溶液,充分反应后滴入几滴溶液
溶液变血红色
与的反应有一定限度
B
向蔗糖固体中加入浓硫酸
蔗糖变黑,体积膨胀,并放出有刺激性气味的气体
浓硫酸具有脱水性和强氧化性
C
向盛有某无机溶液的试管中加入氢氧化钠溶液并加热,将湿润的红色石蕊试纸置于试管口
试纸变蓝
原溶液中含有
D
向某钠盐中滴加浓盐酸,并将产生的气体通入品红溶液
品红溶液褪色
该钠盐可能为
选项
实验目的
方案设计
现象和结论
A
检验,是否变质
向溶液中加入硫酸酸化的KSCN溶液,溶液呈血红色
说明已变质
B
向溶液中通入后再通入气体X
产生白色沉淀
气体X可能是
C
检验溶液是否含
向溶液中加入稀氢氧化钠溶液,用湿润的红色石蕊试纸靠近管口
若试纸未变蓝,则说明不含
D
向滴有酚酞的NaOH溶液中通入
溶液褪色
具有漂白性
实验方案
现象
结论
A
向溶液中滴加溶液
红色变浅
使平衡逆向移动
B
向的醋酸中滴加碳酸钠溶液
有气泡产生
醋酸的酸性强于碳酸
C
向两个同规格烧瓶中分别装入同比例和的混合气体,封闭后并分别浸泡于热水和冷水中
热水烧瓶内颜色较深
是吸热反应
D
取等体积等浓度的两种酸和,测量导电能力
溶液中灯泡更亮
是强酸,是弱酸
目的
方案设计
现象和结论
A
比较不同的粒子和结合能力大小
在12%溶液中,逐滴滴入2%的氨水
先产生沉淀,后沉淀溶解,说明结合能力:
B
比较与的酸性强弱
分别用玻璃板蘸取与溶液点在试纸上,观察现象
前者大,说明酸性弱于
C
探究温度对下列平衡的影响:
把装有和混合气体的烧瓶浸入热水中
颜色加深,平衡逆向移动,表明逆反应是放热反应
D
比较、的
向含有浓度均为0.001的与溶液中,逐滴滴加0.001溶液
生成白色沉淀,所以:
选项
目的
方案设计
现象和结论
A
比较AgCl、AgI的Ksp大小
向1mL0.lml/LAgNO3溶液中先滴加两滴0.1ml/L NaCl溶液,再滴加两滴0.1ml/LKI溶液
先产生白色沉淀,后产生黄色沉淀,Ksp(AgCl)>Kp(AgI)
B
比较CH3COOH与H2CO3的酸性
测定同温同浓度CH3COONa溶液和Na2CO3溶液的pH
Na2CO3的pH大,CH3COOH酸性强于H2CO3
C
验证Na2CO3溶液中存在水解平衡
往2mL含有酚酞的Na2CO3溶液中,加入少量BaCl2晶体
产生白色沉淀且溶液红色变浅,Na2CO3溶液中存在水解平衡
D
探究压强对化学平衡的影响
在容积不变的密闭容器中发生反应:N2(g)+3H2(g) ⇌2NH3(g)向其中通入氩气
化学平衡不移动,化学平衡不受压强影响
相关试卷
这是一份热点题型06 电化学及其应用-2025年高考化学 热点 重点 难点 专练(西北四省专用),文件包含热点题型06电化学及其应用-2025年高考化学热点重点难点专练西北四省专用原卷版docx、热点题型06电化学及其应用-2025年高考化学热点重点难点专练西北四省专用解析版docx等2份试卷配套教学资源,其中试卷共48页, 欢迎下载使用。
这是一份热点题型04 化学反应机理探究与分析-2025年高考化学 热点 重点 难点 专练(西北四省专用),文件包含热点题型04化学反应机理探究与分析-2025年高考化学热点重点难点专练西北四省专用原卷版docx、热点题型04化学反应机理探究与分析-2025年高考化学热点重点难点专练西北四省专用解析版docx等2份试卷配套教学资源,其中试卷共44页, 欢迎下载使用。
这是一份热点题型03 化学微型实验-2025年高考化学 热点 重点 难点 专练(西北四省专用),文件包含热点题型03化学微型实验-2025年高考化学热点重点难点专练西北四省专用原卷版docx、热点题型03化学微型实验-2025年高考化学热点重点难点专练西北四省专用解析版docx等2份试卷配套教学资源,其中试卷共59页, 欢迎下载使用。








