




高中化学鲁科版 (2019)选择性必修2第2节 共价键与分子的空间结构获奖ppt课件
展开meiyangyang8602
请你说说!在日常生活中,你注意到自然景观等所显示的对称性。
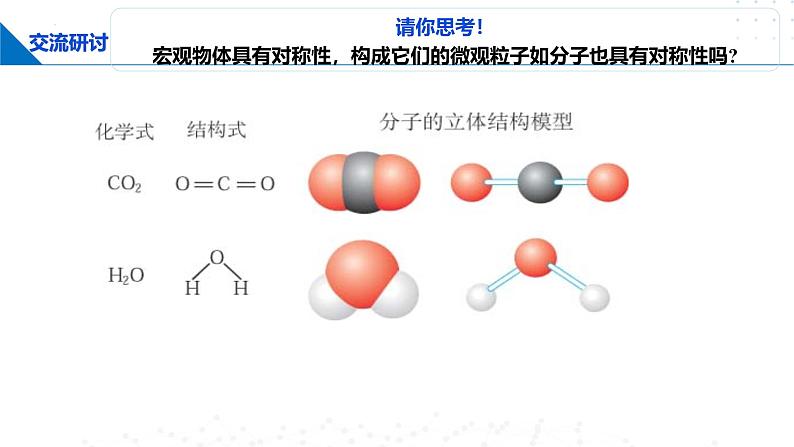
请你思考!宏观物体具有对称性,构成它们的微观粒子如分子也具有对称性吗?
第二章 微粒间相互作用与物质性质
第 2 节 共价键与分子的空间结构
课时3 分子的空间结构与分子性质
通过学习鲍林的杂化轨道理论、价电对互斥理论,学生对分子结构有了深入的认识,既能解释简单分子的空间结构的的成因,也能预测简单分子或离子的空间结构。本节课在此基础上进一步讨论了分子空间结构对分子某些性质的影响。通过对分子空间结构与性质(手性,极性)的讨论,有利于发展学生“结构决定性质”的科学思想,提升化学学科核心素养。。
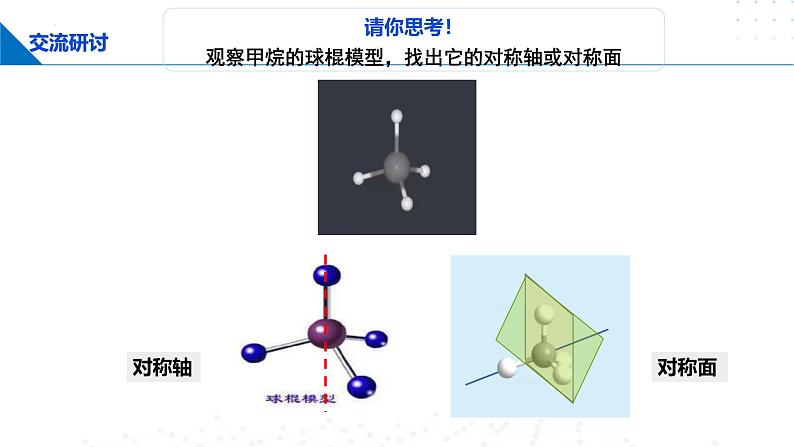
请你思考!观察甲烷的球棍模型,找出它的对称轴或对称面
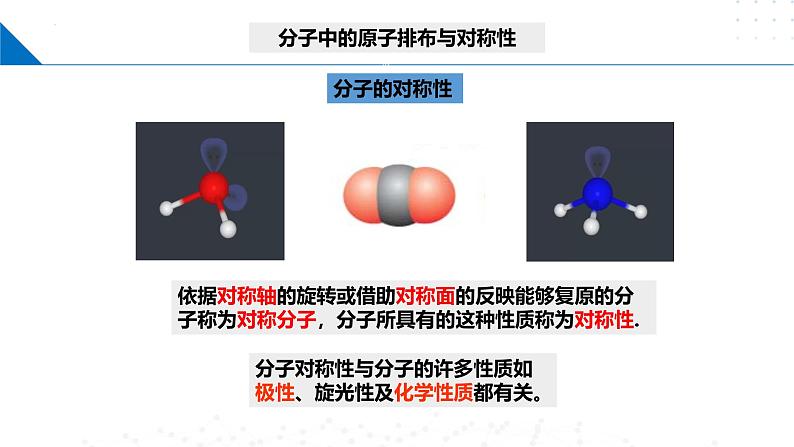
分子中的原子排布与对称性
依据对称轴的旋转或借助对称面的反映能够复原的分子称为对称分子,分子所具有的这种性质称为对称性.
分子对称性与分子的许多性质如极性、旋光性及化学性质都有关。
请你观察!下面两个分子能否完全重合?
互为镜像关系的分子能叠合,是同种分子
互为镜像关系的分子不能叠合,不是同种分子
一种分子本身和它在镜中的像,就如同人的左右手,相似但不能重叠,我们称它们的表现为手性。
手性分子和它的镜像分子构成一对对映异构体。互为对映异构体的两种分子具有相反的旋光性。
在光通过某些化合物时,光波振动的方向会旋转一定的角度,这种性质称为旋光性。
请你思考! 1.这些分子的碳原子以何种方式杂化?2.分子是否具有手性?
以不同色的球代表不同的原子,各小组分别组装下列分子的球棍模型:
大多数的手性分子都含有不对称碳原子(手性碳原子)。
连接四个不同的原子或基团的碳原子。
不对称碳原子采取sp3杂化,采取sp或sp2杂化的一定不是不对称碳原子!
手性碳原子:有机物分子中连有四个各不相同的原子或基团的碳原子。
1.下列化合物中含有手性碳原子的是( ) A.CCl2F2 B. CH3—CH—COOH C.CH3CH2OH D. CH—OH
A.OHC—CH—CH2OH B. OHC—CH—C—ClC.HOOC—CH—C—C—Cl D.CH3—CH—C—CH3
2.下列化合物中含有2个“手性”碳原子的是( )
不同异构体的生理活性相差很大,甚至完全相反。因此,药物的不对称合成早已成为人们极为注目的研究领域。
21世纪的第一个诺贝尔化学奖:手性催化反应领域
请你思考! 微波炉的加热原理?
分子中的电荷分布与极性
1. 使用四氯化碳、水做实验时,观察到的现象是否相同?2. 请画图分析四氯化碳分子和水分子中的化学键是极性键还是非极性键,电荷在化学键乃至整个分子中是如何分布的。这对你解释上述实验现象有什么启示?
请画图分析四氯化碳分子和水分子中的化学键是极性键还是非极性键,电荷在化学键乃至整个分子中是如何分布的。
正电重心和负电重心不重合;H2O中存在着带正电荷的正极和带负电荷的负极。
正电重心和负电重心重合;CCl4分子中无正极和负极之分.
像水分子这样分子内存在正、负两极的分子,称为极性分子(plar mlecule)
即:正、负电荷重心不重合的分子
氯化氢分子——极性分子
像四氯化碳分子这样分子内不存在正、负两极的分子,称为非极性分子(nn-plar mlecule)
即:正、负电荷重心重合的分子
请你思考! 分析氨、二氧化碳和甲烷等分子中各原子的带电情况,指出其中的极性分子和非极性分子并说明理由
正、负电荷重心不重合的是极性分子
正、负电荷重心重合的是非极性分子
双原子分子的极性与化学键的极性一致
分子极性也可根据化学键的极性的向量和判断
大多数情况,含有非极性键的多原子分子是非极性分子
多原子分子的极性与化学键的极性以及分子的空间结构均有关
根据中心原子的化合价判断
中心原子的化合价绝对值 =
中心原子的化合价绝对值 ≠
1,回答下列问题①H2 ②O2 ③HCl ④P4 ⑤C60 ⑥CO2 ⑦CH2==CH2 ⑧HCN ⑨H2O ⑩NH3 ⑪BF3 ⑫CH4 ⑬SO3 ⑭CH3Cl ⑮Ar ⑯H2O2(1)只含非极性键的是_________;只含极性键的是___________________,既含极性键又含非极性键的是_____。(2)属于非极性分子的是_______________________,属于极性分子的是_____________。
分子极性对物质性质的影响
分子的极性对物质的熔、沸点有一定影响
相对分子质量相等的分子,分子极性大,分子间的电性作用强,分子间作用力大,熔、沸点较高。
CO分子 >N2 分子
一般情况下,由极性分子构成的物质易溶于极性溶剂,由非极性分子构成的物质易溶于非极性溶剂。
解释:卤素单质易溶于有机溶剂,微溶于水。
资料在线:糖周围水的密度增大,溶液向周围密度小的地方扩散,相邻两颗糖色素溶于水后密度相似,它们会向盘子中央密度更小的区域扩散,于是形成彩虹漩涡。
色素属于极性分子,根据相似相溶原理,可与水互溶。
分子中极性较大的基团具有亲水性,极性较小的基团具有亲脂性(或称为疏水性)。有些分子中既含有亲水性的基团,又含有疏水性的基团,由这类分子构成的物质称为表面活性剂。
1.下列中心原子采取sp2杂化且为非极性分子的是( )A.CS2 B.H2S C.SO2 D.SO3
2.下列叙述正确的是( )A.NO、N2O、NO2、NH3都是非极性分子B.CO2、SO3、BCl3、NF5都是非极性分子C.H2O、NH3是极性分子,分子中的H—O比N—H的极性弱D.PCl5、NCl3、SO3、BF3、CCl4都是非极性分子
3.①PH3分子的空间结构为三角锥形,②BeCl2分子的空间结构为直线形,③CH4分子的空间结构为正四面体形,④CO2为直线形分子,⑤BF3分子的空间结构为平面三角形,⑥NF3分子结构为三角锥形。下面对分子极性的判断正确的是( )A.①⑥为极性分子,②③④⑤为非极性分子B.只有④为非极性分子,其余为极性分子C.只有②⑤是极性分子,其余为非极性分子D.只有①③是非极性分子,其余是极性分子
鲁科版 (2019)选择性必修2第2节 共价键与分子的空间结构试讲课课件ppt: 这是一份鲁科版 (2019)选择性必修2<a href="/hx/tb_c4002602_t3/?tag_id=26" target="_blank">第2节 共价键与分子的空间结构试讲课课件ppt</a>,共48页。PPT课件主要包含了教材分析,sp2,sp3,演示实验,带负电荷,BF3,CO2,PCl5,SO3,H2O等内容,欢迎下载使用。
高中化学鲁科版 (2019)选择性必修2第2章 微粒间相互作用与物质性质第2节 共价键与分子的空间结构图文ppt课件: 这是一份高中化学鲁科版 (2019)选择性必修2<a href="/hx/tb_c4002602_t3/?tag_id=26" target="_blank">第2章 微粒间相互作用与物质性质第2节 共价键与分子的空间结构图文ppt课件</a>,共47页。PPT课件主要包含了教材分析,sp2,sp3,演示实验,带负电荷,BF3,CO2,PCl5,SO3,H2O等内容,欢迎下载使用。
高中化学沪科技版(2020)选择性必修2共价键的形成与性质教学演示课件ppt: 这是一份高中化学沪科技版(2020)选择性必修2<a href="/hx/tb_c4036484_t3/?tag_id=26" target="_blank">共价键的形成与性质教学演示课件ppt</a>,文件包含21共价分子的空间结构教学课件pptx、21共价分子的空间结构分层作业原卷版docx、21共价分子的空间结构分层作业解析版docx等3份课件配套教学资源,其中PPT共60页, 欢迎下载使用。













