






高中鲁科版 (2019)第1节 原子结构模型精品课件ppt
展开第一节 原子结构模型 课时1 原子结构模型
第一章 原子结构与元素性质
通过"联想·质疑",回顾人类对原子结构的认识历程,提出需要探究的总问题∶现代科学对原子结构的描述究竟是怎样的?通过"观察·思考",了解氢原子光谱事实与卢瑟福核式模型产生的冲突,促使玻尔建立新的理论来解释光谱现象,提出能量量子化。通过"联想·质疑",促使学生再次体会玻尔理论无法解释更复杂的光谱现象,因此多位科学家打破原有理论,建立新的量子力学理论,提出了电子层、能级、原子轨道、自旋概念及其量子化现象以用来描述原子核外电子的运动状态,并且均有光谱现象作为证据。微观粒子与宏观物体运动的不同在于前者具有波动性,因无法同时准确测定其位置和速度,而用电子云来形象描述电子在单位体积内的概率分布;量子力学用波函数描述原子轨道,并用波函数的图形形象化呈现。
请你说说!回顾人类对原子结构的认识过程,你收到了哪些启发?
古希腊哲学家德谟克利特 物质是由不可分割的微粒(原子)构成的
请你总结!原子结构模型的演变
19世纪初,英国化学家和物理学家道尔顿根据实验结果,提出了原子论。其主要内容包括:1.元素是由不可再分的极小微粒构成,这种微粒成为原子。原子在一切化学变化中保持其不可再分性。2.同一元素的原子在质量和性质上都相同,不同元素的原子在质量和性质上都不同3.不同元素化合时,这些元素的原子按简单整数比结合
1858年德国物理学家普吕克尔发现了阴极射线。1897年汤姆孙用阴极射线管重复阴极射线实验。在阴阳两极加上电压,阴极会产生阴极射线。当对阴极射线施加电场后,阴极射线发生偏转。从而证明阴极射线是一种带电粒子。经过一系列的实验后,汤姆孙提出:1.带负电的粒子是构成各种物质的共有成分2.该粒子所带电荷的大小与氢离子大致相同,这种带负电的粒子即为电子。
meiyangyang8602
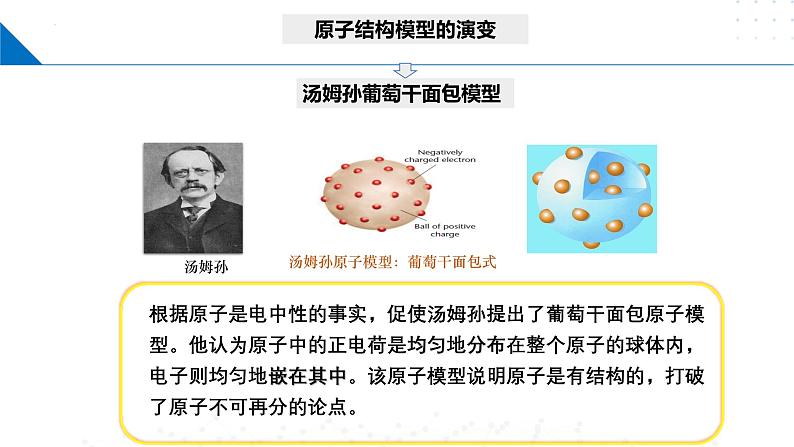
根据原子是电中性的事实,促使汤姆孙提出了葡萄干面包原子模型。他认为原子中的正电荷是均匀地分布在整个原子的球体内,电子则均匀地嵌在其中。该原子模型说明原子是有结构的,打破了原子不可再分的论点。
卢瑟福的带核原子结构模型
“意外跑偏”的α粒子——α粒子散射实验
卢瑟福原子模型(1911年):在原子的中心有一个带正电荷的核,它的质量几乎等于原子的全部质量,电子在它的周围沿着不同的轨道运转,就像行星环绕太阳运转一样。
在模型提出后不久,就遭到了严重的质疑
玻尔的疑惑: 依据卢瑟福的原子模型,带电粒子有加速度时辐射能量,电子轨道半径会连续缩小,电子轨道连续缩小,其运动频率连续变化,光谱应是连续的。
玻尔的轨道原子结构模型
玻尔研究发现,氢原子光谱不连续的现象,通过实验并引入量子论观点,解决了卢瑟福核式结构模型不稳定的问题,提出了一个全新的原子结构模型。
丹麦物理学家玻尔指出:原子核外,电子在一系列稳定的轨道上运动,每个轨道都具有一个确定的能量值;核外电子在这些稳定的轨道上运动时,既不放出能量,也不吸收能量。
现代原子结构理论:电子云模型
1926年,奥地利物理学家薛定谔在德布罗意、海森堡、泡利等人研究的基础上,提出了原子核外的电子排布的新模型——电子云模型,并提出了著名的薛定谔方程式。现代原子结构理论认为:电子在原子核外很小的空间内做高速运动,其运行没有固定的规律。用小黑点的疏密来表示单位体积内电子出现几率。
道尔顿原子模型:实心球
汤姆生原子模型:葡萄干面包
卢瑟福原子模型:行星模型
玻尔原子模型:量子化轨道
科学家探索原子结构的一般方法
创造性的设计实验创造性地提出新理论
联想质疑回顾人类对原子结构的认识过程,你收到了哪些启发?
科学研究永远在不断否定、不断肯定中波浪式前进。保持你的好奇心、求知欲,在继承前人的同时,具有敏锐的洞察力,善于根据新的实验证据去修正原来的理论,开辟出一片新的领域。人类在认识自然的过程中,经历了无数的艰辛,正是因为有了无数的探索者,才使人类对事物的认识一步步走向深入,也越来越接近事物的本质。
你知道吗?现代科学对原子结构的描述究竟是怎样的?
玻尔理论的出现解决了什么问题呢?
氢原子光谱和玻尔的原子结构模型
请你思考!观看视频并阅读教材P2-P4页内容思考以下问题
人们常常利用原子光谱仪将物质吸收的光或发射的光的频率(或波长)和强度分布记录下来得到光谱。
请你思考!(2)根据卢瑟福的核式模型,原子光谱应该是什么光谱?
如果原子结构真如卢瑟福的核式模型所描述的那样,根据经典的电动力学观点,围绕原子核高速运动的电子一定会自动且连续地辐射能量,最终坍塌到原子核上。这样,不仅原子是不稳定的,而且原子的光谱应当是连续光谱,即波长的变化呈连续分布
氢原子光谱是由具有特定波长、彼此分立的谱线组成的线状光谱
请描述氢原子光谱的特点,并说明这对你推测氢原子核外电子的运动特点有什么启示?
为了解释这一实验事实,玻尔在卢瑟福核式模型的基础上提出了核外电子分层排布的原子结构模型
获得了1922年的诺贝尔物理学奖
(1)原子中的电子在具有确定半径的圆周轨道上绕原子核运动,并且不辐射能量。
(2)在不同轨道上运动的电子具有不同的能量(E),而且能量值是不连续的,这称为能量"量子化"。轨道能量依n值(1、2、3、…)的增大而升高,n称为量子数。对氢原子而言,电子处在n=1的轨道时能量最低,这种状态称为基态;能量高于基态能量的状态,称为激发态。
(3)只有当电子从一个轨道(能量为E;)跃迁到另一个轨道(能量为E;)时,才会辐射或吸收能量。当辐射或吸收的能量以光的形式表现出来并被记录,就形成了光谱。
不同原子的电子发生跃迁时可以吸收不同的光,用光谱仪可以摄取各种原子吸收光谱。
不同原子的电子发生跃迁时可以发射不同的光,用光谱仪可以摄取各种原子的发射光谱。
请你思考!为什么氢原子光谱是由具有特定波长、彼此分立的谱线组成的?
根据玻尔模型,电子所处的轨道的能量是量子化的,轨道间的能量差也是确定的,而光的频率与轨道所具有的能量 E 之间的关系可用下式表示。 h = | Ej - Ei |式中:h 为普朗克常数,其值为 6.626×10-34 J·s。由上式计算得到的光的频率 (或波长 λ=c// ,c 为光速)只能是不连续的,此时形成的是具有特征波长的线状光谱。
E = E2- E1= h (=c/)
(1)成功地解释了氢原子光谱是线状光谱的实验事实, (2)阐明了原子光谱源自核外电子在能量不同的轨道之间的跃迁,而电子所处的轨道的能量是量子化的。
[联想·质疑]波尔只引入一个量子数n,能比较好地解释了氢原子线状光谱产生的原因;但复杂的光谱解释不了。
显然,上述问题只用玻尔的轨道概念和量子数 n 是无法解释的。
那么,应当如何解释氢原子的光谱和多电子原子的光谱所产生的复杂现象呢?原子核外电子的运动状态是否还存在玻尔原子结构模型未能描述的其他量子化现象呢?
德国物理学家、量子力学的创立者海森堡
无法同时精确测量某个电子在某一时刻的位置和速率。
1932年获诺贝尔物理学奖
量子力学诞生于1925年末至1926年初,它是由两组物理学家相互独立地用不同方法建立的。直接因量子力学而获得诺贝尔物理学奖的就有六位∶德布罗意( Brglie,1929年)、海森堡(W.Heisenberg,1932年)、狄拉克(,1933年)和薛定谔(E.Schrödinger,1933年)、泡利(,1945年)和玻恩(M.Brn,1954年)。
1927年 第五届索尔维会议
19世纪末,经典力学和经典电动力学在描述微观系统时的不足越来越明显。量子力学是在20世纪初由马克斯·普朗克、尼尔斯·玻尔、沃纳·海森堡、埃尔温·薛定谔、沃尔夫冈·泡利、路易·德布罗意、马克斯·玻恩、恩里科·费米、保罗·狄拉克、阿尔伯特·爱因斯坦、康普顿等一大批物理学家共同创立的。
受到光既具有波动性又具有粒子性的事实的启发,法国物理学家德布罗意提出了微观粒子具有波动性的观点。德布罗意还天才性地预测“一束电子通过一个非常小的孔时可能会产生衍射现象……”。爱因斯坦对德布罗意的观点给予了极高的赞誉,称其“揭开了一幅大幕的一角”。1927 年,美国物理学家戴维孙(C.Davissn)和革末(L.Germer)将电子射到镍的单晶上,得到了完全类似于 X 射线被晶体衍射的图样,证实了电子的确具有波动性。图 1-1-9 显示的是铝箔的电子衍射图样。后来用中子、原子、分子等粒子流代替电子流,也都观察到了衍射现象。人们之所以不能同时准确地测定微观粒子的位置和速度,正是因为微观粒子具有波动性。
以德国物理学家海森堡和泡利为代表的一组物理学家为了解释原子分立能级,创立了矩阵力学。另一组以奥地利物理学家薛定为代表,过建立描述电子运动状态的波动方程来解释电子的波动性,从而创立了波动力学。
量子力学指出:一定空间运动状态的电子并不在玻尔假设的线性轨道上运动,而是在核外空间各处都可以出现,只是出现的概率不同。
薛定语证明了这两种表现形式完全不同的理论实际上是同一种物理规律的两种不同的数字表达形式。
后来经过英国物理学家狄拉克的发展,该理论成为一门相对完整的、即量子力学。
量子力学是目前解决低能量的微观粒子问题的最佳理论。近代量子力学不仅揭示了原子结构、放射性、化学键以及原子光谱的实质,而且与其他理论(如相对论)相结合,成功地解释了核结构与核反应、固体的电性与热性、超导性、物质的基本粒子的产生与湮灭、反物质的存在、某些坍塌恒星的稳定性等问题。该理论的产生同时促进了包括电子显微镜、顺磁共振仪、激光器、晶体管和扫描隧道显微镜在内的许多先进仪器及相应实用技术的快速发展。
量子力学对原子核外电子运动状态的描述
薛定谔方程与四个量子数
①主量子数n: 描述电子离核的远近. n取值为正整数1,2,3,4,5,6… 对应符号为 K,L,M,N,O,P… 习惯上,将 n 所描述的电子运动状态称为电子层
n越大,电子离核的平均距离越远,电子具有能量越高
②角量子数l :描述(电子云)原子轨道的形状. l 取值为 0,1,2,3… (n-1).共n个数值. 符号为 s, p(3个:px、py、pz),d(5个),f(7个)等.若电子的能层n、 能级l 的相同,则电子的能量相同.在一个电子层中,l 的取值有多少个,表示电子层有多少个不同的能级.
规律: 每层的能级数值=电子层数
③磁量子数m: 描述磁场中原子轨道的能量状态 m可以取0、±1、±2 … ±l共(2l +1)个数值. 如l =0, m只可以取0,对应的谱线只有一条. 如l =1, m可以取0, ±1,对应的谱线有三条. n、 l 、m确定,原子轨道就确定了.
描述原子中单个电子的空间运动状态
电子层、能级、轨道数关系
④自旋量子数ms:描述在能量完全相同时电子运动的特殊状态(简称为电子自旋状态). 处于同轨道上的电子的自旋状态只有两种. 分别用ms =+1/2(通常用符号↑表示). ms= -1/2 (通常用符号↓表示).注意:自旋并不是”自转”,实际意义更为深远.
处于同一原子轨道上的电子,自旋状态只有两种,分别用符号“↑”和“↓”表示。
(4)自旋运动:描述同一轨道中电子的不同空间运动状态
(1)任一电子层的能级总是从s能级开始,能级数等于该电子层的序数:第一电子层只有1个能级(1s),第二电子层有2个能级(2s和2p),第三电子层有3个能级(3s、3p和3d),即任一电子层,能级数=电子层序数。
(2)电子层与能级类似楼层与阶梯之间的关系,在每一个电子层中,能级符号顺序是ns、np、nd、nf…(如图所示)。
(3)同一能级又可能包含几个空间取向不同的原子轨道,s能级中有1个原子轨道、p能级中有3个能量相同的原子轨道,分别记作“npx、npy、npz”,d能级中有5个能量相同的原子轨道。
2. 原子轨道的图形描述
原子中单个电子的空间运动状态用原子轨道来描述,而原子轨道在量子力学中用波函数来表示,并可以将其以图形的方式在直角坐标系中呈现出来。
p 轨道在三维空间分布的图形与 s 轨道明显不同,它的空间分布特点是分别相对于 x、y、z 轴对称,也就是说,p 轨道在空间分别沿 x、y、z 轴的方向分布。
d 轨道(l = 2, m = +2, +1, 0, -1, -2) m 五种取值, 空间五种取向, 五条等价(简并) d 轨道.
f 轨道 ( l = 3, m = +3, +2, +1, 0, -1, -2, -3 ) m 七种取值, 空间七种取向, 七条等价(简并) f 轨道.
请你思考!原子轨道可以用波函数来表示,那么,又该如何理解波函数?怎样形象地描述电子在空间中的运动与分布呢?
3. 电子在核外的空间分布
与对宏观物体运动的描述不同,对于质量非常小、运行速度极快且运动空间极小的微观粒子而言,人们不可能同时准确地测定它的位置和速度,但能通过对波函数进行数学处理计算出电子在什么地方出现的概率大、在什么地方出现的概率小。
3.电子在核外的空间分布
这种形象地描述电子在核外空间某处单位体积内的概率分布的图形称为电子云图。
(1)点密集的地方,表示电子在此处单位体积内出现的概率大;(2)点稀疏的地方,表示电子在此处单位体积内出现的概率小
电子云图很难绘制,使用不方便
把电子出现概率90%空间圈出来
氢原子核外电子的电子云呈球形对称
请你思考!霓虹灯为什么能够发出五颜六色的光?
霓虹灯自 1910年问世以来,将城市夜景装扮得格外美丽。它之所以能够发出五颜六色的光,其发光机制与氢原子光谱形成的机制基本相同。对霓虹灯而言,灯管中填充的气体不同,在高电压的激发下发出的光的颜色就不同。例如,在灯管中充入氖气,通电后在电场作用下,放电管里氖原子中的电子吸收能量后激发到能量较高的轨道,但处在能量较高轨道上的电子会很快以光的形式辐射能量而跃迁回能量较低的轨道,所发出的光的波长恰好位于可见光区域中的红色波段,所以我们看到的是红色光。
1.下列叙述正确的是( )A.能级就是电子层B.每个能层最多可容纳的电子数是2n2C.同一能层中的不同能级的能量高低相同D.不同能层中的s能级的能量高低相同
2.以下能级符号正确的是( )A.3f D.2f
3.第N能层所含能级数、最多容纳电子数分别为( )A.3、18 B.4、24C.5、32 D.4、32
4.下列现象和应用与电子跃迁无关的是( )A.激光 B.焰色试验C.燃烧放热 D.霓虹灯
鲁科版 (2019)选择性必修2第1节 原子结构模型精品ppt课件: 这是一份鲁科版 (2019)选择性必修2<a href="/hx/tb_c4002595_t3/?tag_id=26" target="_blank">第1节 原子结构模型精品ppt课件</a>,共60页。PPT课件主要包含了第一部分,课堂导入,量子力学的诞生等内容,欢迎下载使用。
高中化学沪科技版(2020)选择性必修21.1 氢原子结构模型精品课件ppt: 这是一份高中化学沪科技版(2020)选择性必修2<a href="/hx/tb_c4036471_t3/?tag_id=26" target="_blank">1.1 氢原子结构模型精品课件ppt</a>,文件包含11氢原子结构模型教学课件pptx、11氢原子结构模型分层作业原卷版docx、11氢原子结构模型分层作业解析版docx等3份课件配套教学资源,其中PPT共44页, 欢迎下载使用。
2021学年第1节 原子结构模型课文配套课件ppt: 这是一份2021学年第1节 原子结构模型课文配套课件ppt,共30页。PPT课件主要包含了学习目标定位,原子轨道等内容,欢迎下载使用。













