






高中化学沪科技版(2020)必修第一册配制一定物质的量浓度的溶液优秀课件ppt
展开配制一定物质的量浓度的溶液
从一烧杯 40% 的NaOH溶液中取出多少溶液才包含有 8 g 的NaOH呢?
对于溶液,量取体积要比称量质量更易操作。
m(溶液) = 20 g
把40 g NaOH固体溶解于水中配成10 L的溶液,请求出
这10 L溶液中NaOH的物质的量是多少?
1升溶液中含有NaOH的质量是多少?
每升溶液中含有NaOH的物质的量是多少?
每升溶液中所含有的NaOH固体的物质的量为:
=1 ml
1升溶液中含有NaOH的质量为: 1 L×40 g/10 L=4 g
ml/L或 ml·L-1
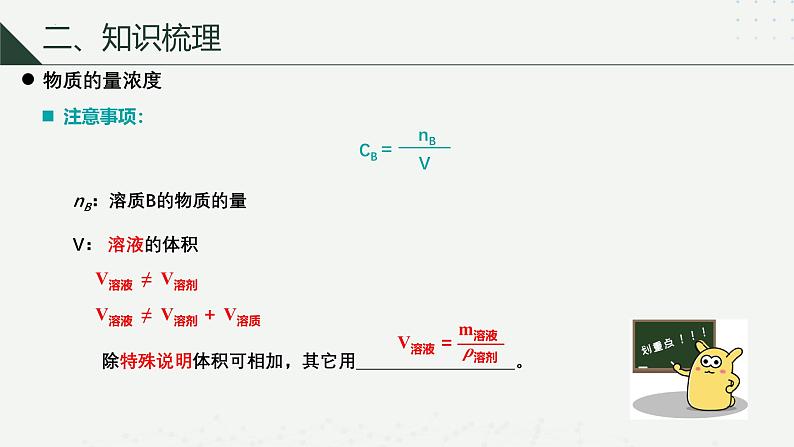
单位体积溶液中所含溶质B的物质的量。
nB:溶质B的物质的量
除特殊说明体积可相加,其它用_____________________。
V溶液 ≠ V溶剂
V溶液 ≠ V溶剂 + V溶质
溶液的体积如何确定呢? 能否用量筒或者烧杯测量溶液的体积?
量筒只适用于量取液体的体积,不适用于配制溶液
适用于配制溶液,但量程的精确度不高
应该选择哪种玻璃仪器呢?
想一想:怎样配制 100mL 1.00ml/L 的NaCl溶液?
精确计量溶液体积的仪器——容量瓶
细颈,梨形,平底玻璃容器,带磨口玻璃塞
温度,容量规格,刻度线
当溶液的凹液面与刻度线相切时,容量瓶中溶液的体积即为容量瓶上所标注的体积。
50 mL,100 mL,250 mL,500 mL,1000 mL
(2)如何检查是否漏水
(1)如何选择规格?若实验时需480 mL一定物质的量浓度的Na2CO3溶液,需选用什么规格的容量瓶?提示 500 mL容量瓶。
选容量瓶——“大而近”原则 ;××mL容量瓶:只能配制与容量瓶规格相同体积的溶液.配制480 mL溶液时选取500 mL容量瓶
使用前要先检查是否漏水
(3)四个“不能”:①不能将固体或浓溶液直接在容量瓶中溶解或稀释;②不能作为反应容器或用来长期贮存溶液;③不能将过冷或过热的溶液转移到容量瓶中,因为容量瓶的容积是在瓶身所标温度下确定的;④不能配制任意体积的溶液,只能配制容量瓶上规定容积的溶液。
如何配制 100mL 1.00ml/L 的NaCl溶液?
(1)计算确定溶质的物质的量:nB=CBV 确定溶质的质量
m = n·M = c·V·M =1.00ml/L×0.1L×58.5g/ml =5.85g
实验步骤:计算→称量→溶解→移液→洗涤→定容→摇匀→装瓶
若配制 80 mL 1.00 ml/L的NaCl溶液,需称量多少克NaCl固体?
没有 80 mL的容量瓶,应选择 100 mL容量瓶,溶液体积以 100 mL计算。
②要用称量纸,如果是NaOH等具有腐蚀性的药品要用表面皿或者烧杯。
【托盘天平使用注意事项】
【拓展】普通电子天平:精确度0.01g或0.001g 分析天平:精确度0.0001g
能否用托盘天平称取5.85 g NaCl固体?
托盘天平精确度为0.1 g,应称取5.9 g NaCl。
将称好的NaCI固体放入烧杯中,加入适量蒸馏水,用玻璃棒搅拌,使NaCl固体全部溶解。
溶解固体,如氢氧化钠,或者稀释浓溶液,如浓硫酸时,要冷却到室温才能转入到容量瓶中。
原因:某些物质在溶解放出大量的热,导致测量不准确
注意:溶解固体,如氢氧化钠,或者稀释浓溶液,如浓硫酸时,要冷却到室温才能转入到容量瓶中。
将烧杯中的溶液沿玻璃棒注入100mL容量瓶,并用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,将洗涤液也都注入容量瓶。轻轻摇动容量瓶,使溶液混合均匀。
玻璃棒作用:引流,避免溶液洒在外面。
洗涤烧杯内壁和玻璃棒沾有少量溶液,保证溶质完全转移至容量瓶,减少误差。
用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,将洗涤液也都注入容量瓶。轻轻摇动容量瓶,使溶液混合均匀。
洗涤烧杯内壁和玻璃棒的目的?
将蒸馏水注入容量瓶,当液面离容量瓶颈部的刻度线1~2cm时,改用胶头滴管滴加蒸馏水至溶液的凹液面与刻度线相切。
如果不小心加水超过刻度线怎么办,能不能拿胶头滴管把多余的水吸出?
易于控制,防止加水超过刻度线
视线要水平,不能俯视或仰视
盖好瓶塞,反复上下颠倒,摇匀。
将配制好的溶液倒入试剂瓶中,并贴好标签。
如果摇匀后发现液面低于刻度线,能不能继续加水?
注意:容量瓶不能长期储存溶液。
实验步骤:计算→称量→溶解→冷却→转移→洗涤→定容→摇匀→装瓶
根据上述公式,由于实验操作不当引起mB或V的变化,会对C造成误差。
(1)使mB增大(或减小)的因素,导致cB偏大(或偏小)。
(2)使V增大(或减小)的因素,导致cB偏小(或偏大)。
容量瓶定容时仰视、俯视对结果的影响(如下图)
①仰视刻度线(如图a):加水量高于基准线(刻度线),溶液体积_________,c_____。②俯视刻度线(如图b):加水量低于基准线(刻度线),溶液体积_________,c_____。
(1)称量过程误差分析
(2)配制过程误差分析。
物质的量浓度有关的几种计算
浓溶液稀释(1)溶质的物质的量不变:c(浓)·V(浓)=c(稀)·V(稀)(2)溶质的质量不变:m(浓)·w(浓)=m(稀)·w(稀)(3)溶液的质量守恒:m(稀)=m(浓)+m(水)
相同溶质两溶液混合(1)溶质的物质的量不变:c1V1+c2V2=c(混)·V(混)(2)溶质的质量不变:m1w1+m2w2=m(混)·w(混)
①若指出不考虑溶液体积改变,可认为是原溶液的体积之和;
生命之水——地表最高浓度白酒
1.实验室进行氯化钠溶液蒸发时,一般有以下操作过程:a.放置酒精灯 b.固定铁圈位置 c.放置蒸发皿d加热搅拌 e.停止加热,余热蒸干 其中正确操作顺序是( ) A. bcdea B. abcde C. bcade D. bacde 【答案】B
2.(1)1 L 0.5 ml·L-1的Al2(SO4)3溶液中n(Al3+)=___________,c(Al3+)=_________,n(SO42-)=_______,c(SO42-))=___________,c[Al2(SO4)3]∶c(Al3+)∶c(SO42-))=__________,由此可知,对于同一溶液中,不同微粒的浓度之比等于____________。(2)某BaCl2溶液中,测得c(Cl-)=0.5 ml·L-1,则c(Ba2+)=____________。(3)下列与0.2 ml·L-1 AlCl3溶液中c(Cl-)相同的是_____。①0.2 ml·L-1 NaCl溶液 ②0.3 ml·L-1 MgCl2溶液 ③0.6 ml·L-1 KCl溶液 ④0.2 ml·L-1 BaCl2溶液
0.25 ml·L-1
3.将2.86 g Na2CO3·10 H2O溶于水配成1 L溶液,则:(1)该溶液的溶质为 ,其物质的量浓度为 ml·L-1。(2)从所配溶液中取出10 mL溶液,取出溶液的物质的量浓度为_____ ml·L-1,Na+的物质的量浓度为 ml·L-1,溶液中溶质的质量为 g。
5.已知V L硫酸铁溶液中含Fe3+m g,则该溶液中Fe3+的物质的量浓度为_____ml·L-1,SO42-的物质的量浓度为 ml·L-1,溶质的物质的量浓度为 ml·L-1。
4.游泳池里的水一般常加适量的硫酸铜,用以杀灭其中的细菌,而对游泳者的身体无害。现取一水样300 mL,经分析其中含有0.019 2 g Cu2+,则水样中硫酸铜的物质的量浓度为 ml·L-1。
6.从1 L 1 ml·L-1氢氧化钠溶液中取出100 mL:(1)取出的这100 mL氢氧化钠溶液的物质的量浓度是 ,含氢氧化钠的质量是 。
解析 m=0.1 L×1 ml·L-1×40 g·ml-1=4.0 g。
(2)若将取出的这100 mL氢氧化钠溶液加水稀释至500 mL,所得溶液的物质的量浓度是 。
7.实验室欲用NaOH固体配制1.0 ml·L-1的NaOH溶液240 mL。(1)配制溶液时,一般有以下几个步骤:①称量 ②计算 ③溶解 ④摇匀 ⑤转移 ⑥洗涤 ⑦定容 ⑧冷却 ⑨摇动其正确的操作顺序为 ______________________。本实验必须用到的仪器有托盘天平、药匙、玻璃棒、量筒、烧杯、 _____________________________。
250 mL容量瓶、胶头滴管
(2)某同学欲称量NaOH固体,他先用托盘天平称量烧杯的质量,天平平衡后的状态如下图所示。烧杯的实际质量为 g,要完成本实验该同学应称取 g NaOH固体。 (3)使用容量瓶前必须进行的一步操作是 。
(4)在配制过程中,其他操作都是正确的,下列操作会引起所配溶液浓度偏大的是 。 A.转移溶液时不慎有少量洒到容量瓶外面B.定容时俯视刻度线C.未冷却到室温就将溶液转移到容量瓶并定容D.定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线
化学必修第一册离子键完整版ppt课件: 这是一份化学必修第一册<a href="/hx/tb_c4025863_t3/?tag_id=26" target="_blank">离子键完整版ppt课件</a>,共25页。PPT课件主要包含了学习要点,课堂导入,知识梳理,思考与交流,钠在氯气中燃烧,离子键,归纳总结,共价键,H2O,CH4等内容,欢迎下载使用。
高中化学沪科技版(2020)必修第一册核外电子排布的规律精品课件ppt: 这是一份高中化学沪科技版(2020)必修第一册<a href="/hx/tb_c4025859_t3/?tag_id=26" target="_blank">核外电子排布的规律精品课件ppt</a>,共18页。PPT课件主要包含了学习要点,课堂导入,知识梳理,电子层,由近到远,由低到高,结构示意图,电子式,由1到8,逐渐减小等内容,欢迎下载使用。
化学必修第一册原子的构成优质ppt课件: 这是一份化学必修第一册<a href="/hx/tb_c4025855_t3/?tag_id=26" target="_blank">原子的构成优质ppt课件</a>,共23页。PPT课件主要包含了学习要点,课堂导入,知识梳理,原子的构成,原子的构成微粒,核外电子数,阳离子,阴离子,微粒符号的含义,几种核素的重要用途等内容,欢迎下载使用。













