






化学苏教版 (2019)专题2 化学反应速率与化学平衡第三单元 化学平衡的移动教学课件ppt
展开
这是一份化学苏教版 (2019)专题2 化学反应速率与化学平衡第三单元 化学平衡的移动教学课件ppt,共40页。
固体或纯液体浓度可视为定值,改变固体或纯液体用量,其浓度保持不变,化学平衡不移动。2.根据浓度商判断反应方向 对于可逆反应mA(g)+nB(g) pC(g)+qD(g),在一定温度下的任意时刻,反应物与生成物的浓度有如下关系。
适当增加相对廉价的反应物或及时分离出生成物,从而提高产物产量、降低成本。
1.其他条件不变时,在有气体参加的可逆反应中,增大压强,平衡向气体总体积减小的方向移
动;减小压强,平衡向气体总体积增大的方向移动。对反应前后气体体积不变的反应,改变容
器体积而改变压强,同等倍数地改变正、逆反应速率,但化学平衡不移动。2.恒温恒容时,充入与该反应无关的气体(如稀有气体),正、逆反应速率不变,平衡不移动;恒
温恒压条件下,充入稀有气体,相当于减小压强,平衡向气体总体积增大的方向移动。
在其他条件不变时,升高温度,平衡向吸热反应方向移动;降低温度,平衡向放热反应方向
移动。
1.平衡移动原理又叫勒夏特列原理:如果改变影响平衡的条件之一(如温度、压强,以及参加
反应的化学物质的浓度),平衡将向着能够减弱这种改变的方向移动。2.平衡移动的结果是“减弱”外界条件的影响,而不是“消除”外界条件的影响,更不是“扭
转”外界条件的影响。
知识辨析1.合成氨工业使用催化剂的目的是使平衡正向移动,提高产率。这种说法对吗?2.平衡正向移动,反应物的转化率一定增大。这种说法对吗?3.改变外界条件使平衡正向移动的原因是v正增大,v逆减小。这种说法对吗?4.反应2NO2(g) N2O4(g)达到平衡时,若缩小反应容器的容积,则c(NO2)减小。这种说法对吗?
一语破的1.不对。使用催化剂不能使平衡正向移动,不能提高产率,只能改变反应速率。2.不对。例如两种气体反应物,增加一种反应物浓度,平衡正向移动,该反应物的转化率减小,
另一种反应物的转化率增大。3.不对。平衡正向移动的原因是v正>v逆,v逆不一定减小。4.不对。缩小反应容器的容积,反应物、生成物的浓度都瞬间增大,然后平衡移动使c(NO2)再
稍减小,但不会比原平衡时小。
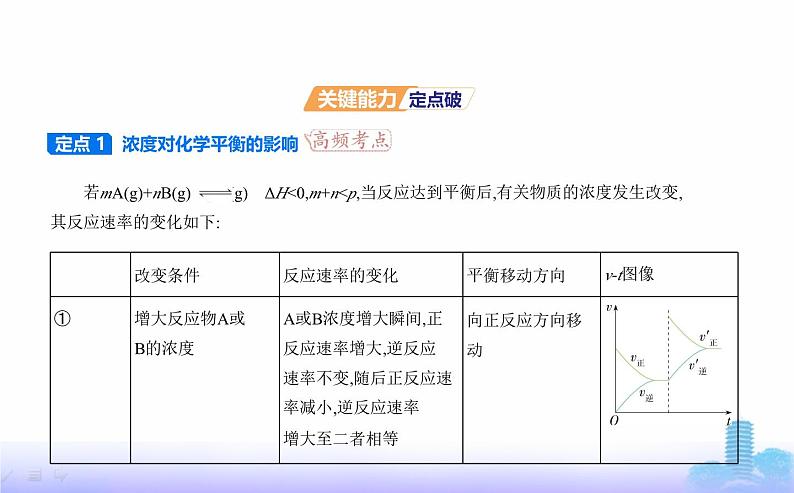
若mA(g)+nB(g) pC(g) ΔH”“
相关课件
这是一份苏教版 (2019)第一单元 化学反应速率教学ppt课件,共33页。
这是一份高中化学苏教版 (2019)选择性必修1第三单元 化学平衡的移动获奖ppt课件,共14页。PPT课件主要包含了等效平衡的概念,随堂训练1,随堂训练2,随堂训练3,习题研究,作业布置等内容,欢迎下载使用。
这是一份高中第三单元 化学平衡的移动获奖ppt课件,共26页。PPT课件主要包含了学习目标,一化学平衡的移动等内容,欢迎下载使用。









