




高中化学人教版 (2019)必修 第一册第三节 化学键备课课件ppt
展开通过Cl2、HCl的形成过程,理解共价键(极性键和非极性键)的形成过程与形成条件。能用电子式表示共价分子的形成过程,能用结构式表示简单的共价分子结构。能从化学键的角度理解化学反应的本质。
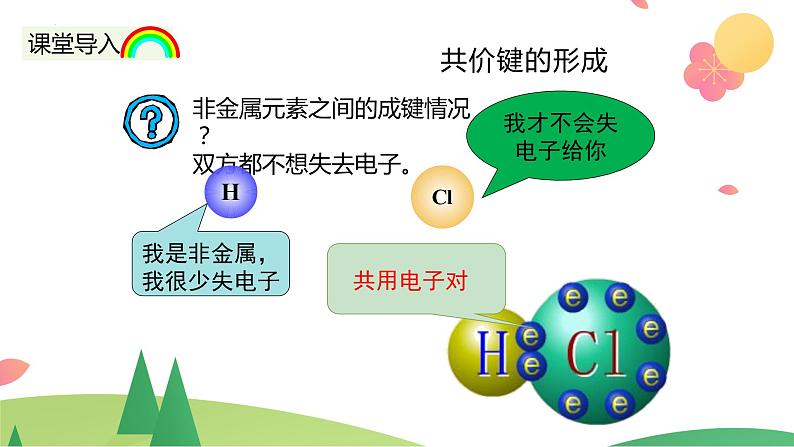
非金属元素之间的成键情况?双方都不想失去电子。
我是非金属,我很少失电子
1.定义:原子之间通过共用电子对所形成的相互作用,叫做共价键。2.成键微粒:原子3.成键本质:共用电子对4.成键条件:一般形成于两个非金属原子之间5.存在:共价键存在于非金属单质的多原子分子中,共价化合物和某些离子化合物中的离子团。
1.概念:原子之间通过共用电子对形成的化合物2.判断:只含有共价键的化合物属于共价化合物(即若存在离子键,一定为离子化合物)3.常见物质类别:(1)非金属氧化物 (2)非金属氢化物(3)酸 (4)绝大部分有机物
1.电子式用电子式表示共价化合物时,不需要加“[ ]”和标电荷。如:Cl2的电子式为 ,HCl的电子式为 ,N2的电子式为 , CO2的电子式为 。
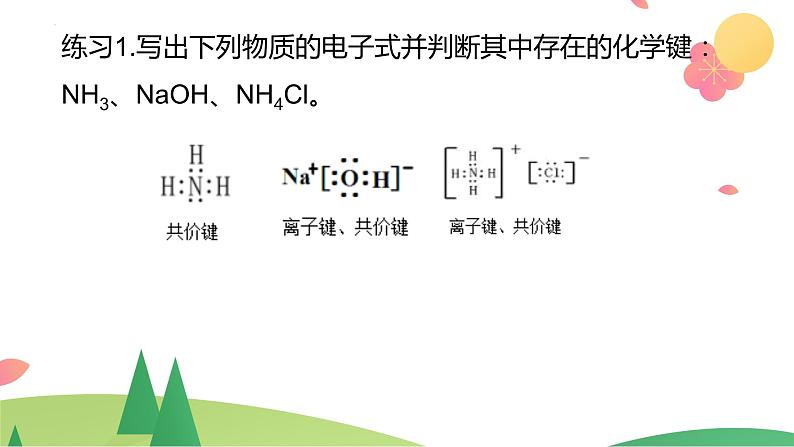
练习1.写出下列物质的电子式并判断其中存在的化学键:NH3、NaOH、NH4Cl。
判断电子式是否正确应注意以下几点:①每个原子周围是否满足了8电子稳定结构(H为2电子稳定结构)共价化合物中8电子稳定结构的判断规律ⅰ.对原子序数不大于5的元素,形成化合物时,一般不可能为8电子稳定结构。如HCl中的H,BeCl2中的Be,BF3中的B等。ⅱ.对原子序数大于5的元素,形成化合物时,若|元素化合价|+原子最外层电子数=8,则该化合物中该元素满足8电子稳定结构;否则不满足。如CO2中的C:|+4|+4=8,满足,O:|-2|+6=8,也满足;PCl5中的P:|+5|+5=10≠8,不满足,Cl:|-1|+7=8,满足。ⅲ。对于共价单质,方法与上面类似,只是将“|元素的化合价|”换成共用电子对数即可。②所标的电子总数是否等于所有原子的最外层电子数之和。
练习2:用电子式表示下列化合物的形成过程CO2 : H2O: NH3 : HCl:
2.结构式在化学上,常用一根短线“—”表示一对共用电子,其余电子一律省去,这样的式子叫做结构式。如:
练习3:下列物质中,(1)F2 (2)O2 (3)NH3 (4)CH4 (5)SO2以极性键结合的( ),以非极性键结合的( )
共价键中元素化合价的体现:形成非极性键的原子间共用电子对不偏移,不会产生化合价的升降;而形成极性键的过程中,电子对偏离的元素化合价升高,电子对偏向的元素化合价降低。
离子化合物和共价化合物的判断方法
五、化学键与化学反应的实质
1.化学键(1)使离子相结合或原子相结合的作用力。(2)分类:化学键2.化学反应的实质:化学反应的实质是旧化学键的断裂和新化学键的形成。
注意:①化学反应的本质是旧化学键的断裂和新化学键的形成,只有化学键的断裂,不一定是化学变化,如熔融NaCl。②物质中不一定都存在化学键,如He等稀有气体分子。③非金属元素的两个原子之间能形成共价键,但多个非金属元素原子间也可能形成离子键,如NH4Cl。
六.分子间作用力和氢键
> > >
冰中氢键的存在使冰的结构中有空隙,造成其密度低于液态水。
1.下列关于共价键的叙述正确的是A.共价键是成键原子间通过一对共用电子对而形成的化学键B.共价键只存在不同种元素的非金属原子之间C.共价键只存在同种元素的非金属原子之间D.共价键是成键原子间通过共用电子对而形成的化学键【答案】D
2.下列关于离子键,共价键的各种叙述中,正确的是( )A.在离子化合物里,只存在离子键,没有共价键B.非极性键只存在于双原子的单质分子中C.在共价化合物分子内,一定不存在离子键D.由不同元素组成的多原子分子里,一定只存在极性键【答案】C
3.已知微粒间的相互作用有以下几种:①离子键 ②极性共价键 ③非极性共价键 ④氢键 ⑤分子间作用力下面是某同学对一些变化过程破坏的微粒间的相互作用的判断:其中判断正确的是A.冰熔化②④⑤ B.氢氧化钠溶于水①②C.氯化氢气体溶于水②④D.干冰升华⑤【答案】D
4.下列物质中是共价化合物的是( )A. B.C. D.【答案】B
5.下列物质中,同时具有离子键和极性共价键的是( )A.NH3 B.NH4Cl C.H2S D.KCl【答案】B
6.书写下列物质电子式①Cl2:_______________; ②CO2:_______________; ③NaOH:_______________;④Na2S:_______________; ⑤H2O2:_______________;
人教版 (2019)必修 第一册第三节 化学键集体备课课件ppt: 这是一份人教版 (2019)必修 第一册<a href="/hx/tb_c162000_t3/?tag_id=26" target="_blank">第三节 化学键集体备课课件ppt</a>,共23页。PPT课件主要包含了考纲要求,实验1氯化钠的形成,概念要点,成键微粒,阴阳离子,键的实质,静电作用力,成键范围,一离子键,二离子化合物等内容,欢迎下载使用。
高中人教版 (2019)第一节 原子结构与元素周期表教案配套ppt课件: 这是一份高中人教版 (2019)<a href="/hx/tb_c161996_t3/?tag_id=26" target="_blank">第一节 原子结构与元素周期表教案配套ppt课件</a>,共22页。PPT课件主要包含了考纲要求,原子的表示,三相对原子质量等内容,欢迎下载使用。
化学必修 第一册第一节 原子结构与元素周期表教案配套课件ppt: 这是一份化学必修 第一册<a href="/hx/tb_c161996_t3/?tag_id=26" target="_blank">第一节 原子结构与元素周期表教案配套课件ppt</a>,共27页。PPT课件主要包含了考纲要求,一原子的构成,原子的构成微粒,核外电子数,阳离子,阴离子,微粒符号的含义,电子层,由近到远,由低到高等内容,欢迎下载使用。














