
化学九年级下册第十单元 酸和碱实验活动6 酸、碱的化学性质教案
展开1、知识与技能
(1)会使用酸碱指示剂判断溶液呈酸性还是碱性。
(2)明确酸碱指示剂(石蕊、酚酞)遇到酸性或者碱性溶液的具体变色情况。
(3)明白变色的是指示剂而不是酸性或者碱性溶液。
(4)知道指示剂变色属于化学变化。
(5)能利用植物花瓣等自制酸碱指示剂,并根据变色情况判断能否作为酸碱指示剂使用。
2、过程与方法
通过一些探究活动,进一步认识与体验科学探究的过程;学会运用酸碱指示剂检验酸性溶液(本课题主要针对针对酸溶液)和碱性溶液(本课题主要针对碱溶液)。
3、情感态度与价值观
(1)使学生感受“从生活走进化学,由化学走向社会”。
(2)使学生认识“从生动的直观到抽象思维,再到实践”的辩证唯物主义的观念”。
(3)通过师生间、学生间合作学习,研究性学习,体验探究成功的乐趣,激发学生的探究欲望。
二、学情分析
九年级学生把化学实验当作一件非常有趣的事情、有强烈的好奇心,且在九年级上学期,学生已经学习了一部分化学知识,具备了一些化学基本技能。而本节课注意联系学生的实际、涉及的实验较多且都是学生操作,刚好符合学生的心理,也能激发起学习兴趣。所以针对这节课,通过小组活动等方式,学生学习起来会很轻松,培养了学生的创新精神和实验操作能力,训练学生进行科学探究的方法。
三、教学重难点
1、教学重点:会使用酸碱指示剂区分酸性溶液和碱性溶液。
2、教学难点:会使用酸碱指示剂区分酸性溶液和碱性溶液。
四、实验准备
教师用具:白醋、炉具清洁剂、紫色石蕊溶液、无色酚酞试剂、烧杯(2只)
学生用具:稀盐酸、稀硫酸、水、氢氧化钠溶液、石灰水、石蕊溶液、无色酚酞试剂、酒精(1:1)、紫甘蓝、红玫瑰、红苋菜、绿萝、小烧杯(4只)、试管(16支)、滴管(2支)、剪刀、纱布(3张)、试管架、研钵(3个)
五、教学过程(第1学时)
【开场布置】同学们喜欢花吗?今天表现最好的三个小组,可以得到今天桌面上的玫瑰花~班长在哪里?班长公正无私吗?好的,这节课会由班长根据各小组的课堂表现评出今天的三个最佳小组。
【引入】视频:宜简苏打水广告(30s)——生活宜简,身体宜碱!
Why?
研究表明:
1、在自然健康的状态,我们身体应当呈现弱碱性。
2、当身体及血液转成偏酸性,久而久之,会导致器官衰竭,而衍生各种疾病。比如,癌!
3、如果不幸患癌,通过调整饮食、规律作息、健康心态,调整体质呈弱碱性,癌症将不会扩展!
怎么自查自己身体是酸性体质还是碱性体质呢?教同学们一个比较粗略的办法:你经常容易感到比较的疲惫吗?
【生答】会
【师述】初三下期了,我相信同学们的疲惫更多的来自于繁重的学业!老师也相信同学们都拥有一个非常健康的身体。
【过渡】在我们生活中也有许多呈酸性或者碱性的液体,你知道哪些?
【生答】酸性的:醋、柠檬汁、苹果汁、汽水;碱性的:肥皂水
【师述】嗯,不错!在我们生活中有这么一些呈酸性和碱性的液体:比如……(PPT展示图片)
如何科学有效的判断溶液到底呈酸性还是碱性还是既不酸也不碱的中性呢?
首先看老师带来的两个演示实验。
【演示实验】白醋(告知是酸性的)中加紫色的石蕊溶液;炉具清洁剂(告知是碱性的)中加入无色的酚酞试剂。
【学生】观看实验!哇!
【师述】是的,炉具清洁剂的碱性是比较强的,是很伤手的,所以今天回家以后你们一定要告诉你们的妈妈,在使用炉具清洁剂的时候一定要记得……
【生答】戴手套
【过渡】嗯,紫色石蕊溶液和无色酚酞在遇到酸性或碱性溶液的时候会表现出一些颜色的改变,具体变色是怎样的,在每个桌面上都有2瓶酸性溶液,分别是稀盐酸和稀硫酸,2瓶碱性溶液——氢氧化钠溶液、石灰水,一瓶中性液体:水,分别向其中加入紫色石蕊溶液 和无色酚酞试剂,观察并最好记录。小组分工合作,4分钟倒计时!
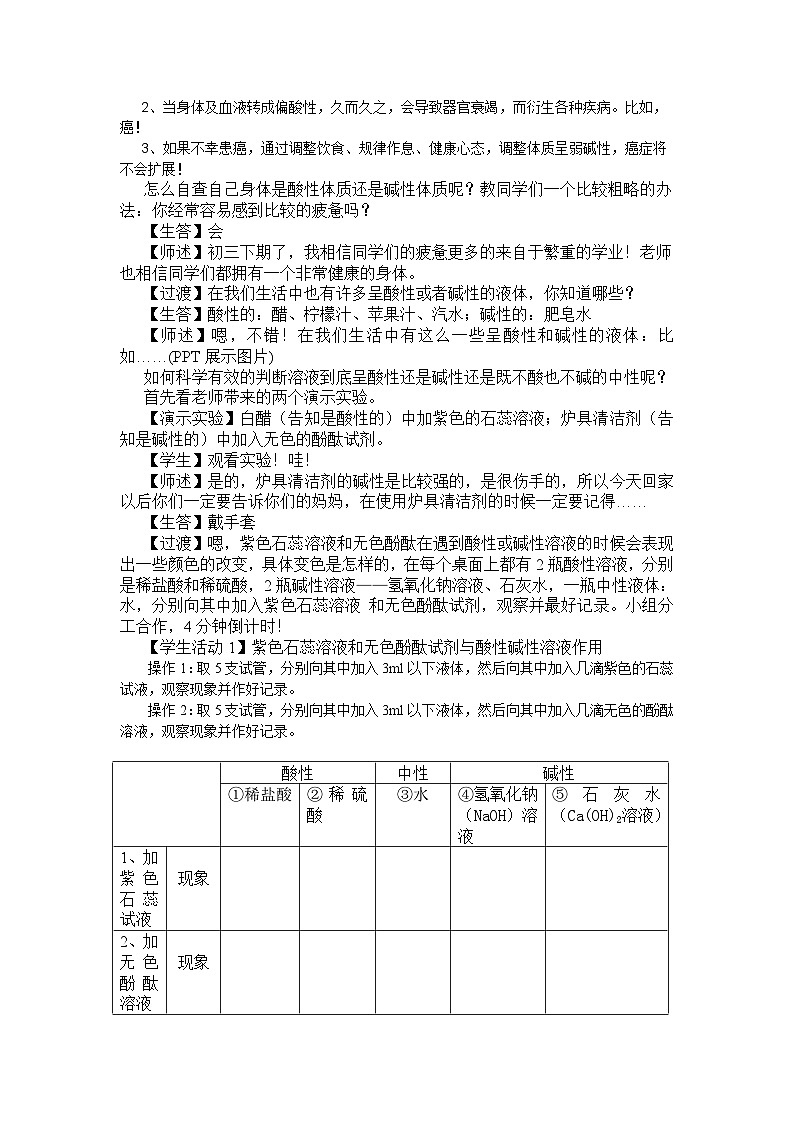
【学生活动1】紫色石蕊溶液和无色酚酞试剂与酸性碱性溶液作用
操作1:取5支试管,分别向其中加入3ml以下液体,然后向其中加入几滴紫色的石蕊试液,观察现象并作好记录。
操作2:取5支试管,分别向其中加入3ml以下液体,然后向其中加入几滴无色的酚酞溶液,观察现象并作好记录。
【小组讨论】通过上述实验,你收获了什么?
【学生小结】
紫色石蕊试液和无色酚酞溶液在酸碱性不同的溶液中可呈现出不同的颜色,由此判断出溶液的酸碱性。
石蕊试液遇酸性变红,遇碱性变蓝,在中性溶液中不变色。酚酞遇碱性溶液变红,在中性和酸性溶液中不变色。
因为现象明显与否的关系,鉴别酸性溶液最好选择石蕊溶液。判断是否为碱性,最好选择酚酞溶液。
【教师补充】变色的是指示剂,而不是酸性或碱性溶液。
……
(后记:在实际课堂中,还出现了有的小组氢氧化钠一加进试管就变红,在学生小结时,认为是试管之前没有洗干净;)
【师述】紫色石蕊溶液和无色酚酞试剂在遇到酸碱性不同的液体时会变成不同的颜色,从而可以用来鉴别溶液到底成酸性、还是碱性,所以我们给他们俩取了一个名副其实的名字——酸碱指示剂。
【学生】齐读——石蕊试液遇酸性变红,遇碱性变蓝,在中性溶液中不变色。酚酞遇碱性溶液变红,在中性和酸性溶液中不变色。
【课堂随练】还记得这个实验吗?学习了今天的内容,你知道A烧杯的液体为什么会变红了吗?
【生答】因为氨水呈碱性
【师述】你知道酸碱指示剂当年是怎么被发现的吗?
【学生】想
【视频】波义耳发现指示剂的故事(3分钟)
【师述】波义耳是个爱花之人,当时他最爱的是紫罗兰花。并通过他最爱的花,发现了石蕊指示剂。
通过波义耳,你有何感想?
【生答】做个有心人,留心身边的变化只有想不到,没有做不到……我也想发明一种指示剂
【师述】嗯,同学们你们今天想不想也当一次波义耳?想不想自己也自制一些酸碱指示剂呢?
【生答】想
【师述】老师在每个小组准备了几种植物,同学们接下来就根据资料上的实验方法自制植物汁液,并判断他们可以作为酸碱指示剂吗?先花1分钟时间了解实验操作。
【学生】了解操作方法
【学生活动2】自制酸碱指示剂(6分钟)
操作:(1)利用桌面上的花瓣或果实(分开实验),先用剪刀剪碎,然后在研钵中捣烂,加入10ml酒精溶液(1:1)浸泡1分钟;
(2)用纱布将浸泡出的汁液挤到小烧杯中,得到指示剂备用;
(3)准备2支试管,分别加入3ml稀盐酸和3ml氢氧化钠溶液,然后分别向其中加入几滴刚刚自制的指示剂,观察并做好记录。(各小组自制2-3种指示剂)
【小组讨论】通过实验,你自制的植物汁液可以充当酸碱指示剂吗?为什么?
【学生小结】
1、红玫瑰遇酸性溶液变红,遇碱性溶液变成 ,效果明显,可以充当酸碱指示剂。
2、紫甘蓝遇酸性溶液变红,遇碱性溶液变为才绿色,效果明显,可以充当酸碱指示剂。
3、红苋菜遇酸性溶液不变色,遇碱性溶液变绿,单向变色,可以充当酸碱指示剂。
(后记:在实际课堂中,还出现了两个小组在利用红玫瑰检验酸碱性溶液时,表现出了两种不一样的颜色的情况,老师及时抓住这一问题问同学们,造成这一不同现象的可能原因是什么?同学们有的答因为浓度不同,有的答玫瑰花品种,生长周期不同)
【过渡】同学们,觉得这节课好玩吗?那你们有没有学到东西呢?请看到资料【我会运用】这一个环节,完成三道题。
【练习】我会运用
1、小明在学习酸碱指示剂与酸碱性溶液作用时,归纳成如右图所示的关系。图中A、B、C、D分别表示指示剂与酸性、碱性溶液作用时所显现出来的颜色,其中表示不正确的是( )
A、紫色 B、蓝色 C、红色 D、无色
2、用酒精溶液浸泡蝴蝶兰花可得到紫色溶液,该溶液遇酸性溶液变红,遇碱性溶液变黄。下列说法不正确的是( )
A、蝴蝶兰花溶液与酸性溶液作用显红色是物理变化。
B、蝴蝶兰花的溶液可用作酸碱指示剂。
C、是指示剂蝴蝶兰花溶液发生的颜色改变。
D、将中性的氯化钠溶液加入蝴蝶兰花溶液中,溶液仍为紫色
3、小红通过查阅资料得知红色、蓝色、紫色的花里含有的色素叫花青素,花青素遇酸性溶液变红,遇碱性溶液变蓝。于是她做了如下实验:把一朵紫色喇叭花泡在肥皂水里,喇叭花很快就变成了蓝色,她又将另一朵喇叭花浸泡在家庭厨房里的某种调味品中,喇叭花变成了红色,请你根据以上实验现象回答:
(1)肥皂水显 性。
(2)小红选用的调味品可能是 。
(3)喇叭花汁液的性质与化学实验室中常用的 的性质相似。
【学后感】通过本节课的探究,你收获了什么?你喜欢这节课吗?为什么呢?
【生答】…………………….
【课后作业】利用今天所学,试验家中常用液体的酸碱性!并拍照发到班级群共享~~
【板书设计】
酸碱指示剂
1、紫色石蕊溶液
2、无色酚酞试剂酸性
中性
碱性
①稀盐酸
②稀硫酸
③水
④氢氧化钠(NaOH)溶液
⑤石灰水(Ca(OH)2溶液)
1、加紫色石蕊试液
现象
2、加无色酚酞溶液
现象
= 1 \* GB3 ①红玫瑰
②红苋菜/紫甘蓝
③绿萝(选做)
加入稀盐酸中
(现象)
加入氢氧化钠溶液中
(现象)
人教版九年级下册实验活动6 酸、碱的化学性质教案及反思: 这是一份人教版九年级下册实验活动6 酸、碱的化学性质教案及反思,共5页。教案主要包含了教学目标,教学重点,教学难点,教材分析,教学过程等内容,欢迎下载使用。
人教版九年级下册实验活动6 酸、碱的化学性质教案设计: 这是一份人教版九年级下册实验活动6 酸、碱的化学性质教案设计,共5页。教案主要包含了酸碱指示剂,指示剂变色规律,自制酸碱指示剂等内容,欢迎下载使用。
人教版九年级下册实验活动6 酸、碱的化学性质教学设计及反思: 这是一份人教版九年级下册实验活动6 酸、碱的化学性质教学设计及反思,共5页。教案主要包含了引入,学习石蕊溶液和酚酞溶液遇酸,课堂小结等内容,欢迎下载使用。














