






- 新教材适用2023_2024学年高中化学第2章海水中的重要元素__钠和氯第3节物质的量第1课时物质的量的单位和摩尔质量课件新人教版必修第一册 课件 0 次下载
- 新教材适用2023_2024学年高中化学第2章海水中的重要元素__钠和氯第3节物质的量第2课时气体摩尔体积课件新人教版必修第一册 课件 0 次下载
- 新教材适用2023_2024学年高中化学第2章海水中的重要元素__钠和氯第3节物质的量第4课时配制一定物质的量浓度的溶液课件新人教版必修第一册 课件 0 次下载
- 新教材适用2023_2024学年高中化学第2章海水中的重要元素__钠和氯阶段重点突破练3课件新人教版必修第一册 课件 0 次下载
- 新教材适用2023_2024学年高中化学第2章海水中的重要元素__钠和氯阶段重点突破练4课件新人教版必修第一册 课件 0 次下载
高中化学人教版 (2019)必修 第一册第二章 海水中的重要元素——钠和氯第三节 物质的量图文ppt课件
展开第3课时 物质的量浓度
1.认识物质的量浓度的含义。2.掌握与物质的量浓度有关的计算。 1.通过对“物质的量浓度”的学习,提升实验探究能力和创新意识。2.通过对“物质的量浓度有关计算”的学习,逐步提升证据推理的能力。
2.溶质的物质的量浓度
特别提醒:①表达式中的体积(V)指溶液的体积,不是溶剂,也不是溶剂和溶质的体积之和。②从一定物质的量浓度的溶液中取出任意体积的溶液,其物质的量浓度、溶质的质量分数均不发生变化。
正误判断(1)将58.5 g NaCl投入1 000 mL水中形成的溶液的物质的量浓度为1 ml·L-1。( )(2)从200 mL 0.1 ml·L-1盐酸中取出50 mL溶液,其物质的量浓度仍为0.1 ml·L-1。( )(3)0.1 ml·L-1的NaCl溶液中含有Na+的物质的量为0.1 ml。( )(4)将25 g CuSO4·5H2O溶于水配成1 L溶液,所得溶液的物质的量浓度为0.1 ml·L-1。( )
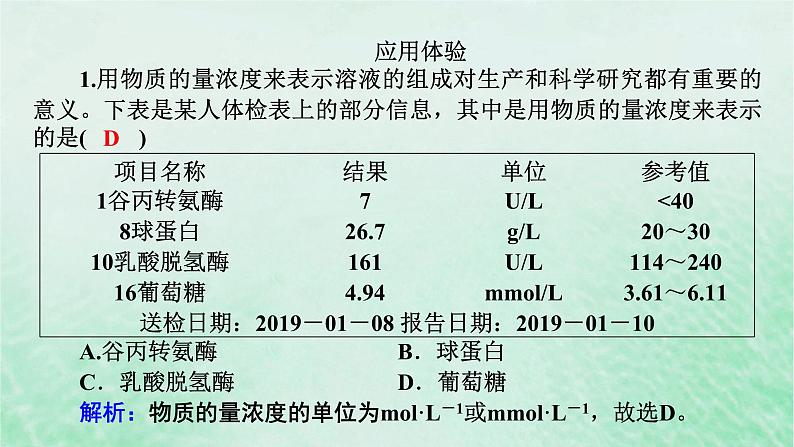
应用体验1.用物质的量浓度来表示溶液的组成对生产和科学研究都有重要的意义。下表是某人体检表上的部分信息,其中是用物质的量浓度来表示的是( )
A.谷丙转氨酶B.球蛋白C.乳酸脱氢酶D.葡萄糖解析:物质的量浓度的单位为ml·L-1或mml·L-1,故选D。
2.2 ml·L-1的KOH溶液100 mL,取出5 mL,这5 mL溶液中K+浓度为( )A.0.2 ml·L-1B.0.4 ml·L-1C.1 ml·L-1D.2 ml·L-1解析:由于溶液具有均一稳定性,取出5 mL溶液,溶液的浓度不变,故5 mL溶液中K+离子浓度为2 ml·L-1,故选D。
3.下列溶液中Cl-的物质的量浓度与100 mL 1 ml·L-1MgCl2溶液中的Cl-物质的量浓度相等的是( )A.150 mL 2 ml·L-1NaCl溶液B.50 mL 2 ml·L-1CaCl2溶液C.150 mL 2 ml·L-1KClO3溶液D.75 mL 1 ml·L-1AlCl3溶液解析:1 ml·L-1 MgCl2溶液中Cl-的物质的量浓度为2 ml·L-1。A项中,NaCl溶液中Cl-浓度为2 ml·L-1,正确;B项中,Cl-浓度为4 ml·L-1,错误;C项中无Cl-,错误;D项中Cl-浓度为3 ml·L-1,错误。
二、与物质的量浓度相关的计算
4.溶液的稀释与混合(1)稀释规律①语言描述:将浓溶液加水稀释,稀释前后溶质的物质的量和质量都保持不变。②公式:c(浓)·V(浓)=c(稀)·V(稀)(2)混合规律①语言描述:同一溶质不同浓度的两溶液相混合,混合后,溶质的总物质的量(或总质量)等于混合前两溶液中溶质的物质的量之和(或质量之和)。②公式:c1·V1+c2·V2=c(混)·V(混)
正误判断(1)溶液的体积越大,浓度越大。( )(2)将1 L 2 ml·L-1的稀硫酸加水稀释到2 L,所得溶液中溶质的物质的量浓度为1 ml·L-1。( )(3)向100 mL 1 ml·L-1K2SO4溶液中加入900 mL水,混合溶液的体积是1 L。( )(4)1 L 1 ml·L-1的KOH溶液中取出100 mL,取出溶液中溶质的质量分数与原溶液相同。( )(5)把100 mL 1 ml·L-1的NaCl溶液加水稀释成200 mL,则稀释后溶液中所含的NaCl的物质的量变为原来的一半。( )
应用体验1.将标准状况下体积为V L的HCl气体溶于1 L水中,所得溶液的密度为ρ g·cm-3,计算溶液的物质的量浓度为____________________。2.从1 L 1 ml·L-1氢氧化钠溶液中取出100 mL,将其加水稀释至500 mL,所得溶液的物质的量浓度是________________________。
3.取100 mL 0.3 ml·L-1和300 mL 0.25 ml·L-1的硫酸混合后再加水至溶液体积为500 mL,所得混合溶液中H+的物质的量浓度是___________ml·L-1。解析:令混合后溶质硫酸的物质的量浓度为a,则:100×10-3L ×0.3 ml·L-1+300×10-3L×0.25 ml·L-1=500×10-3L×a,解得a=0.21 ml·L-1,混合稀释后溶液中c(H+)=2c(H2SO4)=2×0.21 ml·L-1=0.42 ml·L-1。
4.市售浓硫酸中溶质的质量分数为98%,密度为1.84 g·cm-3。计算市售浓硫酸中硫酸的物质的量浓度为__________________________。
18.4 ml·L-1
6.将0.10 ml·L-1氢氧化钠溶液和0.60 ml·L-1氢氧化钠溶液混合成0.20 ml·L-1的氢氧化钠溶液。求两种溶液的体积比为(忽略混合时溶液体积变化)_________。
1.国家对学生健康教育一直很重视,建立学生体质健康档案,确保学生健康成长。下图是某同学体检的血液化验单的一部分:
结果显示葡萄糖为4.2 mml·L-1。表示该体检指标的物理量是( )A.质量分数(w) B.物质的量(n)C.物质的量浓度(c)D.摩尔质量(M)
4.已知硫酸、氨水的密度与所加水量的关系如图所示,现有硫酸与氨水各一份,请根据表中信息,回答下列问题:
化学必修 第一册第三节 物质的量课文内容ppt课件: 这是一份化学必修 第一册第三节 物质的量课文内容ppt课件,共60页。PPT课件主要包含了课前·基础认知,课堂·重难突破,随堂训练,2配制过程,章末知识体系构建等内容,欢迎下载使用。
化学人教版 (2019)第三节 物质的量课堂教学课件ppt: 这是一份化学人教版 (2019)第三节 物质的量课堂教学课件ppt,共33页。PPT课件主要包含了第三节物质的量,玻璃棒,容量瓶,胶头滴管,000mL,③④⑧,①②⑤,随堂演练•知识落实,mL容量瓶等内容,欢迎下载使用。
化学必修 第一册第三节 物质的量示范课课件ppt: 这是一份化学必修 第一册第三节 物质的量示范课课件ppt,共41页。PPT课件主要包含了第三节物质的量,近似相等,不相同或差别较大,不一定,几乎相等,气体摩尔体积,g·mol-1,阿伏加德罗定律,物质的量,mol等内容,欢迎下载使用。













