化学九年级上册课题2 二氧化碳制取的研究教学设计
展开课题2 二氧化碳制取的研究
【学习目标】
1.了解实验室制取二氧化碳的反应原理。
2.探究实验室里制取二氧化碳的装置。
3.了解实验室里制取气体的一般思路和方法。
【学习重点】实验室制取CO2的化学反应原理、实验装置和制取方法;掌握气体制取的一般思路和方法。
【学习难点】从实验室制取气体的思路出发,学习二氧化碳的实验室制取方法和反应原理。
【学习过程】
一、自主学习
1.实验室制取CO2常选用石灰石或大理石和稀盐酸,其反应原理是CaCO3+2HCl===CaCl2+H2O+CO2↑。
2.发生装置的确定取决于反应物的状态和反应条件;CO2气体只能用向上排空气法收集,是因为二氧化碳能溶于水且密度比空气大。
3.CO2的检验与验满:检验CO2气体通常用澄清的石灰水,验满的方法是将燃着的木条放在集气瓶口。
二、新知导学
知识点一 实验室制取二氧化碳的药品和反应原理
【师生合作】探究实验室制取二氧化碳的药品,分小组完成以下三个实验,并完成下表:
信息:选择制取气体时药品的一般原则:较易反应、反应速度适中、生成的气体纯净、易于收集、操作简便、原料廉价易得等。
编号 | 实验 | 现象 | 分析 | 结论(是否适宜制取二氧化碳) |
1 | 碳酸钠+稀盐酸 | 快速产生气泡,反应很快停止 | 反应太剧烈,反应速率太快,不便于收集气体 | 否 |
2 | 石灰石+稀盐酸 | 快速产生气泡,反应很快停止 | 反应速率适中,适合用来制取二氧化碳 | 是 |
3 | 石灰石+稀硫酸 | 快速产生气泡,反应很快停止 | 石灰石与稀硫酸反应会生成微溶的硫酸钙,附着在石灰石表面,阻止反应继续进行 | 否 |
总结 | 实验室制取二氧化碳最理想的药品是大理石(或石灰石)和稀盐酸,反应原理为:CaCO3+2HCl===CaCl2+H2O+CO2↑(用化学方程式表示) | |||
知识点二 实验室制取二氧化碳的装置
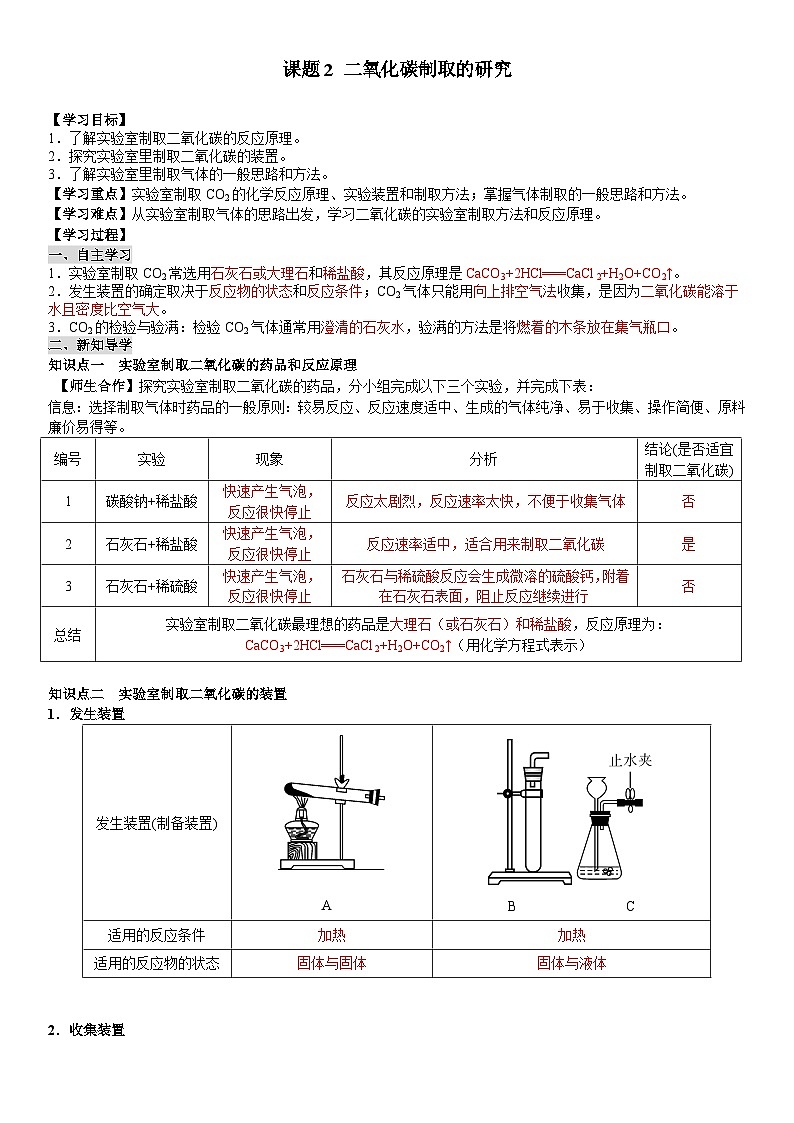
1.发生装置
发生装置(制备装置) | A | B C |
适用的反应条件 | 加热 | 加热 |
适用的反应物的状态 | 固体与固体 | 固体与液体 |
2.收集装置
收集装置 |
| ||
名称 | 排水法 | 向上排空气法 | 向下排空气法 |
适用的气体 | 不易溶于水,不与水反应 | 密度大于空气,不与空气中任何成分反应 | 密度小于空气,不与空气中任何成分反应 |
总结 | 选择收集装置:排水法:考虑气体的溶解性;排空气法:考虑气体的密度 | ||
知识点三 实验室制取二氧化碳的步骤
1.连接仪器,组成装置;
2.检查装置气密性;
3.加入药品(先装入大理石,后加入稀盐酸);
4.制取并收集气体。
5.检验、验满与存放二氧化碳
(1)检验:将气体通入澄清石灰水中,若澄清石灰水变浑浊,证明该气体是CO2。
(2)验满和存放:把燃着的木条放在盛有CO2的集气瓶口,若木条的火焰熄灭,证明气体已经收集满;收集满CO2的集气瓶要用玻璃片盖住并正放在桌面上。
总结: 实验室制取气体的一般思路
1. 确定制取气体的反应原理,即在实验室条件下(如常温、加热、加催化剂等),可用什么药品、通过什么反应来制取这种气体。
2. 确定制取气体时的实验装置,包括气体的发生装置和收集装置。
3. 确定如何验证所制取的气体
三、我的收获
四、当堂检测
1.选择气体收集装置,不必考虑的是( C )
A.溶解性 B.密度
C.气体味道 D.常温下能否与氧气反应
2.实验室制取二氧化碳时,不需选用的仪器有( A )
A.酒精灯 B.导管 C.带孔橡胶塞 D.试管
3.下列不适合作实验室制取二氧化碳的发生装置的是( A )
4.一氧化氮是一种无色、密度比空气略大、难溶于水的气体,在空气中会迅速与氧气反应生成红棕色的二氧化氮气体。实验室收集一氧化氮可采用的方法是( A )
A.排水法 B.排水法或向上排空气法
C.向上排空气法 D.向下排空气法
5.如图是实验室制取二氧化碳的装置。
(1)锥形瓶中加入的药品是大理石(或石灰石)和稀盐酸。
(2)发生反应的化学方程式为CaCO3+2HCl===CaCl2+H2O+CO2↑。
(3)收集气体的方法是向上排空气法。
6.如图所示,图中A是检验CO2的方法,若澄清石灰水变浑浊,证明是CO2;图B是证明CO2是否收集满的方法,若燃着的木条熄灭,证明CO2已收集满。
人教版九年级上册课题2 水的净化教案设计: 这是一份人教版九年级上册课题2 水的净化教案设计,共3页。教案主要包含了学习目标,学习重点,学习难点,学习过程,引导自学,师生合作等内容,欢迎下载使用。
人教版九年级上册课题2 氧气教学设计: 这是一份人教版九年级上册课题2 氧气教学设计,共3页。教案主要包含了学习目标,学习重点,学习难点,学习过程,引导自学,师生合作等内容,欢迎下载使用。
2021学年课题2 二氧化碳制取的研究教学设计: 这是一份2021学年课题2 二氧化碳制取的研究教学设计,共2页。教案主要包含了[学生谈收获体会]等内容,欢迎下载使用。













