


所属成套资源:通用版高考化学一轮复习检测含答案解析
(通用版)高考化学一轮复习检测21 物质结构与性质综合题(含答案解析)
展开
这是一份(通用版)高考化学一轮复习检测21 物质结构与性质综合题(含答案解析),共10页。
高考化学复习检测:21 物质结构与性质综合题1.A、B、C、D、E、F为原子序数依次增大的六种元素,其中A、B、C、D、E为短周期元素,F为第四周期元素,F还是前四周期中电负性最小的元素。 已知:A原子的核外电子数与电子层数相等;B元素原子的核外p电子数比s电子数少1个;C原子的第一至第四电离能为I1=738 kJ·mol-1,I2=1 451 kJ·mol-1,I3=7 733 kJ·mol-1,I4=10 540 kJ·mol-1;D原子核外所有p轨道为全充满或半充满;E元素的族序数与周期序数的差为4。(1)写出E元素在周期表中位置:________;D元素的原子的核外电子排布式:__________________。(2)某同学根据题目信息和掌握的知识分析C的核外电子排布为![]() 该同学所画的轨道式违背了________。(3)已知BA5为离子化合物,写出其电子式:________。(4)DE3中心原子杂化方式为________,其空间构型为_________________。 2.K2Cr2O7是一种常见的强氧化剂,酸性条件下会被还原剂还原成Cr3+。(1)Cr3+能与OH-、CN-形成配合物[Cr(OH)4]-、[Cr(CN)6]3-。①Cr3+的电子排布式可表示为________。②不考虑空间构型,[Cr(OH)4]-的结构可用示意图表示为________(若有配位键,用箭头表示)。③CN-与N2互为等电子体,写出CN-的电子式:________。(2)K2Cr2O7能将乙醇氧化为乙醛,直至乙酸。①乙醛中碳原子的杂化方式有________、________。②乙酸的沸点是117.9 ℃,甲酸甲酯的沸点是31.5 ℃,乙酸的沸点高于甲酸甲酯的沸点的主要原因是________________________。 3.现有部分元素的原子结构特点如表:
该同学所画的轨道式违背了________。(3)已知BA5为离子化合物,写出其电子式:________。(4)DE3中心原子杂化方式为________,其空间构型为_________________。 2.K2Cr2O7是一种常见的强氧化剂,酸性条件下会被还原剂还原成Cr3+。(1)Cr3+能与OH-、CN-形成配合物[Cr(OH)4]-、[Cr(CN)6]3-。①Cr3+的电子排布式可表示为________。②不考虑空间构型,[Cr(OH)4]-的结构可用示意图表示为________(若有配位键,用箭头表示)。③CN-与N2互为等电子体,写出CN-的电子式:________。(2)K2Cr2O7能将乙醇氧化为乙醛,直至乙酸。①乙醛中碳原子的杂化方式有________、________。②乙酸的沸点是117.9 ℃,甲酸甲酯的沸点是31.5 ℃,乙酸的沸点高于甲酸甲酯的沸点的主要原因是________________________。 3.现有部分元素的原子结构特点如表: (1)画出W原子结构示意图_____________________________________。(2)元素X与元素Z相比,非金属性较强的是_____________________,写出一个能表示X、Z非金属性强弱关系的化学反应方程式_________________________________________________________。(3)X、Y、Z、W四种元素形成的一种离子化合物,其水溶液显强酸性,该化合物的化学式为________。(4)元素X和元素Y以原子个数比1∶1化合形成的化合物Q,元素W和元素Y化合形成的化合物M,Q和M的电子总数相等。以M为燃料,Q为氧化剂,可作火箭推进剂,最终生成无毒的、且在自然界中稳定存在的物质,写出该反应的化学方程式__________________________________________。 4.钾和碘的相关化合物在化工、医药、材料等领域有着广泛的应用。回答下列问题:(1)元素K的焰色反应呈紫红色,其中紫色对应的辐射波长为_______nm(填标号)。A.404.4 B.553.5 C.589.2 D.670.8 E.766.5(2)基态K原子中,核外电子占据最高能层的符号是_________,占据该能层电子的电子云轮廓图形状为___________。K和Cr属于同一周期,且核外最外层电子构型相同,但金属K的熔点、沸点等都比金属Cr低,原因是___________________________。(3)X射线衍射测定等发现,I3AsF6中存在
(1)画出W原子结构示意图_____________________________________。(2)元素X与元素Z相比,非金属性较强的是_____________________,写出一个能表示X、Z非金属性强弱关系的化学反应方程式_________________________________________________________。(3)X、Y、Z、W四种元素形成的一种离子化合物,其水溶液显强酸性,该化合物的化学式为________。(4)元素X和元素Y以原子个数比1∶1化合形成的化合物Q,元素W和元素Y化合形成的化合物M,Q和M的电子总数相等。以M为燃料,Q为氧化剂,可作火箭推进剂,最终生成无毒的、且在自然界中稳定存在的物质,写出该反应的化学方程式__________________________________________。 4.钾和碘的相关化合物在化工、医药、材料等领域有着广泛的应用。回答下列问题:(1)元素K的焰色反应呈紫红色,其中紫色对应的辐射波长为_______nm(填标号)。A.404.4 B.553.5 C.589.2 D.670.8 E.766.5(2)基态K原子中,核外电子占据最高能层的符号是_________,占据该能层电子的电子云轮廓图形状为___________。K和Cr属于同一周期,且核外最外层电子构型相同,但金属K的熔点、沸点等都比金属Cr低,原因是___________________________。(3)X射线衍射测定等发现,I3AsF6中存在![]() 离子。
离子。![]() 离子的几何构型为_____________,中心原子的杂化形式为________________。(4)KIO3晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立方结构,边长为a=0.446 nm,晶胞中K、I、O分别处于顶角、体心、面心位置,如图所示。K与O间的最短距离为______nm,与K紧邻的O个数为__________。
离子的几何构型为_____________,中心原子的杂化形式为________________。(4)KIO3晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立方结构,边长为a=0.446 nm,晶胞中K、I、O分别处于顶角、体心、面心位置,如图所示。K与O间的最短距离为______nm,与K紧邻的O个数为__________。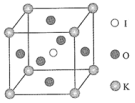 (5)在KIO3晶胞结构的另一种表示中,I处于各顶角位置,则K处于______位置,O处于______位置。 5.磷存在于人体所有细胞中,是维持骨骼和牙齿的必要物质,几乎参与所有生理上的化学反应。回答下列问题:(1)基态P原子的核外电子排布式为____________,有________个未成对电子。(2)磷的一种同素异形体——白磷(P4)的立体构型为________,其键角为________,推测其在CS2中的溶解度________(填“大于”或“小于”)在水中的溶解度。(3)两种三角锥形气态氢化物膦(PH3)和氨(NH3)的键角分别为93.6°和107°,试分析PH3的键角小于NH3的原因_____________________________________________________________________________________________________________________。(4)常温下PCl5是一种白色晶体,其立方晶系晶体结构模型如图甲所示,由A、B两种微粒构成。将其加热至148 ℃熔化,形成一种能导电的熔体。已知A、B两种微粒分别与CCl4、SF6互为等电子体,则A为__________,其中心原子杂化轨道类型为____________,B为____________。(5)磷化硼(BP)是一种超硬耐磨涂层材料,图乙为其立方晶胞,其中的每个原子均满足8电子稳定结构,试判断其熔点________(填“高于”或“低于”)金刚石熔点。
(5)在KIO3晶胞结构的另一种表示中,I处于各顶角位置,则K处于______位置,O处于______位置。 5.磷存在于人体所有细胞中,是维持骨骼和牙齿的必要物质,几乎参与所有生理上的化学反应。回答下列问题:(1)基态P原子的核外电子排布式为____________,有________个未成对电子。(2)磷的一种同素异形体——白磷(P4)的立体构型为________,其键角为________,推测其在CS2中的溶解度________(填“大于”或“小于”)在水中的溶解度。(3)两种三角锥形气态氢化物膦(PH3)和氨(NH3)的键角分别为93.6°和107°,试分析PH3的键角小于NH3的原因_____________________________________________________________________________________________________________________。(4)常温下PCl5是一种白色晶体,其立方晶系晶体结构模型如图甲所示,由A、B两种微粒构成。将其加热至148 ℃熔化,形成一种能导电的熔体。已知A、B两种微粒分别与CCl4、SF6互为等电子体,则A为__________,其中心原子杂化轨道类型为____________,B为____________。(5)磷化硼(BP)是一种超硬耐磨涂层材料,图乙为其立方晶胞,其中的每个原子均满足8电子稳定结构,试判断其熔点________(填“高于”或“低于”)金刚石熔点。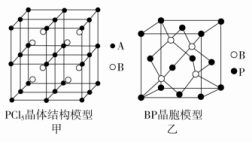 6. (1)周期表前四周期的元素a、b、c、d、e,原子序数依次增大。a的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有1个电子,但次外层有18个电子。b、c、d中第一电离能最大的是________(填元素符号),e的价层电子轨道示意图为________________________。(2)X、Y、Z、R为前四周期元素,且原子序数依次增大。XY2是红棕色气体;X与氢元素可形成XH3;Z基态原子的M层与K层电子数相等;R2+离子的3d轨道中有9个电子。请回答下列问题:Y基态原子的电子排布式是________;Z所在周期中第一电离能最大的主族元素是________。(3)基态硼原子的电子排布式为____________。(4)Cu+基态核外电子排布式为________。(5)Na位于元素周期表第________周期第________族;S的基态原子核外有________个未成对电子;Si的基态原子核外电子排布式为________。 7.原子序数依次增大的四种元素A、B、C、D分别处于第一至第四周期。自然界中存在多种A的化合物,B原子核外电子有6种不同的运动状态,B与C可形成正四面体形分子,D的基态原子的最外能层只有一个电子,其他能层均已充满电子。请回答下列问题:(1)这四种元素中,电负性最大的元素的基态原子的价电子排布图为____________。(2)A与B形成的化合物B2A2中含有的σ键、π键的数目之比为________。(3)B元素可形成多种单质,一种晶体结构如图甲所示,其原子的杂化类型为________;另一种的晶胞如图乙所示,该晶胞的空间利用率为________(保留两位有效数字,=1.732)。
6. (1)周期表前四周期的元素a、b、c、d、e,原子序数依次增大。a的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有1个电子,但次外层有18个电子。b、c、d中第一电离能最大的是________(填元素符号),e的价层电子轨道示意图为________________________。(2)X、Y、Z、R为前四周期元素,且原子序数依次增大。XY2是红棕色气体;X与氢元素可形成XH3;Z基态原子的M层与K层电子数相等;R2+离子的3d轨道中有9个电子。请回答下列问题:Y基态原子的电子排布式是________;Z所在周期中第一电离能最大的主族元素是________。(3)基态硼原子的电子排布式为____________。(4)Cu+基态核外电子排布式为________。(5)Na位于元素周期表第________周期第________族;S的基态原子核外有________个未成对电子;Si的基态原子核外电子排布式为________。 7.原子序数依次增大的四种元素A、B、C、D分别处于第一至第四周期。自然界中存在多种A的化合物,B原子核外电子有6种不同的运动状态,B与C可形成正四面体形分子,D的基态原子的最外能层只有一个电子,其他能层均已充满电子。请回答下列问题:(1)这四种元素中,电负性最大的元素的基态原子的价电子排布图为____________。(2)A与B形成的化合物B2A2中含有的σ键、π键的数目之比为________。(3)B元素可形成多种单质,一种晶体结构如图甲所示,其原子的杂化类型为________;另一种的晶胞如图乙所示,该晶胞的空间利用率为________(保留两位有效数字,=1.732)。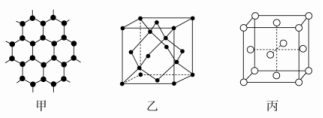 (4)向D的硫酸盐溶液中滴加过量氨水,首先形成蓝色沉淀,继续滴加氨水,沉淀溶解,得到深蓝色的透明溶液。写出沉淀溶解的离子方程式:________________________________。(5)图丙为一个由D元素形成的单质的晶胞,该晶胞“实际”拥有的D原子数目为________。其晶体的堆积模型为____________。此晶胞中的棱长为a cm,D的相对原子质量为M,密度为ρ g·cm-3,则阿伏加德罗常数可表示为________mol-1(用含M、a、ρ的代数式表示)。 8.下图为几种晶体或晶胞的示意图:
(4)向D的硫酸盐溶液中滴加过量氨水,首先形成蓝色沉淀,继续滴加氨水,沉淀溶解,得到深蓝色的透明溶液。写出沉淀溶解的离子方程式:________________________________。(5)图丙为一个由D元素形成的单质的晶胞,该晶胞“实际”拥有的D原子数目为________。其晶体的堆积模型为____________。此晶胞中的棱长为a cm,D的相对原子质量为M,密度为ρ g·cm-3,则阿伏加德罗常数可表示为________mol-1(用含M、a、ρ的代数式表示)。 8.下图为几种晶体或晶胞的示意图: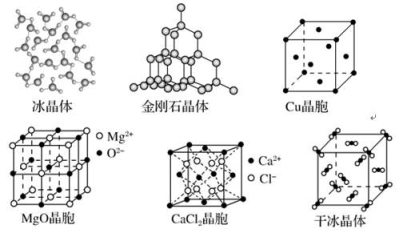 请回答下列问题:(1)上述晶体中,粒子之间以共价键结合形成的晶体是________。(2)冰、金刚石、MgO、CaCl2、干冰5种晶体的熔点由高到低的顺序为___________。(3)NaCl晶胞与MgO晶胞相同,NaCl晶体的晶格能______(填“大于”或“小于”)MgO晶体,原因是________________________________。(4)每个Cu晶胞中实际占有________个Cu原子,CaCl2晶体中Ca2+的配位数为________。 (5)冰的熔点远高于干冰,除H2O是极性分子、CO2是非极性分子外,还有一个重要的原因是___________________________。 9. (1)金属镍及其化合物在合金材料以及催化剂等方面应用广泛。请回答下列问题:①NiO、FeO的晶体结构类型均与氯化钠的相同,Ni2+和Fe2+的离子半径分别为69 pm和78 pm,则熔点FeO________NiO(填“<”或“>”);②铁有δ、γ、α三种同素异形体,各晶胞如下图,则δ、α两种晶胞中铁原子的配位数之比为________。
请回答下列问题:(1)上述晶体中,粒子之间以共价键结合形成的晶体是________。(2)冰、金刚石、MgO、CaCl2、干冰5种晶体的熔点由高到低的顺序为___________。(3)NaCl晶胞与MgO晶胞相同,NaCl晶体的晶格能______(填“大于”或“小于”)MgO晶体,原因是________________________________。(4)每个Cu晶胞中实际占有________个Cu原子,CaCl2晶体中Ca2+的配位数为________。 (5)冰的熔点远高于干冰,除H2O是极性分子、CO2是非极性分子外,还有一个重要的原因是___________________________。 9. (1)金属镍及其化合物在合金材料以及催化剂等方面应用广泛。请回答下列问题:①NiO、FeO的晶体结构类型均与氯化钠的相同,Ni2+和Fe2+的离子半径分别为69 pm和78 pm,则熔点FeO________NiO(填“<”或“>”);②铁有δ、γ、α三种同素异形体,各晶胞如下图,则δ、α两种晶胞中铁原子的配位数之比为________。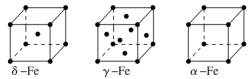 (2)元素金(Au)处于周期表中的第六周期,与Cu同族,一种铜金合金晶体具有立方最密堆积的结构,在晶胞中Cu原子处于面心,Au原子处于顶点位置,则该合金中Cu原子与Au原子数量之比为________;该晶体中,原子之间的强相互作用是________。(3)某钙钛型复合氧化物如图1所示,以A原子为晶胞的顶点,A位可以是Ca、Sr、Ba或Pb,当B位是V、Cr、Mn、Fe等时,这种化合物具有CMR效应。
(2)元素金(Au)处于周期表中的第六周期,与Cu同族,一种铜金合金晶体具有立方最密堆积的结构,在晶胞中Cu原子处于面心,Au原子处于顶点位置,则该合金中Cu原子与Au原子数量之比为________;该晶体中,原子之间的强相互作用是________。(3)某钙钛型复合氧化物如图1所示,以A原子为晶胞的顶点,A位可以是Ca、Sr、Ba或Pb,当B位是V、Cr、Mn、Fe等时,这种化合物具有CMR效应。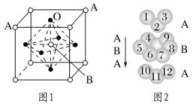 ①用A、B、O表示这类特殊晶体的化学式:__________________。②已知La为+3价,当被钙等二价元素A替代时,可形成复合钙钛矿化合物La1-xAxMnO3(x<0.1),此时一部分锰转变为+4价。导致材料在某一温度附近有反铁磁-铁磁、铁磁-顺磁及金属-半导体的转变,则La1-xAxMnO3中三价锰与四价锰的物质的量之比为________。③下列有关说法正确的是________。 A.镧、锰、氧分别位于周期表f、d、p区 B.氧的第一电离能比氮的第一电离能大 C.锰的电负性为1.59,Cr的电负性为1.66,说明锰的金属性比铬强 D.铬的堆积方式与钾相同,则其堆积方式如图2所示 10.研究发现,在CO2低压合成甲醇反应(CO2+3H2=CH3OH+H2O)中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。回答下列问题:(1)Co基态原子核外电子排布式为_____________。元素Mn与O中,第一电离能较大的是_________,基态原子核外未成对电子数较多的是_________________。(2)CO2和CH3OH分子中C原子的杂化形式分别为__________和__________。(3)在CO2低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为_________________,原因是______________________________。(4)硝酸锰是制备上述反应催化剂的原料,Mn(NO3)2中的化学键除了σ键外,还存在________。(5)MgO具有NaCl型结构(如图),其中阴离子采用面心立方最密堆积方式,X射线衍射实验测得MgO的晶胞参数为a=0.420 nm,则r(O2-)为________nm。MnO也属于NaCl型结构,晶胞参数为a' =0.448 nm,则r(Mn2+)为________nm。
①用A、B、O表示这类特殊晶体的化学式:__________________。②已知La为+3价,当被钙等二价元素A替代时,可形成复合钙钛矿化合物La1-xAxMnO3(x<0.1),此时一部分锰转变为+4价。导致材料在某一温度附近有反铁磁-铁磁、铁磁-顺磁及金属-半导体的转变,则La1-xAxMnO3中三价锰与四价锰的物质的量之比为________。③下列有关说法正确的是________。 A.镧、锰、氧分别位于周期表f、d、p区 B.氧的第一电离能比氮的第一电离能大 C.锰的电负性为1.59,Cr的电负性为1.66,说明锰的金属性比铬强 D.铬的堆积方式与钾相同,则其堆积方式如图2所示 10.研究发现,在CO2低压合成甲醇反应(CO2+3H2=CH3OH+H2O)中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。回答下列问题:(1)Co基态原子核外电子排布式为_____________。元素Mn与O中,第一电离能较大的是_________,基态原子核外未成对电子数较多的是_________________。(2)CO2和CH3OH分子中C原子的杂化形式分别为__________和__________。(3)在CO2低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为_________________,原因是______________________________。(4)硝酸锰是制备上述反应催化剂的原料,Mn(NO3)2中的化学键除了σ键外,还存在________。(5)MgO具有NaCl型结构(如图),其中阴离子采用面心立方最密堆积方式,X射线衍射实验测得MgO的晶胞参数为a=0.420 nm,则r(O2-)为________nm。MnO也属于NaCl型结构,晶胞参数为a' =0.448 nm,则r(Mn2+)为________nm。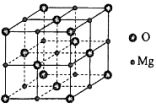
答案解析1.答案为:(1)第三周期ⅦA族 1s22s22p63s23p3(2)能量最低原理(3)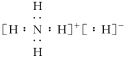 ;(4)sp3 三角锥形解析:(1)由题意分析知F为K,A为H,B为N;由电离能知C的常见化合价为+2价,为Mg,D为P,E为Cl。(2)原子的核外电子分能级排布,按构造原理先排能量低的能级,再排能量高的能级,遵循能量最低原理时,该原子才最稳定。该同学未排满3s能级就排3p能级,违背了能量最低原理。(3)NH5为离子化合物,则为铵盐,存在NH和H-。(4)PCl3中心原子P上的价层电子对=3+(5-3×1)=4,杂化类型为sp3杂化;存在一个孤电子对,故分子构型为三角锥形。 2.答案为:(1)①1s22s22p63s23p63d3或[Ar]3d3 ②
;(4)sp3 三角锥形解析:(1)由题意分析知F为K,A为H,B为N;由电离能知C的常见化合价为+2价,为Mg,D为P,E为Cl。(2)原子的核外电子分能级排布,按构造原理先排能量低的能级,再排能量高的能级,遵循能量最低原理时,该原子才最稳定。该同学未排满3s能级就排3p能级,违背了能量最低原理。(3)NH5为离子化合物,则为铵盐,存在NH和H-。(4)PCl3中心原子P上的价层电子对=3+(5-3×1)=4,杂化类型为sp3杂化;存在一个孤电子对,故分子构型为三角锥形。 2.答案为:(1)①1s22s22p63s23p63d3或[Ar]3d3 ②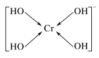 ;③
;③![]() (2)①sp2 sp3 ②乙酸分子间存在氢键解析:(1)①铬为24号元素,铬元素失去3个电子变成Cr3+,所以Cr3+核外有21个电子,根据构造原理知,该离子核外电子排布式为1s22s22p63s23p63d3。②[Cr(OH)4]-中的Cr3+与4个OH-形成配位键,可表示为
(2)①sp2 sp3 ②乙酸分子间存在氢键解析:(1)①铬为24号元素,铬元素失去3个电子变成Cr3+,所以Cr3+核外有21个电子,根据构造原理知,该离子核外电子排布式为1s22s22p63s23p63d3。②[Cr(OH)4]-中的Cr3+与4个OH-形成配位键,可表示为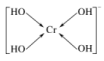 。③根据氮气分子的电子式写出CN-的电子式,且CN-是离子,符合离子电子式的书写规则,所以其电子式为
。③根据氮气分子的电子式写出CN-的电子式,且CN-是离子,符合离子电子式的书写规则,所以其电子式为![]() 。(2)①乙醛中甲基上的碳原子含有四个共价单键,所以甲基上碳原子采用sp3杂化,醛基上碳原子含有3个共价单键,所以醛基上碳原子采用sp2杂化。 3.答案为:(1)
。(2)①乙醛中甲基上的碳原子含有四个共价单键,所以甲基上碳原子采用sp3杂化,醛基上碳原子含有3个共价单键,所以醛基上碳原子采用sp2杂化。 3.答案为:(1)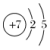 (2)X(或氧) 2H2S+O22H2O+2S↓(其他合理答案也可)(3)NH4HSO4(4)N2H4+2H2O2N2+4H2O解析:由表中信息可确定X为O、Y为H、Z为S、W为N。 4.参考答案:(1)A;(2)N 球形 K的原子半径较大且价电子数较少,金属键较弱(3)V形 sp3 (4)0.315 12 (5)体心 棱心解析:(1)紫色波长400 nm~435 nm,因此选项A正确;(2)K位于第四周期IA族,电子占据最高能层是第四层,即N层,最后一个电子填充在s能级上,电子云轮廓图为球形;K的原子半径大于Cr的半径,且价电子数较少,金属键较弱,因此K的熔点、沸点比Cr低;(3)
(2)X(或氧) 2H2S+O22H2O+2S↓(其他合理答案也可)(3)NH4HSO4(4)N2H4+2H2O2N2+4H2O解析:由表中信息可确定X为O、Y为H、Z为S、W为N。 4.参考答案:(1)A;(2)N 球形 K的原子半径较大且价电子数较少,金属键较弱(3)V形 sp3 (4)0.315 12 (5)体心 棱心解析:(1)紫色波长400 nm~435 nm,因此选项A正确;(2)K位于第四周期IA族,电子占据最高能层是第四层,即N层,最后一个电子填充在s能级上,电子云轮廓图为球形;K的原子半径大于Cr的半径,且价电子数较少,金属键较弱,因此K的熔点、沸点比Cr低;(3)![]() 与OF2互为等电子体,OF2属于V形,因此
与OF2互为等电子体,OF2属于V形,因此![]() 几何构型为V形,其中心原子的杂化类型为sp3;(4)根据晶胞结构,K与O间的最短距离是面对角线的一半,即为
几何构型为V形,其中心原子的杂化类型为sp3;(4)根据晶胞结构,K与O间的最短距离是面对角线的一半,即为![]() nm=0.315nm,根据晶胞的结构,距离K最近的O的个数为12个;(5)根据KIO3的化学式,以及晶胞结构,可知K处于体心,O处于棱心。 5.答案为:(1)1s22s22p63s23p3 3(2)正四面体形 60° 大于(3)电负性N强于P,中心原子的电负性越大,成键电子对离中心原子越近,成键电子对之间距离越小,成键电子对之间的排斥力增大,键角变大(4)PCl sp3 PCl(5)低于解析:(1)基态P原子核外有15个电子,其核外电子排布式为1s22s22p63s23p3,有3个未成对电子。(2)P4为正四面体结构,其键角为60°,P4为非极性分子,根据“相似相溶”原理,P4易溶于非极性溶剂CS2,难溶于极性溶剂H2O。(4)根据题意可知,PCl5为离子晶体,则晶体中存在阴、阳离子,A与CCl4互为等电子体,则A为PCl,根据价电子对互斥理论,其采用sp3杂化,B与SF6互为等电子体,则B为PCl。(5)BP与金刚石都是原子晶体,由于C—C键的键长比B—P键短,则C—C键的键能更大,故金刚石的熔点高于BP。 6.答案为:(1)N
nm=0.315nm,根据晶胞的结构,距离K最近的O的个数为12个;(5)根据KIO3的化学式,以及晶胞结构,可知K处于体心,O处于棱心。 5.答案为:(1)1s22s22p63s23p3 3(2)正四面体形 60° 大于(3)电负性N强于P,中心原子的电负性越大,成键电子对离中心原子越近,成键电子对之间距离越小,成键电子对之间的排斥力增大,键角变大(4)PCl sp3 PCl(5)低于解析:(1)基态P原子核外有15个电子,其核外电子排布式为1s22s22p63s23p3,有3个未成对电子。(2)P4为正四面体结构,其键角为60°,P4为非极性分子,根据“相似相溶”原理,P4易溶于非极性溶剂CS2,难溶于极性溶剂H2O。(4)根据题意可知,PCl5为离子晶体,则晶体中存在阴、阳离子,A与CCl4互为等电子体,则A为PCl,根据价电子对互斥理论,其采用sp3杂化,B与SF6互为等电子体,则B为PCl。(5)BP与金刚石都是原子晶体,由于C—C键的键长比B—P键短,则C—C键的键能更大,故金刚石的熔点高于BP。 6.答案为:(1)N ![]() (2)1s22s22p4 Cl(3)1s22s22p1(4)1s22s22p63s23p63d10(或[Ar]3d10)(5)三 ⅠA 2 1s22s22p63s23p2(或[Ne]3s23p2)解析:(1)由题意推出a、b、c、d、e依次是H、N、O、S、Cu。第一电离能同周期从左向右呈逐渐增大趋势,由于N的2p轨道处于半满,较稳定,所以第一电离能N>O。同主族从上到下,第一电离能逐渐减小,故O>S。Cu的价层电子轨道示意图为
(2)1s22s22p4 Cl(3)1s22s22p1(4)1s22s22p63s23p63d10(或[Ar]3d10)(5)三 ⅠA 2 1s22s22p63s23p2(或[Ne]3s23p2)解析:(1)由题意推出a、b、c、d、e依次是H、N、O、S、Cu。第一电离能同周期从左向右呈逐渐增大趋势,由于N的2p轨道处于半满,较稳定,所以第一电离能N>O。同主族从上到下,第一电离能逐渐减小,故O>S。Cu的价层电子轨道示意图为![]() 。(2)根据题给信息,可以推断X为N,Y为O,Z为Mg,R为Cu。O原子核外有8个电子,基态原子的核外电子排布式为1s22s22p4。Mg位于第三周期,第三周期中第一电离能最大的主族元素为Cl。(5)钠位于第三周期第ⅠA 族;S的基态原子电子排布式为1s22s22p63s23p4,其中3p轨道示意图为
。(2)根据题给信息,可以推断X为N,Y为O,Z为Mg,R为Cu。O原子核外有8个电子,基态原子的核外电子排布式为1s22s22p4。Mg位于第三周期,第三周期中第一电离能最大的主族元素为Cl。(5)钠位于第三周期第ⅠA 族;S的基态原子电子排布式为1s22s22p63s23p4,其中3p轨道示意图为![]() ,有2个未成对电子。 7.答案为:(1)
,有2个未成对电子。 7.答案为:(1)![]() (2)3∶2(3)sp2 34%(4)Cu(OH)2+4NH3·H2O===[Cu(NH3)4]2++2OH-+4H2O(5)4 面心立方最密堆积 解析:A为第一周期元素,且自然界中存在多种A的化合物,则A为氢元素;B原子核外电子有6种不同的运动状态,即核外有6个电子,则B为碳元素;D的基态原子的最外能层只有一个电子,其他能层均已充满电子,D原子外围电子排布式为3d104s1,则D为铜元素;结合原子序数大小顺序可知,C只能处于第三周期,B与C可形成正四面体形分子,则C为氯元素。(1)四种元素中电负性最大的是Cl元素,其基态原子的价电子数为7,其基态原子的价电子排布图为
(2)3∶2(3)sp2 34%(4)Cu(OH)2+4NH3·H2O===[Cu(NH3)4]2++2OH-+4H2O(5)4 面心立方最密堆积 解析:A为第一周期元素,且自然界中存在多种A的化合物,则A为氢元素;B原子核外电子有6种不同的运动状态,即核外有6个电子,则B为碳元素;D的基态原子的最外能层只有一个电子,其他能层均已充满电子,D原子外围电子排布式为3d104s1,则D为铜元素;结合原子序数大小顺序可知,C只能处于第三周期,B与C可形成正四面体形分子,则C为氯元素。(1)四种元素中电负性最大的是Cl元素,其基态原子的价电子数为7,其基态原子的价电子排布图为![]() 。(2)H与C形成的化合物B2A2为C2H2,其结构式是H—C≡C—H,C2H2分子中含有3个σ键、2个π键,则σ键、π键数目之比为3∶2。(3)图甲是石墨的层状晶体结构,每个C原子与另外3个C原子相连,则C原子采取sp2杂化;图乙是金刚石的晶胞结构,晶胞含8个碳原子,若晶胞参数为a cm,C原子半径为r cm,体对角线的长度为4个碳原子的直径,则有:8r=a,该晶胞的空间利用率为×100%=×100%≈34%。(5)图丙为一个由D元素形成的单质的晶胞,该晶胞“实际”拥有的D原子数为8×+6×=4。晶体的堆积模型为面心立方最密堆积。此晶胞中的棱长为a cm,D的相对原子质量为M,密度为ρ g·cm-3,则有ρ== g·cm-3,故阿伏加德罗常数可表示为NA= mol-1。 8.答案为:(1)金刚石晶体(2)金刚石>MgO>CaCl2>冰>干冰(3)小于 MgO晶体中离子的电荷数大于NaCl晶体中离子电荷数;且r(Mg2+)<r(Na+)、r(O2-)<r(Cl-)(4)4 8;(5)H2O分子之间能形成氢键解析:(2)离子晶体的熔点与离子半径及离子所带电荷数有关,离子半径越小,离子所带电荷数越大,则离子晶体熔点越高。金刚石是原子晶体,熔点最高,冰、干冰均为分子晶体,冰中存在氢键,冰的熔点高于干冰。(4)铜晶胞实际占有铜原子数用均摊法分析:8×+6×=4,氯化钙类似于氟化钙,Ca2+的配位数为8,Cl-配位数为4。 9.答案为:(1)①< ②4∶3(2)3∶1 金属键(3)①ABO3 ② ③AC解析:(1)①NiO、FeO均为离子晶体,Ni2+的离子半径小于Fe2+离子半径,因此熔点:FeO<NiO ②δ-Fe是体心立方堆积,配位数是8,α-Fe是简单立方堆积,配位数为6,则δ、α两种晶胞中Fe的配位数比为4∶3。(2)晶胞中Cu原子数=6×=3,Au原子数=8×=1。(3)①由图1可知:A为8×=1个,B位为体心,含有1个,O为6×=3,则化学式为ABO3; ②设La1-xAxMnO3中三价锰与四价锰的物质的量分别为m和n,则有 解之得m=1-x,n=x,则三价锰与四价锰的物质的量之比为; ③B项,N的核外电子排布中2p轨道半充满,第一电离能N>O,B错误;D项,图中堆积方式为镁型,故D项错误,A、C正确。 10.答案为:(1)1s22s22p63s23p63d74s2或[Ar]3d74s2 O Mn;(2)sp sp3(3)H2O>CH3OH>CO2>H2 H2O与CH3OH均为极性分子,H2O中氢键比甲醇多;CO2与H2均为非极性分子,CO2分子量较大、范德华力较大;(4)离子键和π键(或
。(2)H与C形成的化合物B2A2为C2H2,其结构式是H—C≡C—H,C2H2分子中含有3个σ键、2个π键,则σ键、π键数目之比为3∶2。(3)图甲是石墨的层状晶体结构,每个C原子与另外3个C原子相连,则C原子采取sp2杂化;图乙是金刚石的晶胞结构,晶胞含8个碳原子,若晶胞参数为a cm,C原子半径为r cm,体对角线的长度为4个碳原子的直径,则有:8r=a,该晶胞的空间利用率为×100%=×100%≈34%。(5)图丙为一个由D元素形成的单质的晶胞,该晶胞“实际”拥有的D原子数为8×+6×=4。晶体的堆积模型为面心立方最密堆积。此晶胞中的棱长为a cm,D的相对原子质量为M,密度为ρ g·cm-3,则有ρ== g·cm-3,故阿伏加德罗常数可表示为NA= mol-1。 8.答案为:(1)金刚石晶体(2)金刚石>MgO>CaCl2>冰>干冰(3)小于 MgO晶体中离子的电荷数大于NaCl晶体中离子电荷数;且r(Mg2+)<r(Na+)、r(O2-)<r(Cl-)(4)4 8;(5)H2O分子之间能形成氢键解析:(2)离子晶体的熔点与离子半径及离子所带电荷数有关,离子半径越小,离子所带电荷数越大,则离子晶体熔点越高。金刚石是原子晶体,熔点最高,冰、干冰均为分子晶体,冰中存在氢键,冰的熔点高于干冰。(4)铜晶胞实际占有铜原子数用均摊法分析:8×+6×=4,氯化钙类似于氟化钙,Ca2+的配位数为8,Cl-配位数为4。 9.答案为:(1)①< ②4∶3(2)3∶1 金属键(3)①ABO3 ② ③AC解析:(1)①NiO、FeO均为离子晶体,Ni2+的离子半径小于Fe2+离子半径,因此熔点:FeO<NiO ②δ-Fe是体心立方堆积,配位数是8,α-Fe是简单立方堆积,配位数为6,则δ、α两种晶胞中Fe的配位数比为4∶3。(2)晶胞中Cu原子数=6×=3,Au原子数=8×=1。(3)①由图1可知:A为8×=1个,B位为体心,含有1个,O为6×=3,则化学式为ABO3; ②设La1-xAxMnO3中三价锰与四价锰的物质的量分别为m和n,则有 解之得m=1-x,n=x,则三价锰与四价锰的物质的量之比为; ③B项,N的核外电子排布中2p轨道半充满,第一电离能N>O,B错误;D项,图中堆积方式为镁型,故D项错误,A、C正确。 10.答案为:(1)1s22s22p63s23p63d74s2或[Ar]3d74s2 O Mn;(2)sp sp3(3)H2O>CH3OH>CO2>H2 H2O与CH3OH均为极性分子,H2O中氢键比甲醇多;CO2与H2均为非极性分子,CO2分子量较大、范德华力较大;(4)离子键和π键(或![]() 键);(5)0.148 0.076解析:(1)Co是27号元素,位于元素周期表第4周期第VIII族,其基态原子核外电子排布式为1s22s22p63s23p63d74s2或[Ar]3d74s2。元素Mn与O中,由于O元素是非金属元素而Mn是金属元素,所以第一电离能较大的是O。O元素的基态原子价电子排布式为2s22p4,所以其核外未成对电子数是2,而Mn元素的基态原子价电子排布式为3d54s2,所以其核外未成对电子数是5,因此核外未成对电子数较多的是Mn。(2)CO2和CH3OH的中心原子C原子的价层电子对数分别为2和4,所以CO2和CH3OH分子中C原子的杂化形式分别为sp和sp3。(3)在CO2低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为H2O>CH3OH>CO2>H2,原因是常温下水和甲醇是液体而二氧化碳和氢气是气体,液体的沸点高于气体;H2O与CH3OH均为极性分子,H2O中氢键比甲醇多,所以水的沸点高于甲醇;CO2与H2均为非极性分子,CO2分子量较大、范德华力较大,所以CO2的沸点较高。(4)硝酸锰是离子化合物,硝酸根和锰离子之间形成离子键,硝酸根中N原子与3个氧原子形成 3个σ键,硝酸根中有一个氮氧双键,所以还存在π键。(5)因为O2-是面心立方最密堆积方式,面对角线是O2-半径的4倍,即4r(O2-)=
键);(5)0.148 0.076解析:(1)Co是27号元素,位于元素周期表第4周期第VIII族,其基态原子核外电子排布式为1s22s22p63s23p63d74s2或[Ar]3d74s2。元素Mn与O中,由于O元素是非金属元素而Mn是金属元素,所以第一电离能较大的是O。O元素的基态原子价电子排布式为2s22p4,所以其核外未成对电子数是2,而Mn元素的基态原子价电子排布式为3d54s2,所以其核外未成对电子数是5,因此核外未成对电子数较多的是Mn。(2)CO2和CH3OH的中心原子C原子的价层电子对数分别为2和4,所以CO2和CH3OH分子中C原子的杂化形式分别为sp和sp3。(3)在CO2低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为H2O>CH3OH>CO2>H2,原因是常温下水和甲醇是液体而二氧化碳和氢气是气体,液体的沸点高于气体;H2O与CH3OH均为极性分子,H2O中氢键比甲醇多,所以水的沸点高于甲醇;CO2与H2均为非极性分子,CO2分子量较大、范德华力较大,所以CO2的沸点较高。(4)硝酸锰是离子化合物,硝酸根和锰离子之间形成离子键,硝酸根中N原子与3个氧原子形成 3个σ键,硝酸根中有一个氮氧双键,所以还存在π键。(5)因为O2-是面心立方最密堆积方式,面对角线是O2-半径的4倍,即4r(O2-)=![]() a,解得r(O2-)=
a,解得r(O2-)=![]() nm=0.148nm;MnO也属于NaCl型结构,根据晶胞的结构,晶胞参数=2 r(O2-)+2 r(Mn2+),则r(Mn2+)=(0.448 nm-2×0.148 nm)/2=0.076nm。
nm=0.148nm;MnO也属于NaCl型结构,根据晶胞的结构,晶胞参数=2 r(O2-)+2 r(Mn2+),则r(Mn2+)=(0.448 nm-2×0.148 nm)/2=0.076nm。
相关试卷
这是一份新高考化学二轮复习检测卷专题16 物质结构与性质综合题(含解析),共16页。试卷主要包含了5ml,转移电子数为0等内容,欢迎下载使用。
这是一份(通用版)高考化学一轮复习检测23 有机化学基础 综合题(含答案解析),共17页。
这是一份(通用版)高考化学一轮复习检测20 物质结构与性质(含答案解析),共10页。试卷主要包含了5NA等内容,欢迎下载使用。









