

2023年陕西省西安市莲湖区中考模拟化学试题(含解析)
展开2023年陕西省西安市莲湖区中考模拟化学试题
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.分类观念是化学学科核心素养的重要组成部分。下列物质属于盐的是
A.溶液 B. C. D.
2.化学促进了科技进步和社会发展。下列叙述中不正确的是
A.《神农本草经》中记载的“石胆能化铁为铜”这一变化属于物理变化
B.用镁铝合金代替钢材制造飞船零部件,可以减轻飞船自身的重量
C.氢气属于新型能源,用作发射卫星的燃料可以防止环境污染
D.使用跨临界直冷制冰,是利用了的某些物理性质
3.下列实验操作正确的是
A.收集氧气 B.加热溶液
C.二氧化碳的验满 D.蒸发食盐水
4.符号表征是化学学科特有的表示方法。对下面化学符号所表示的含义理解正确的是
① ② ③ ④
A.①只能表示金属钠 B.②表示两个二氧化碳分子
C.③表示铁元素的化合价为价 D.④中甲乙两种微粒属于同种元素的不同离子
5.劳动开创未来。对下列劳动项目中所涉及的化学原理解释不合理的是
选项
劳动项目
解释
A
环保工程师用熟石灰处理酸性废水
熟石灰具有碱性
B
面包师用小苏打作发泡剂烘焙面包
可与酸反应
C
食品工业常用氮气作为食品保鲜剂
氮气性质稳定,且不能供给微生物呼吸
D
技术人员开发高端耐腐蚀镀铝钢板
铝能形成致密氧化膜
A.A B.B C.C D.D
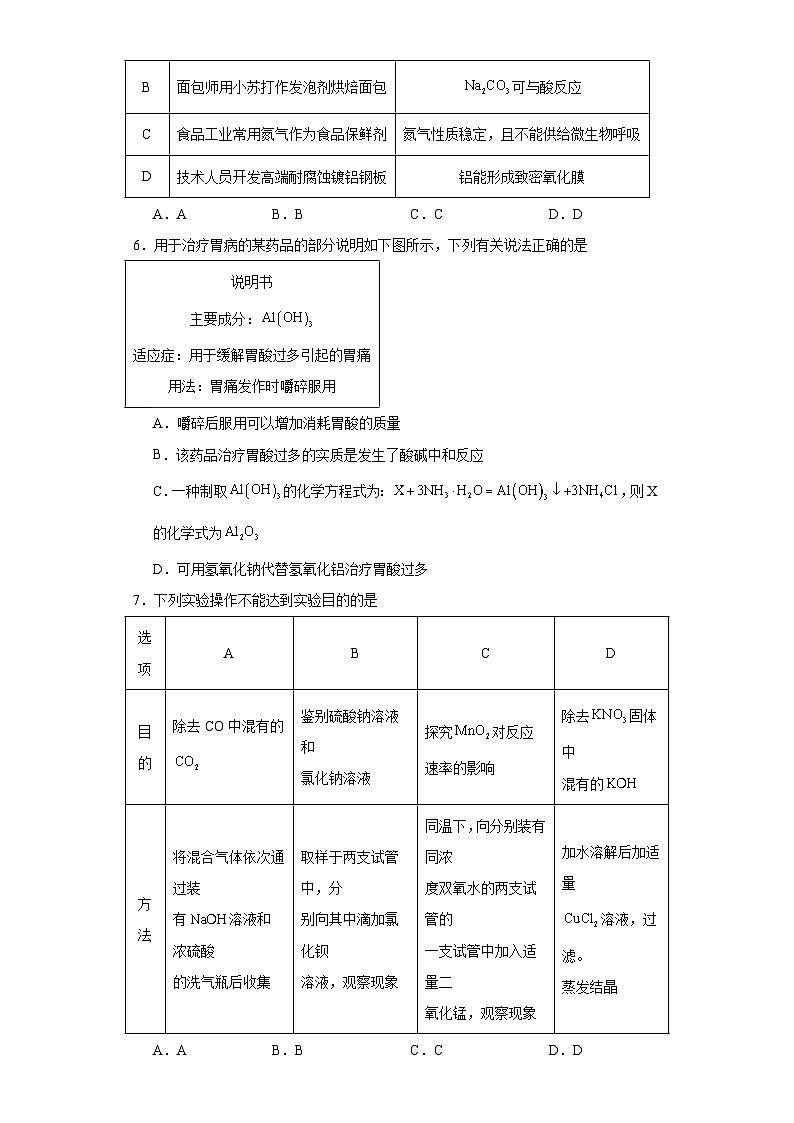
6.用于治疗胃病的某药品的部分说明如下图所示,下列有关说法正确的是
说明书
主要成分:
适应症:用于缓解胃酸过多引起的胃痛
用法:胃痛发作时嚼碎服用
A.嚼碎后服用可以增加消耗胃酸的质量
B.该药品治疗胃酸过多的实质是发生了酸碱中和反应
C.一种制取的化学方程式为:,则X的化学式为
D.可用氢氧化钠代替氢氧化铝治疗胃酸过多
7.下列实验操作不能达到实验目的的是
选项
A
B
C
D
目的
除去CO中混有的
鉴别硫酸钠溶液和
氯化钠溶液
探究对反应
速率的影响
除去固体中
混有的
方法
将混合气体依次通过装
有溶液和浓硫酸
的洗气瓶后收集
取样于两支试管中,分
别向其中滴加氯化钡
溶液,观察现象
同温下,向分别装有同浓
度双氧水的两支试管的
一支试管中加入适量二
氧化锰,观察现象
加水溶解后加适量
溶液,过滤。
蒸发结晶
A.A B.B C.C D.D
8.如图装置内盛放的物质不同则产生的现象不同,对以下实验现象叙述不正确的是( )
A.若甲为稀盐酸,乙为贝壳,丙中盛Ca(OH)2溶液,则丙中溶液变浑浊
B.若甲为H2O,乙为CaO固体,丙中盛水,则丙中导管口冒气泡
C.若甲为H2O,乙为NH4NO3固体,丙中盛水,则丙中水会沿导管上升
D.若甲为浓NaOH溶液,乙为NH4NO3固体,丙中盛酚酞溶液,则丙中溶液不变色
二、填空题
9.人间最美三月天,春花烂漫展新颜。三月,是人们赏花踏青的的最好时节。
(1)赏花踏青时,人们能体验到花香四溢的原因是______;
(2)野炊是艳艳赏花踏青时喜欢的一种活动,她带的食物有牛肉、面包、苹果、果粒橙饮料等,其中牛肉中富含的主要营养素是______;
(3)小龙观察到园林工人为花木注射的营养液中含有①、②、③等物质,其中属于复合肥的是______(选填序号);
(4)野炊烧烤时,人们为使木炭燃烧的更剧烈,常将其架空,其原理是______。
10.我国向世界庄严承诺将力争在2030年前实现碳达峰,在2060年实现碳中和,体现了大国的责任与担当。为实现这一目标,我国除积极倡导并大力发展新的绿色经济、完善环保体制外,还采用了先进的“碳捕捉与封存”技术(如图所示)来处理已有的二氧化碳。请回答下列问题:
(1)“碳捕捉与封存”技术有利于控制______的加剧。
(2)将分离聚集的压入地下的过程中,分子间隔会______;
(3)将封入蓄水层时发生的化学反应属于______反应(填基本反应类型)。
(4)生活中的下列做法有利于实现碳达峰和碳中和目标的是______(选填字母)
A.植树造林 B.将燃煤脱硫后燃烧 C.推广使用风能、水能
11.水是生命之源,与人类生活息息相关。
(1)饮用硬度过大的水不利于人体健康,生活中常用______的方法来降低水的硬度。
(2)净化水时常用二氧化氯()消毒杀菌,二氧化氯中氯元素的化合价为______价。
(3)小亮同学在使用“除垢剂”去除热水瓶中的水垢时,发现有气泡产生。根据水垢的主要成分含有碳酸钙和氢氧化镁等物质,猜想到“除垢剂”的有效成分中可能含有酸。于是,他设计了用家庭中常见物质验证自己猜想的实验方案,请完成实验报告。
实验步骤
实验现象
结论
取适量“除垢剂”于瓷碗中,
向其中加入______
______
“除垢剂”的有效成分
中一定含有酸。
(4)根据实验结论,得出使用“除垢剂”时的注意事项有______(写一条)。
12.根据给出的和两种物质的溶解度表,溶解度曲线,回答问题:
温度/℃
0
20
30
40
60
80
溶解度/g
13.3
31.6
63.9
110
169
246
35.7
36.0
36.6
37.3
38.4
39.8
(1)20℃时,的溶解度为______g;
(2)从海水中提取氯化钠,通常采用蒸发溶剂的方法,而不采用冷却热饱和溶液的方法,主要原因是______
(3)将和的混合物放入60℃的水中;充分推拌,再降温致20℃,有大量晶体析出,下列说法中,正确的是______(填序号)。
A.析出的晶体只有 B.降温到20℃时溶液中的溶质只有
C.20℃时的溶液是的饱和溶液 D.60℃时有部分固体与溶液共存
三、流程题
13.黄铜渣中含有锌,氧化锌铜和氧化铜,其余为杂质。处理黄铜渣可得到硫酸锌,其主要流程如下(杂质不溶于水也不参与反应):
(1)溶液A中的阳离子有和______(填离子符号)。
(2)加酸溶解黄铜渣时,需要通风并远离火源,其原因是______;
(3)步骤Ⅱ中溶液由蓝色变为无色的化学反应方程式为______;
(4)步骤Ⅲ加热蒸发时所用到的玻璃仪器有酒精灯和______。
四、实验题
14.实验室有失去标签的三瓶无色溶液,分别是稀硫酸、碳酸钠和石灰水。为确定三瓶溶液的成分,小李同学进行了如下实验,
(1)步骤①中加入试剂X的名称是______;
(2)步骤②中发生反应的化学方程式为:______;以上试管中盛放石灰水的是______。(填“A”“B”或“C”)
(3)同学们设计了更多的方法鉴别三种物质,以下实验方案正确的是______。
①将步骤一鉴别出的B试管中的溶液分别滴入A、C试管中,也可达到实验目的
②将步骤二中的溶液换成溶液或通入气体,均可达到实验目的
③不用试剂X,将溶液分别滴入三种溶液中也可达到实验目的
15.某同学利用如下装置制取二氧化碳气体并探究其部分化学性质。请回答下列问题:
(1)装置一中发生反应的化学方程式为______;
(2)若用装置四收集二氧化碳气体,气体应从______处通入;
(3)小燕同学按A—C—B—E—D—H—I—J的顺序将各装置组装成一套完整的实验装置,则:
①装置五中观察到的现象为______;
②装置六的烧杯内应盛放的是______溶液;
③装置三中浓硫酸的作用是______。
五、科学探究题
16.小亮在实验室发现一瓶盛有无色溶液的试剂瓶,其标签已破损,从残余部分只能看出溶质质量分数为10%,具体是什么物质无法辨认。老师告诉他,这瓶溶液可能是氢氧化钠、氯化钠、氢氧化钙或碳酸钠中的一种。
(1)小亮查阅到氢氧化钙常温下的溶解度为,认为该溶液不可能是氢氧化钙,理由是______
(2)小亮用洁净干燥的玻璃棒蘸取该溶液滴到湿润的试纸上,测得,他判断这是一种碱性溶液,进而得出该溶液不可能是氯化钠溶液的结论。对他的操作方法、测量结果及结论的评价,正确的是______(填序号);
A.方法,结果,结论均正确 B.方法不正确,结果偏小,但结论正确
C.方法不正确,结果偏大,结论不正确 D.方法正确,结果正确,但结论不正确
(3)为了确定该溶液的成分,小亮同学继续进行下列实验,请你一起参与,并填写下列实验报告。
[设计实验方案]方案甲:选择氢氧化钡溶液来确定该溶液的成分;
方案乙:选择稀盐酸来确定该溶液的成分。
[进行实验]请你从方案甲和方案乙中选择一种方案进行实验、
实验步骤
实验现象
实验结论
取少量溶液于试管中,
滴加______
______
该溶液是碳酸钠溶液,有关反应
的化学方程式为:______
[实验反思]有同学认为还可以用一种常见的盐溶液来确定,该盐的化学式是______(填化学式)。
六、计算题
17.同学们为测定某未知浓度的氢氧化钠溶液的溶质质量分数,先在烧杯中加入该氢氧化钠溶液,然后滴入2滴酚酞溶液,再用滴管慢慢滴入10%的稀盐酸,并不断搅拌,当溶液颜色恰好变为无色时,共用去了稀盐酸。请回答:
(1)酚酞溶液的作用是______;
(2)计算这瓶氢氧化钠溶液的溶质质量分数。
参考答案:
1.B
【详解】A、CuSO4溶液属于混合物,而盐为纯净物,故错误;
B、KNO3是由钾离子和硝酸根离子构成的化合物,为盐,故正确;
C、NaOH是由钠离子和氢氧根离子构成的化合物,属于碱,故错误;
D、H2O是由氢、氧两种元素组成的化合物,为氧化物,故错误。
故选B。
2.A
【详解】A、“石胆能化铁为铜”的过程实际就是铁和硫酸铜溶液反应生成铜和硫酸亚铁,反应中有新物质生成,这一变化属于化学变化,故说法错误;
B、用镁铝合金代替钢材制造飞船零部件,由于镁铝合金密度小,可以减轻飞船自身的重量,故说法正确;
C、氢气属于新型能源,燃烧产物只有水,用作发射卫星的燃料可以防止环境污染,故说法正确;
D、使用CO2跨临界直冷制冰,是利用了CO2的某些物理性质——升华吸热,故说法正确。
故选A。
3.D
【详解】A、氧气不易溶于水,采用排水法收集时,从左到右,导气管应该短进长出,故错误;
B、给试管里的液体加热,要用酒精灯的外焰加热,试管口不能对着有人的地方,故错误;
C、二氧化碳气体验满时,燃着的木条要平放在集气瓶口,不能伸入集气瓶内,故错误;
D、食盐溶液放在蒸发皿中,用酒精灯直接加热,玻璃棒不断搅拌,故正确。
故选D。
4.B
【详解】A、Na可以钠元素,表示一个钠原子,还可以表示金属钠,故A错误;
B、微粒符号前的数值表示微粒个数,所以2CO2 表示两个二氧化碳分子,故B正确;
C、Fe3+表示一个铁离子带三个单位的正电荷,故C错误;
D、元素的种类由质子数决定,甲乙两种微粒中质子数不同,不属于同种元素,故D错误。
故选B。
5.B
【详解】A、熟石灰具有碱性,因此环保工程师用熟石灰处理酸性废水,故说法正确;
B、小苏打是碳酸氢钠的俗称,碳酸氢钠受热时会分解产生二氧化碳气体,且小苏打能与酸性物质反应生成二氧化碳气体,因此面包师用小苏打作发泡剂烘焙面包,故说法错误;
C、氮气性质稳定,且不能供给微生物呼吸,因此食品工业常用氮气作为食品保鲜剂,故说法正确;
D、铝的化学性质较活泼,在常温下易与空气中的氧气反应生成致密的氧化铝薄膜,从而阻止内部的铝进一步氧化,因此技术人员开发高端耐腐蚀镀铝钢板,故说法正确。
故选B。
6.B
【详解】A、嚼碎后服用能够增大反应物的接触面积,加速反应的进行,不能增加消耗胃酸的质量,故选项说法错误;
B、氢氧化铝和盐酸反应生成氯化铝和水,该反应的反应物是酸和碱,生成物是盐和水,属于中和反应,故选项说法正确;
C、根据质量守恒定律,化学反应前后元素种类不变,X中一定含有氯元素,不可能是氧化铝,根据反应前后原子种类和数目不变,反应前有3个N、15个H、3个O,反应后有1个Al、3个N、15个H、3个O,3个Cl,则X含有1个Al和3个Cl,化学式为AlCl3,故选项说法错误;
D、氢氧化钠具有强腐蚀性,不能代替氢氧化铝治疗胃酸过多,故选项说法错误;
故选:B。
7.D
【详解】A、将混合气体依次通过装有NaOH溶液(吸收二氧化碳)和浓硫酸(干燥气体)的洗气瓶后收集,可以除去CO中混有的CO2,故A正确;
B、硫酸钠与氯化钡反应生成硫酸钡沉淀,取样于两支试管中,分别向其中滴加氯化钡溶液,由白色沉淀产生的是硫酸钠溶液,无明显现象的是氯化钠溶液,可以鉴别硫酸钠溶液和氯化钠溶液,故B正确;
C、同温下,向分别装有同浓度、等体积的双氧水的两支试管的一支试管中加入适量二氧化锰,观察现象,加入二氧化锰的比没有加二氧化锰的,产生气泡快,可以探究MnO2对反应速率的影响,故C正确;
D、加水溶解后加适量CuCl2溶液,氢氧化钾与氯化铜反应生成氢氧化铜沉淀和氯化钾,引入了新的杂质氯化钾,故不能达到实验目的,故D错误。
故选D。
8.D
【详解】A、甲为稀盐酸,乙为贝壳,二者反应生成二氧化碳气体,通入装有Ca(OH)2溶液的丙中,反应生成难溶于水的碳酸钙,会有白色沉淀产生,则丙中溶液变浑浊,正确;
B、若甲为H2O,乙为CaO固体,CaO固体溶于水中放热,气体受热膨胀,使得丙中导管口冒气泡,正确;
C、NH4NO3固体溶于水会吸热,则丙中水会沿导管上升,正确;
D、氢氧化钠与硝酸铵反应生成氨气,氨气溶于水生成氨水,氨水显碱性会使丙中酚酞溶液变红色,错误。
故选D。
9.(1)分子在不断运动
(2)蛋白质
(3)②③/③②
(4)增大木炭与空气的接触面(合理即可)
【详解】(1)花香四溢的原因是花香中含有的分子不断运动,向四周扩散,使人们闻到香味;
(2)牛肉中富含的主要营养素是蛋白质;
(3)①Ca(NO3)2中只含氮、磷、钾中的氮元素,属于氮肥;
②KNO3中含氮、磷、钾中的氮元素和钾元素,属于复合肥;
③NH4H2PO4中含氮、磷、钾中的氮元素和磷元素,属于复合肥;
故属于复合肥的为:②③;
(4)野炊烧烤时,人们为使木炭燃烧的更剧烈,常将其架空,其原理是增大木炭与空气的接触面积。
10.(1)温室效应
(2)变小
(3)化合
(4)AC
【详解】(1)二氧化碳的大量排放会造成温室效应,“碳捕捉与封存”技术可以处理已有的二氧化碳,有利于控制温室效应的加剧。
(2)分子间有间隔,将分离聚集的 CO2 压入地下的过程中,分子间隔会变小。
(3)将 CO2 封入蓄水层时,二氧化碳和水反应生成碳酸,反应物有两种,生成物只有一种,属于化合反应。
(4)A、植树造林,可以通过光合作用吸收二氧化碳,故A正确;
B、燃煤脱硫,可以减少二氧化硫生成,减少空气污染,但并没有减少二氧化碳的排放,故B错误;
C、推广使用风能、水能,可以减少化石燃料的使用,减少二氧化碳的排放,故C正确。
故选AC。
11.(1)煮沸
(2)
(3) 苏打(碳酸钠、)或小苏打()(铁钉、锌皮) 产生气泡(合理即可)
(4)不能用于去除金属表面的污渍、不能用于去除大理石或石材表面的污渍等(合理即可)
【详解】(1)饮用硬度过大的水不利于人体健康,生活中常用煮沸的方法来降低水的硬度,加热煮沸时,水中的钙离子、镁离子能够以碳酸钙沉淀、氢氧化镁沉淀的形式从水中析出,从而降低水的硬度;
(2)二氧化氯中,氧元素的化合价为-2价,根据在化合物中各元素正负化合价代数和为零,设氯元素的化合价为x,则有x+(-2)×2=0,解得x=+4价;
(3)在使用“除垢剂”去除热水瓶中的水垢时,发现有气泡产生,根据水垢的主要成分含有碳酸钙和氢氧化镁等物质,猜想到“除垢剂”的有效成分中可能含有酸;
根据实验结论“除垢剂”的有效成分中一定含有酸,根据酸的通性,酸能够与活泼金属反应产生氢气,酸能够与碳酸氢钠或碳酸钠反应生成二氧化碳气体等,所以取适量“除垢剂”于瓷碗中,向其中加入苏打(碳酸钠)(或碳酸钠)(或铁钉),观察到有气泡产生,则说明“除垢剂”的有效成分中一定含有酸;
(4)根据实验结论,“除垢剂”的有效成分中一定含有酸,酸能和活泼金属反应生成盐和氢气,酸能和碳酸盐反应生成二氧化碳气体,则使用“除垢剂”时的注意事项有不能用于去除金属表面的污渍、不能用于去除大理石或石材表面的污渍等(合理即可)。
12.(1)31.6
(2)温度变化对氯化钠的溶解度影响小
(3)AD
【详解】(1)根据表格可以看出,在20℃时,KNO3的溶解度是31.6g;
(2)由表格数据可知,氯化钠的溶解度受温度影响变化不明显,故从海水中提取氯化钠,通常采用蒸发溶剂的方法,而不采用冷却热饱和溶液的方法;
(3)将180gKNO3跟20gNaCl的混合物放入100g60℃的水中,充分搅拌,在降温到20℃,氯化钠的溶解度是36g,形成的是20℃氯化钠的不饱和溶液,故不会有氯化钠的晶体析出,降温到20℃时,硝酸钾的溶解度为31.6g,析出的晶体只有硝酸钾,得到的是20℃硝酸钾的饱和溶液。
A、由上可知,析出的晶体只有硝酸钾,故A说法正确;
B、由上可知,降温到20℃时溶液中的溶质有 NaCl和KNO3,故B说法错误;
C、由表格数据可知,20℃,氯化钠的溶解度是36g>20g,所以20℃时的溶液是 NaCl 的不饱和溶液,故C说法错误;
D、由表格数据可知,60℃时,硝酸钾的溶解度为169g<180g,所以60℃时,将180g硝酸钾加入100g水中,最多只能溶解169g硝酸钾,故60℃时有部分 KNO3 固体与溶液共存,故D说法正确;
故选:AD。
13.(1)
(2)反应过程中会产生氢气,通风并远离火源目的是为了防止氢气遇火爆炸
(3)
(4)玻璃棒
【详解】(1)溶液A中的阳离子有过量稀硫酸中的H+,反应生成硫酸锌中的Zn2+ 和反应生成硫酸铜中的Cu2+;
(2)加酸溶解黄铜渣时,需要通风并远离火源,是因为反应过程中会产生氢气,通风并远离火源目的是为了防止氢气遇火爆炸;
(3)步骤Ⅱ中溶液由蓝色变为无色,是因为锌和硫酸铜反应生成硫酸锌和铜,反应的化学方程式为:Zn+CuSO4=ZnSO4+Cu;
(4)步骤Ⅲ加热蒸发时所用到的玻璃仪器有酒精灯和玻璃棒。
14.(1)酚酞试液
(2) A
(3)①②
【分析】A、B、C三种溶液中加入试剂X后,A、C变红色,B无色,而稀硫酸呈酸性,碳酸钠溶液和石灰水呈碱性,加入酚酞可使得A. C变红色,B无色;之后加入A、C中加入氯化钡溶液,碳酸钠和氯化钡反应生成碳酸钡沉淀和氧化钠,氢氧化钙和氧化钡不反应,有此可确定A为氢氧化钙,C为碳酸钠,B为稀硫酸。
【详解】(1)由分析可知,x为酣酞试液,故填:酚酞试液;
(2)由步骤一可知,A、C为碳酸钠、氢氧化钙中的一种,步骤二中,A、C试管加入氯化钡后,A试管无现象,C试管中产生白色沉淀,而碳酸钠和氯化钡反应生成碳酸钡白色沉淀和氯化钠,反应的化学方程式为,故C为碳酸钠,A为氢氧化钙,故填:;A;
(3)实验方案正确的是:
①将硫酸加入碳酸钠和氢氧化钙中,碳酸钠和硫酸反应生成二氧化碳、水和硫酸钠,故有气泡产生的为碳酸钠,故②正确;
②由步骤一可知, A、C为碳酸钠和氢氧化钙中的一种,步骤二加入碳酸钾时,碳酸钾和碳酸钠不反应,碳酸钾和氢氧化钙反应生成碳酸钙的白色沉淀,则产生白色沉淀的为氢氧化钙,无明显现象的为碳酸钠,现象不同,可以区分;或通入二氧化碳,碳酸钠溶液中通入二氧化碳无明显现象,氢氧化钙和二氧化碳反应生成碳酸钙的白色沉淀,现象不同,也能区分,故①正确;
③将氯化钡直接加入三种试剂中,硫酸和氧化钡反应产生硫酸钡的白色沉淀,氯化钡和碳酸钠反应产生碳酸钡的白色沉淀,氯化钡和氢氧化钙不反应。其中氯化钡和稀硫酸、碳酸钠反应现象相同,不能鉴别,故③错误。
故选①②。
15.(1)
(2)G
(3) 干燥的紫色石蕊试纸不变色,湿润的紫色石蕊试纸变为红色 氢氧化钙 吸收气体中的水蒸气或干燥气体
【详解】(1)装置一中发生的反应为制取二氧化碳,碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,化学方程式为。
(2)二氧化碳密度比空气大,可用向上排空气法收集,用装置四收集二氧化碳气体,气体应从G处通入。
(3)①装置五中,二氧化碳和水反应生成碳酸,碳酸呈酸性,可以使紫色石蕊溶液变红,无水氯化钙可以吸水,干燥二氧化碳气体,所以往装置五中通过二氧化碳气体,可以观察到的现象为干燥的紫色石蕊试纸不变色,湿润的紫色石蕊试纸变为红色。
②二氧化碳可以使澄清石灰水变浑浊,所以装置六的烧杯内可以盛放的是氢氧化钙溶液,用来检验二氧化碳。
③浓硫酸具有吸水性,则装置三中浓硫酸的作用是吸收气体中的水蒸气或干燥气体。
16.(1)室温下饱和氢氧化钙溶液的质量分数仅为0.18%
(2)B
(3) 溶液(或稀盐酸) 溶液变浑浊,有白色沉淀生成(有气泡产生) () (任填一种即可)
【详解】(1)根据资料显示:氢氧化钙常温下的溶解度仅为0.18g,常温下饱和氢氧化钙溶液溶质质量分数为,达不到10%,所以该溶液不可能是氢氧化钙溶液;
(2)用pH试纸测定溶液的pH时,正确的操作方法为在白瓷板或玻璃片上放一小片pH试纸,用玻璃棒蘸取待测液滴到pH试纸上,把试纸显示的颜色与标准比色卡比较,读出pH。题目中是用洁净干燥的玻璃棒蘸取该溶液滴到湿润的 pH 试纸上,相当于稀释了溶液,溶液的碱性减弱,则测量pH偏小,但是不会改变溶液的酸碱性,所以该方法不正确,结果偏小,但是结论是正确的,故选B;
(3)通过前面探究排除了氯化钠与氢氧化钙,下面只是区分氢氧化钠与碳酸钠了;
[进行实验]
根据实验结论,该溶液是碳酸钠溶液,可取少量溶液于试管中,滴加稀盐酸,碳酸钠可以与盐酸反应生成氯化钠、二氧化碳和水,可观察到产生气泡,即可说明该溶液为碳酸钠溶液,该反应的化学方程式为:2HCl+Na2CO3=2NaCl+H2O+CO2↑;
或取少量溶液于试管中,滴加氢氧化钡溶液,碳酸钠与氢氧化钡反应生成碳酸钡沉淀和氢氧化钠,会看到产生白色沉淀,即可说明该溶液为碳酸钠溶液,该反应的化学方程式为:Na2CO3+Ba(OH)2═BaCO3↓+2NaOH;
[实验反思]
碳酸根离子可以与钙离子、钡离子反应生成碳酸钙(或碳酸钡)沉淀,所以可以加入CaCl2或BaCl2或Ca(NO3)2或Ba(NO3)2 溶液来验证。
17.(1)判断反应是否恰好完成
(2)解:设5g氢氧化钠溶液中含有氢氧化钠的质量为x
该氢氧化钠溶液的溶质质量分数
答:这瓶氢氧化钠溶液的溶质质量分数为32%
【详解】(1)氢氧化钠与稀盐酸的溶质氯化氢反应无明显现象产生,为了判断该反应是否发生以及是否恰好完全反应,需要借助酚酞溶液,故填写:判断该反应是否发生以及是否恰好完全反应。
(2)详解见答案。
【点睛】该题为文字计算题,难点在于本题没有已知的纯净物质量,需要根据溶质质量分数的变形公式,计算出溶质质量,代入化学方程式中解未知的溶质质量,再通过溶质质量分数公式,计算问题中的溶质质量分数。
2023年陕西省西安市莲湖区中考模拟化学试题(含答案): 这是一份2023年陕西省西安市莲湖区中考模拟化学试题(含答案),共9页。试卷主要包含了本试卷分为第一部分,劳动开创未来,人间最美三月天,春花烂漫展新颜,来处理已有的二氧化碳等内容,欢迎下载使用。
2023年陕西省西安市莲湖区部分学校中考三模化学试题(含答案): 这是一份2023年陕西省西安市莲湖区部分学校中考三模化学试题(含答案),共10页。试卷主要包含了本试卷分为第一部分,领到试卷和答题卡后,请用0等内容,欢迎下载使用。
2022年陕西省西安市莲湖区5校联考中考二模化学试题(word版含答案): 这是一份2022年陕西省西安市莲湖区5校联考中考二模化学试题(word版含答案),共9页。试卷主要包含了本试卷分为第一部分,领到试卷和答题卡后,请用0,5 Ca-40等内容,欢迎下载使用。













