

选择性必修1第四节 沉淀溶解平衡优秀教案
展开![]()
第四节 沉淀溶解平衡
第2课时 教学设计
【教学目标】
1.了解沉淀的生成、溶解与转化。能结合实例说明pH调控的沉淀生成、溶解与转化等在工农业生产和科学研究中的重要作用。
2.能综合运用离子反应和沉淀溶解平衡理论,分析和解决生产、生活中有关沉淀溶解平衡的实际问题
【教学重难点】
沉淀溶解平衡的应用
【教学过程】
1.新课导入
[创设情境]锅炉水垢CaSO4既会降低燃料的利用率,造成能源浪费,也会影响锅炉的使用寿命,造成安全隐患,因此要定期清除。硫酸钙在硫酸、盐酸中的溶解度小,如何除去锅炉水垢呢?带着问题我们一起学习今天的内容——沉淀溶解平衡的应用。
2.新课讲授
[讲解](一)沉淀的生成
1、原理:生成溶解度小的电解质,越小越好。
2、应用:在无机物的制备和提纯、废水处理等领域,常利用生成沉淀来达到分离或除去某些离子的目的。
3、沉淀生成时沉淀剂的选择原则
①使生成沉淀的反应进行得越完全越好(被沉淀离子形成沉淀的Ksp尽可能地小,即沉淀溶解度越小越好)。
如除去废水中的Cu2+,可以使Cu2+转化成CuCO3、Cu(OH)2或CuS,依据三者溶解度的大小可知,应选择沉淀剂使废水中的Cu2+转化成溶解度最小的CuS。
②不能影响其他离子的存在,由沉淀剂引入溶液的杂质离子要便于除去或不引入新的杂质离子。
4、方法
(1)调pH:工业原料氯化铵中含杂质氯化铁,将含杂质的氯化铵溶解于水,再加入 氨水 调节pH,可使Fe3+生成 Fe(OH)3沉淀而除去。
离子反应方程式为: Fe3+ + 3NH3•H2O==Fe(OH)3↓+3NH4+ 。
[思考讨论]调节pH形成氧化物沉淀
氢氧化物 | 开始沉淀时的pH值 (0.1mol/L) | 沉淀完全时的pH值 (<10-5mol/L) |
Cu(OH)2 | 4.67 | 6.67 |
Fe(OH)3 | 1.48 | 2.81 |
根据上表的数据,CuCl2中混有少量Fe3+如何除去?
[回答]加入氢氧化铜或碱式碳酸铜或氧化铜,调节pH至3~4,促进Fe3+水解,转化为氢氧化铁沉淀。
[讲解](2)除了调节pH的方法达到沉淀的目的,还可以用加沉淀剂的方法,在工业废水处理过程中,以Na2S作沉淀剂,使废水中的某些金属离子如Cu2+、Hg2+等,生成极难溶的CuS、HgS等沉淀而除去。
[生产实际]化学沉淀法废水处理工艺流程示意图
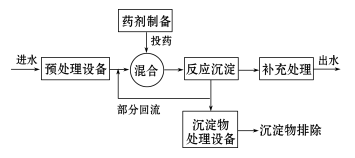
(3)氧化还原法
[议一议]在粗制CuSO4·5H2O晶体中常含有杂质Fe2+,在提纯时,为了除去Fe2+,常用什么方法?(溶液中Fe2+ 、Cu2+、Fe3+完全沉淀为氢氧化物,需要的pH分别为9.6、6.4、3.2)
[讲解]常加少量的H2O2,使Fe2+氧化为Fe3+,然后再加少量碱至溶液
(4)还可以应用同离子效应法,比如![]() ,加入硫酸,硫酸根浓度大,使平衡左移有利于沉淀生成。
,加入硫酸,硫酸根浓度大,使平衡左移有利于沉淀生成。
[过渡]反过来考虑,不断减少溶解平衡体系中的相应离子,使平衡向沉淀溶解的方向移动,就达到使沉淀溶解的目的。
(二)沉淀的溶解
[讲解]1、原理:不断减少溶解平衡体系中的相应离子,使平衡向沉淀溶解的方向移动,就达到使沉淀溶解的目的。
(1)酸溶解法:强酸是常用的溶解难溶电解质的试剂
[设疑]CaCO3为什么能溶于稀盐酸?
[回答]碳酸钙在水中电离出CO32-和Ca2+,碳酸钙溶于稀盐酸,稀盐酸中含有大量的H+,CO32-结合H+生成CO2,CO2气体的生成和逸出,使CaCO3溶解平衡体系中的CO32-浓度不断减小,促进碳酸钙的溶解平衡向沉淀溶解的方向移动。
[学生活动]写出氢氧化镁沉淀溶解平衡的表达式。若使氢氧化镁沉淀溶解,可以采取什么方法?所依据的原理是什么?
(2) 盐溶解法
[引导]根据勒夏特列原理,使沉淀溶解平衡向溶解方向移动可采取的方法有:升温、加水、加盐酸……
[学生活动] 向该饱和溶液中分别加入盐酸、CH3COONa、NH4Cl时固体Mg(OH)2的质量有什么变化?
[对点练习]见课件
[讲解] (3) 配位溶解法
如AgCl也可溶于NH3 · H2O溶液中,在有固态AgCl存在的饱和溶液中,存在着如下平衡:
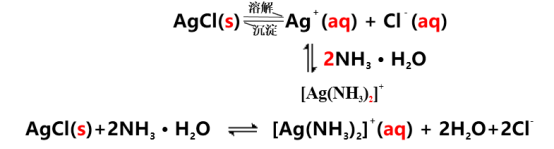
[讲解] (4) 氧化还原法
如不溶于盐酸的Ag2S、CuS、HgS等硫化物加热条件下可溶于硝酸中。

[实验探究2]
1.向盛有2 mL 0.1 mol/L NaCl溶液的试管中滴加2滴0.1mol/L AgNO3,溶液,观察并记录现象。
2.振荡试管,然后向其中滴加4滴0.1 mol/L KI溶液,观察并记录现象。
3.振荡试管,然后再向其中滴加8滴0.1 mol/L Na2S溶液,观察并记录现象。
实验方程式:
[讲解](三)沉淀的转化
Ksp(AgCl)<Ksp(AgI),即AgI在水中的溶解度远比AgCl的溶解度小,当向AgCl沉淀中滴加KI溶液中,溶液中Ag+和 I- 的离子积Q(AgI) Ksp(AgI),因此,Ag+ 和I- 结合成AgI沉淀,导致AgCl的沉淀溶解平衡向 的方向移动,直至建立新的沉淀溶解平衡。
[归纳小结](四)沉淀转化的实质与规律
①实质:沉淀的转化是指由种沉淀转化为另一种沉淀的过程,其实质是沉淀溶解平衡的移动。
②规律
a.一般来说,溶解度小的沉淀转化为溶解度更小的沉淀容易实现。两者的溶解度差别越大,转化越容易。
b.当一种试剂能沉淀溶液中的几种离子时,生成沉淀所需要试剂离子浓度越小的越先沉淀。
c.如果生成各种沉淀所需要试剂离子的浓度相差较大,就能分步沉淀,从而达到分离离子的目的。
[讲解]回到我们最开始的问题,怎么解释?
[回答]先要考虑水垢的成分,有CaCO3 、Mg(OH)2、 CaSO4 等,现用饱和Na2CO3溶液浸泡数天,将CaSO4转化为CaCO3 ,再用用盐酸或饱氯化铵液除去CaCO3 、Mg(OH)2。
一些自然现象的解释:各种原生铜的硫化物经氧化、淋滤变成CuSO4溶液,向深部渗透,遇到深层闪锌矿(ZnS)和方铅矿(PbS),便慢慢地转变为铜蓝(CuS)。
[对点练习]见课件
[课堂小结]
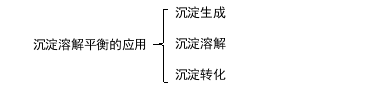
[板书设计]
3.4.2沉淀溶解平衡的应用
人教版 (2019)选择性必修1第二节 电解池优秀教学设计及反思: 这是一份人教版 (2019)选择性必修1第二节 电解池优秀教学设计及反思,共7页。教案主要包含了教学目标,教学重难点,教学过程,思考交流,课堂专练,拓展提升,学生活动,归纳对比等内容,欢迎下载使用。
人教版 (2019)选择性必修1第三章 水溶液中的离子反应与平衡第四节 沉淀溶解平衡一等奖教案设计: 这是一份人教版 (2019)选择性必修1第三章 水溶液中的离子反应与平衡第四节 沉淀溶解平衡一等奖教案设计,共6页。教案主要包含了教学目标,教学重难点,教学过程,创设情境,思考交流,查阅资料,进一步思考,得出结论等内容,欢迎下载使用。
高中化学人教版 (2019)选择性必修1第三节 盐类的水解优秀教学设计: 这是一份高中化学人教版 (2019)选择性必修1第三节 盐类的水解优秀教学设计,共7页。教案主要包含了教学目标,教学重难点,教学过程,创设情境,学生活动,科学探究,归纳小结,课堂专练等内容,欢迎下载使用。













