突破05 物质制备型实验(一)-备战2023年高考化学《化学实验大题》专题突破系列
展开化学实验专题训练(三)
——物质制备型实验
1、无机物制备型实验方案设计的基本思路:
原料
2、无机物制备综合实验的思维方法
【课后作业】
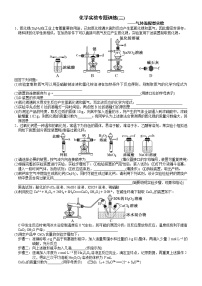
1、过氧化钙微溶于水,溶于酸,可用作分析试剂、医用防腐剂、消毒剂。以下是一种制备过氧化钙的实验方法。回答下列问题:
(一)碳酸钙的制备:
(1)步骤①加入氨水的目的是______________________,小火煮沸的作用是使沉淀颗粒长大,有利于________
(2)右图是某学生的过滤操作示意图,其操作不规范的是________(填标号)。
a.漏斗末端颈尖未紧靠烧杯壁 b.玻璃棒用作引流
c.将滤纸湿润,使其紧贴漏斗壁 d.滤纸边缘高出漏斗
e.用玻璃棒在漏斗中轻轻搅动以加快过滤速度
(二)过氧化钙的制备
CaCO3滤液 白色结晶
(3)步骤②的具体操作为逐滴加入稀盐酸,至溶液中尚存有少量固体,此时溶液呈________性(填“酸”“碱”或“中”),将溶液煮沸,趁热过滤。将溶液煮沸的作用是___________________________________________________
(4)步骤③中反应的化学方程式为______________________________________________________,该反应需要在冰浴下进行,原因是_________________________________________________________
(5)将过滤得到的白色结晶依次使用蒸馏水、乙醇洗涤,使用乙醇洗涤的目的是________________
(6)制备过氧化钙的另一种方法是:将石灰石煅烧后,直接加入双氧水反应,过滤后可得到过氧化钙产品。该工艺方法的优点是______________________,产品的缺点是________________________
2、醋酸亚铬[(CH3COO)2Cr·2H2O]为砖红色晶体,难溶于冷水,易溶于酸,在气体分析中用作氧气吸收剂。一般制备方法是先在封闭体系中利用金属锌作还原剂,将三价铬还原为二价铬;二价铬再与醋酸钠溶液作用即可制得醋酸亚铬。实验装置如图所示。回答下列问题:
(1)实验中所用蒸馏水均需经煮沸后迅速冷却,目的是________________________,仪器a的名称是________
(2)将过量锌粒和氯化铬固体置于c中,加入少量蒸馏水,按图连接好装置。打开K1、K2,关闭K3。
①c中溶液由绿色逐渐变为亮蓝色,该反应的离子方程式为_____________________________________
②同时c中有气体产生,该气体的作用是____________________________________
(3)打开K3,关闭K1和K2。c中亮蓝色溶液流入d,其原因是____________________________________________;
d中析出砖红色沉淀。为使沉淀充分析出并分离,需采用的操作是_____________、__________、洗涤、干燥
(4)指出装置d可能存在的缺点_____________________________________________
3、氮化镓(GaN)被称为第三代半导体材料,其应用已经取得了突破性的进展。
已知:(ⅰ)氮化镓性质稳定,不与水、酸反应,只在加热时溶于浓碱
(ⅱ)NiCl2溶液在加热时,先转化为Ni(OH)2,后分解为NiO
(ⅲ)制备氮化镓的反应为2Ga+2NH32GaN+3H2 (Ni做催化剂)
某学校化学兴趣小组实验室制备氮化镓,设计实验装置如图所示
设计实验步骤如下:
①滴加几滴NiCl2溶液润湿金属镓粉末,置于反应器内
②先通入一段时间的H2,再加热
③停止通氢气,改通入氨气,继续加热一段时间
④停止加热,继续通入氨气,直至冷却
⑤将反应器内的固体转移到盛有盐酸的烧杯中,充分反应后过滤、洗涤、干燥
(1)仪器X中的试剂是____________,仪器Y的名称是__________
(2)该套装置中存在的一处明显的错误是___________________________________
(3)步骤①中选择NiCl2溶液,不选择氧化镍的原因是__________
a.增大接触面积,加快化学反应速率 b.使镍能均匀附着在镓粉的表面,提高催化效率
c.为了能更好形成原电池,加快反应速率
(4)步骤③中制备氮化镓,则判断该反应接近完成时,观察到的现象是_____________________________________
(5)请写出步骤⑤中检验产品氮化镓固体洗涤干净的操作:_____________________________________________
(6)镓元素与铝同族,其性质与铝类似,请写出氮化镓溶于热的浓NaOH溶液的离子方程式:__________________
4、碳酸镧咀嚼片是一种不含钙和铝的磷酸盐结合剂,用于慢性肾衰患者高磷血症的治疗。碳酸镧可由LaCl3为原料来制备,整个反应在较低的pH条件下进行,避免生成碱式碳酸镧[La(OH)CO3]。
(1)化学兴趣小组利用下列装置在实验室中用碳酸氢铵制备碳酸镧。
①仪器X的名称为___________;检验装置甲气密性良好的方法是_____________________________________
②实验中K1、K2打开的先后顺序为__________________;为保证碳酸镧的纯度,实验过程中需要注意的问题有____________________
(2)碳酸钠或碳酸氢钠与氯化镧反应均可生成碳酸镧。
①为了高磷血症患者的安全,通常选用碳酸氢钠溶液,过程中会发生两个平行反应,其离子方程式为______________________________和______________________________
②选择碳酸氢钠溶液制备碳酸镧的优点是____________________________________(任写一条)
③T ℃时,碳酸镧饱和溶液的浓度为1.0×10-7 mol·L-1,HCO的电离常数为6.0×10-11。请计算反应
2LaCl3+3NaHCO3La2(CO3)3↓+3NaCl+3HCl的平衡常数K=________
④利用手持技术测定溶液的pH从而监控反应过程,得到如图曲线。请说明bc段变化的原因:___________
_________________________________________________________________________________________
(3)碳酸镧(相对分子质量为458)质量分数的测定:准确称取15.0 g产品试样,溶于10.0 mL稀盐酸中,加入10 mL NH3—NH4Cl缓冲溶液,加入0.2 g紫脲酸铵混合指示剂,用1.0 mol·L-1 EDTA(Na2H2Y)标准溶液滴定至呈蓝紫色(La3++H2Y2-===LaY-+2H+),消耗EDTA溶液60.00 mL。则产品中碳酸镧的质量分数w=________
5、氢化铝锂(LiAlH4)是有机合成中的重要还原剂。某课题组设计实验制备氢化铝锂并测定其纯度。已知: 氢化铝锂、氢化锂遇水都剧烈反应并产生同一种气体。
Ⅰ.制备氢化锂:选择图1中的装置制备氢化锂(有些装置可重复使用):
(1)装置的连接顺序(从左至右)为A→______________________________
(2)检查好装置的气密性,点燃酒精灯前需进行的实验操作是________________________________________
(3)写出制备氢化锂的化学方程式:_____________________________________________________
Ⅱ.制备氢化铝锂:1947年,Schlesinger、Bond和Finholt首次制得氢化铝锂,其方法是使氢化锂与无水三氯化铝按一定比例在乙醚中混合,搅拌,充分反应后,经一系列操作得到LiAlH4晶体。
(4)写出氢化锂与无水三氯化铝反应的化学方程式:_______________________________________________
Ⅲ.测定氢化铝锂产品(不含氢化锂)的纯度
(5)按图2装配仪器、检查装置气密性并装好试剂(Y形管中的蒸馏水足量,为了避免氢化铝锂遇水发生爆炸,蒸馏水中需掺入四氢呋喃作稀释剂),启动反应的操作是______________________________________________。读数之前,上下移动量气管右侧的容器,使量气管左、右两侧的液面在同一水平面上,其目的是__________
________________________________
(6)在标准状况下,反应前量气管读数为V1 mL,反应完毕并冷却之后,量气管读数为V2 mL。该样品的纯度为______(用含a、V1、V2 的代数式表示)。如果起始读数时俯视刻度线,测得的结果将________(填“偏高”“偏低”或“无影响”)
6、一氧化二氯(Cl2O)是一种氯化剂和氧化剂,极易溶于水,与水反应生成HClO,遇有机物易燃烧或爆炸。利用如图装置可制备Cl2O。回答下列问题:
已知Cl2O的部分性质如表:
熔点
沸点
制备方法
-120.6 ℃
2.0 ℃
2HgO+2Cl2===Cl2O+HgCl2·HgO
(1)装置甲中仪器B的名称是____________
(2)装置甲的作用是为该制备反应提供Cl2,写出该装置中制备Cl2的离子方程式:__________________________
(3)装置乙的作用是____________________,装置丙的洗气瓶中盛有的试剂是____________
(4)装置戊中的特型烧瓶内盛有玻璃丝,玻璃丝上附着有HgO粉末,其中玻璃丝的作用是___________________
(5)装置戊和装置己之间的装置为玻璃连接装置,而不是橡胶管,其原因是_________________________________
(6)氨的沸点为-33.4 ℃,熔点为-77.7 ℃,则装置己中收集到的产物为________(填“固体”“液体”或“气体”)物质。
若实验开始前称量装置戊中的玻璃丝与HgO的混合物的质量为a g,实验结束后玻璃丝及其附着物的质量为b g,则制备的Cl2O为________mol
(7)尾气中的有毒气体成分是________,可用________吸收除去
7、实验室以绿矾(FeSO4·7H2O)制备补血剂甘氨酸亚铁[(NH2CH2COO)2Fe] 有关物质性质如下:
甘氨酸(NH2CH2COOH)
柠檬酸
甘氨酸亚铁
易溶于水,微溶于乙醇,两性化合物
易溶于水和乙醇,有强酸性和还原性
易溶于水,难溶于乙醇
实验过程:
Ⅰ.配制含0.10 mol FeSO4的绿矾溶液
Ⅱ.制备FeCO3:向配制好的绿矾溶液中,缓慢加入200 mL 1.1 mol·L-1 NH4HCO3溶液,边加边搅拌,反应结束后过滤并洗涤沉淀
Ⅲ.制备(NH2CH2COO)2Fe:实验装置如下图(夹持和加热仪器略去),将实验Ⅱ得到的沉淀和含0.20 mol甘氨酸的水溶液混合后加入C中,然后利用A中的反应将C中空气排净,接着滴入柠檬酸溶液并加热。反应结束后过滤,滤液经蒸发结晶、过滤、洗涤、干燥得到产品
回答下列问题:
(1)实验Ⅰ中:实验室配制绿矾溶液时,为防止FeSO4被氧化变质,应加入的试剂为________(写化学式)。再滴加少量稀硫酸的作用是________________________________
(2)实验Ⅱ中:生成沉淀的离子方程式为_____________________________________
(3)实验Ⅲ中:
①C中盛柠檬酸溶液的仪器名称为_____________________________
②装置A中所盛放的试剂是________
A.Na2CO3和稀H2SO4 B.CaCO3和稀H2SO4 C.CaCO3和稀盐酸
③确认C中空气排尽的实验现象是_______________________________________
④加入柠檬酸溶液一方面可调节溶液的pH促进FeCO3溶解,另一个作用是________________
⑤洗涤实验Ⅲ中得到的沉淀,所选用的最佳洗涤试剂是________
A.热水 B.乙醇溶液 C.柠檬酸溶液
⑥若产品的质量为17.34 g,则产率为________%
8、三氯氧磷(POCl3)是一种重要的化工原料,工业上可以直接氧化PCl3制备POCl3,反应原理为:
P4(白磷)+6Cl2===4PCl3,2PCl3+O2===2POCl3。
PCl3、POCl3的部分性质如下:
物质
熔点/℃
沸点/℃
其他
PCl3
-112
75.5
遇水生成H3PO3和HCl
POCl3
2
105.3
遇水生成H3PO4和HCl
某兴趣小组模拟该工艺设计实验装置如下(某些夹持装置、加热装置已略去):
(1)仪器a的名称为________________,B装置中长颈漏斗的作用是________________
(2)装置E用来制取Cl2,反应的离子方程式为________________________________
(3)为使实验顺利进行,还需补充的装置为_____________
(4)反应时,需严格控制三个条件:
①先制取________________,缓慢地通入C 中,直至C 中的白磷消失后,再通入另一种气体
②C装置用水浴加热控制温度为60~65 ℃,除加快反应速率外,另一目的是_____________________
③反应物必须干燥,否则会在C 装置中产生大量的白雾,其主要成分为________(写化学式)
(5)反应结束后通过下面步骤测定POCl3产品中Cl 的含量,元素Cl 的质量分数为____________(写出计算式)
Ⅰ.取x g产品于锥形瓶中,加入足量NaOH溶液,POCl3完全反应后加稀硝酸至酸性;
Ⅱ.向锥形瓶中加入0.100 0 mol·L-1 的AgNO3 溶液40.00 mL,使Cl-完全沉淀;
Ⅲ.再向锥形瓶中加入20 mL硝基苯,振荡,使沉淀表面被有机物覆盖;
Ⅳ.然后加入指示剂,用c mol·L-1 NH4SCN溶液滴定过量Ag+至终点,记下所用体积为V mL。
[已知:Ag3PO4溶于酸,Ksp(AgCl )=3.2×10-10,Ksp(AgSCN )=2×10-12]
9、肼是重要的化工原料。某探究小组利用下列反应制取水合肼(N2H4·H2O):
CO(NH2)2+2NaOH+NaClO===Na2CO3+N2H4·H2O+NaCl
实验一:制备NaClO溶液(实验装置如图所示)
(1)配制 30% NaOH溶液时,所需的玻璃仪器除量筒外,还有________
A.容量瓶 B.烧杯 C.烧瓶 D.玻璃棒
(2)锥形瓶中发生反应的化学方程式是______________________________________
(3)因后续实验需要,需利用中和滴定原理测定反应后锥形瓶内混合溶液中NaOH的浓度。请选用所提供的试剂,设计实验方案:________________________________________________________________________
提供的试剂:H2O2溶液、FeCl2溶液、0.100 0 mol·L-1盐酸、酚酞试液
实验二:制取水合肼(实验装置如图所示)。
控制反应温度,将分液漏斗中溶液缓慢滴入三颈烧瓶中,充分反应。加热蒸馏三颈烧瓶内的溶液,收集108~114 ℃馏分 (已知:N2H4·H2O+2NaClO===N2↑+3H2O+2NaCl)
(4)分液漏斗中的溶液是________,选择的理由是___________________________________________________
A.CO(NH2)2溶液 B.NaOH和NaClO混合溶液
实验三:测定馏分中水合肼的含量。
称取馏分5.000 g,加入适量NaHCO3固体,加水配成250 mL溶液,移取25.00 mL,用0.100 0 mol·L-1的I2溶液滴定。滴定过程中,溶液的pH保持在6.5左右 (已知:N2H4·H2O+2I2===N2↑+4HI+H2O)
(5)滴定过程中,NaHCO3能控制溶液的pH在6.5左右,原因是_________________________________________
(6)实验测得消耗I2溶液的平均值为18.00 mL,馏分中水合肼(N2H4·H2O)的质量分数为________
10、S2Cl2用作橡胶的低温硫化剂和粘结剂,由硫与限量氯气在50~60℃反应制得,进一步氯化可得SCl2、S2Cl2、SCl2的某些性质如下:
水溶性
密度(g/cm3)
颜色
熔点
沸点
S2Cl2
空气中发烟雾,通水即分解
1.687
金黄色
-76℃
138℃
SCl2
溶于水且剧烈反应
1.621
樱桃红
-122℃
59℃
用如图所示装置制备S2Cl2回答下列问题:
(1)写出S2Cl2的电子式_________________
(2)写出仪器c的名称_____________,实验开始前先在b中放入一定量的硫粉,加热使硫熔化,然后转动和摇动烧瓶使硫附着在烧瓶内壁形成一固体薄层,这样做的目的是_____________________________
(3)实验时,b装置需加热,最好采用何种方式加热_____________________
(4)b中的反应开始前,需排除装置中的空气,简述相关操作:_________________________
(5)装置d中盛放的试剂是_____________________,其作用是①_________________,②_________________
(6)为了获得更纯净的S2Cl2,需要对产品进行的操作是_____________________
(7)若将S2Cl2放入水中同时产生沉淀和气体,写出反应的方程式_____________________________
11、无水MgBr2可用作催化剂。实验室采用镁屑与液溴为原料制备无水MgBr2,装置如图1,主要步骤如下:
图1 图2
步骤1:三颈瓶中装入10 g镁屑和150 mL无水乙醚;装置B中加入15 mL液溴
步骤2:缓慢通入干燥的氮气,直至溴完全导入三颈瓶中
步骤3:反应完毕后恢复至常温,过滤,滤液转移至另一干燥的烧瓶中,冷却至0 ℃,析出晶体,再过滤得三乙醚合溴化镁粗品
步骤4:室温下用苯溶解粗品,冷却至0 ℃,析出晶体,过滤,洗涤得三乙醚合溴化镁,加热至160 ℃分解得无水MgBr2产品
已知:①Mg与Br2反应剧烈放热;MgBr2具有强吸水性
②MgBr2+3C2H5OC2H5MgBr2·3C2H5OC2H5
请回答:
(1)仪器A的名称是________,实验中不能用干燥空气代替干燥N2,原因是________
(2)如将装置B改为装置C(图2),可能会导致的后果是________
(3)步骤3中,第一次过滤除去的物质是________
(4)有关步骤4的说法,正确的是________
A.可用95%的乙醇代替苯溶解粗品 B.洗涤晶体可选用0 ℃的苯
C.加热至160 ℃的主要目的是除去苯 D.该步骤的目的是除去乙醚和可能残留的溴
(5)为测定产品的纯度,可用EDTA(简写为Y4-)标准溶液滴定,反应的离子方程式:Mg2++Y4-===MgY2-
①滴定前润洗滴定管的操作方法是______________________________________
②测定时,先称取0.250 0 g无水MgBr2产品,溶解后,用0.050 0 mol·L-1的EDTA标准溶液滴定至终点,消耗EDTA标准溶液26.50 mL,则测得无水MgBr2产品的纯度是________(以质量分数表示)
12、硫化碱法是工业上制备Na2S2O3的方法之一。某研究小组在实验室用硫化碱法制备Na2S2O3·5H2O。
(1)利用吸硫装置A制取Na2S2O3
①写出吸硫装置A中发生反应的化学方程式______________________________________________
②装置B的作用是检验装置中SO2的吸收效率,B中试剂是________________,表明SO2吸收效率低的实验现象是B中溶液____________________
③为了使SO2尽可能吸收完全,除了及时搅拌反应物外,还可采取的合理措施是____________(写出一条即可)
(2)从反应液中获得Na2S2O3·5H2O的方法是____________________、减压抽滤、洗涤干燥
(3)实验制得的Na2S2O3·5H2O产品中可能含有Na2SO3、Na2SO4等杂质。请设计实验检测Na2S2O3·5H2O产品中是否存在Na2SO4杂质,简要说明实验操作、现象和结论:_________________________________
(4)①Na2S2O3溶液是定量实验中的常用试剂,测定其浓度的过程如下:
第一步:准确称取a g KIO3(相对分子质量为214)固体配成溶液;
第二步:加入过量KI固体和H2SO4溶液,滴加指示剂;
第三步:用Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液的体积为V mL。
则c(Na2S2O3)=________mol·L-1。(列出算式即可)
(已知:IO+5I-+6H+===3I2+3H2O,2S2O+I2===S4O+2I-)
②在滴定过程中下列实验操作会造成实验结果偏低的是________
A.滴定管未用Na2S2O3溶液润洗
B.滴定终点时仰视读数
C.锥形瓶用蒸馏水润洗后未进行干燥处理
D.滴定管尖嘴处滴定前无气泡,达滴定终点时发现有气泡
【化学实验专题训练(三)——物质制备型实验】答案
1、(2016·全国卷Ⅲ)
(1)调节溶液pH 使Fe(OH)3沉淀 过滤分离
(2)ade
(3)酸 除去溶液中的CO2
(4)CaCl2+2NH3·H2O+H2O2+6H2O===CaO2·8H2O↓+2NH4Cl
或CaCl2+2NH3·H2O+H2O2===CaO2↓+2NH4Cl+2H2O 温度过高时双氧水易分解
(5)去除结晶表面水分
(6)工艺简单、操作方便 纯度较低
2、(2018·全国卷Ⅰ)
(1)去除水中溶解氧 分液(或滴液)漏斗
(2)①Zn+2Cr3+===Zn2++2Cr2+ ②排除c中空气
(3)c中产生H2使压强大于大气压 (冰浴)冷却 过滤
(4)敞开体系,可能使醋酸亚铬与空气接触
3、(1)浓氨水 球形干燥管
(2)装置F中会产生倒吸
(3)ab
(4)装置F中几乎不再产生气泡
(5)取最后一次的洗涤液于试管中,滴加AgNO3溶液,若无白色沉淀产生,则证明产品氮化镓固体已洗涤干净
(6)GaN+OH-+H2OGaO+NH3↑
4、(1)①球形干燥管 关闭活塞K1,向球形漏斗中加水至漏斗内外形成液面差,一段时间后,液面差保持不变,
说明气密性良好 ②先打开K2再打开K1 控制NH3(或CO2)通入量
(2)①2La3++3HCO===La2(CO3)3↓+3H+ H++HCO===CO2↑+H2O
②碳酸氢钠碱性相对较弱,可防止生成碱式碳酸镧[La(OH)CO3]
③200
④La3+完全沉淀,再滴入碳酸氢钠,水解使溶液的碱性增强,pH发生突跃
(3)91.6%
5、(1)D→B→C→B→E
(2)打开装置A中分液漏斗的活塞,一段时间后,用小试管在装置E的水槽中收集气体并验纯
(3)2Li+H22LiH
(4)4LiH+AlCl3===LiAlH4+3LiCl
(5)倾斜Y形管,将蒸馏水(掺入四氢呋喃)全部注入a g产品中 确保量气管内气体的压强与大气压强相等
(6)% 偏高
6、(1)圆底烧瓶
(2)2Cl-+4H++MnO2Cl2↑+Mn2++2H2O
(3)除去Cl2中的HCl杂质 浓硫酸
(4)增大反应物接触面积,提高反应速率
(5)防止Cl2O与橡胶管接触发生燃烧或爆炸
(6)液体
(7)Cl2、Cl2O 碱液
7、(1)Fe 防止Fe2+水解
(2)Fe2++2HCO===FeCO3↓+CO2↑+H2O
(3)①滴液漏斗
②C
③D中澄清石灰水变浑浊
④防止二价铁被氧化
⑤B
⑥85
8、(1)球形冷凝管 平衡气压
(2)4H++2Cl-+MnO2Mn2++Cl2↑+2H2O
(3)在a仪器后连接装有碱石灰的干燥管
(4)①Cl2 ②防止PCl3气化 ③HCl
(5)×100%
9、(1)BD
(2)Cl2+2NaOH===NaClO+NaCl+H2O
(3)取一定量锥形瓶内的混合溶液,加入适量的H2O2溶液后,滴加2~3滴酚酞试液,用0.100 0 mol·L-1盐酸滴定,重复上述操作2~3次
(4)B 如果将氢氧化钠和次氯酸钠的混合溶液装在烧瓶中,反应生成的水合肼会被次氯酸钠氧化
(5)NaHCO3会与滴定过程中产生的HI反应
(6)9%
10、(1)
(2)直型冷凝管 增大反应接触面积
(3)水浴加热
(4)通Cl2一段时间后,看到黄绿色气体充满装置b后,再开始加热b
(5)碱石灰 防止空气中的水蒸气进入d使产品与水反应 吸收剩余的Cl2
(6)分馏(或蒸馏)
(7)2S2Cl2+2H2O=SO2↑+3S↓+4HCl
11、(1)干燥管 防止镁屑与氧气反应,生成的MgO阻碍Mg与Br2的反应
(2)会将液溴快速压入三颈瓶,反应过快大量放热而存在安全隐患
(3)镁屑
(4)BD
(5)①从滴定管上口加入少量待装液,倾斜着转动滴定管,使液体润湿内壁,然后从下部放出,重复2~3次 ②97.5%
12、(1)①2Na2S+Na2CO3+4SO2===3Na2S2O3+CO2
②品红、溴水或酸性KMnO4溶液 颜色很快褪去(其他合理答案也可)
③控制SO2的流速或增大反应物的浓度(其他合理答案也可)
(2)蒸发浓缩、降温结晶
(3)取少量制得的Na2S2O3·5H2O产品于试管中,加水溶解再加入稀盐酸调至酸性,静置片刻,再取上层清液于试管中,加入BaCl2溶液,有白色沉淀产生,则证明含Na2SO4杂质,否则不含Na2SO4
(4)①
②AB
01 以无机物质制备为载体的综合型实验 (附答案解析)-备战高考化学大题逐空突破系列(全国通用): 这是一份01 以无机物质制备为载体的综合型实验 (附答案解析)-备战高考化学大题逐空突破系列(全国通用),共15页。
突破10 探究性型实验(二)-备战2023年高考化学《化学实验大题》专题突破系列: 这是一份突破10 探究性型实验(二)-备战2023年高考化学《化学实验大题》专题突破系列,共8页。
突破09 探究性型实验(一)-备战2023年高考化学《化学实验大题》专题突破系列: 这是一份突破09 探究性型实验(一)-备战2023年高考化学《化学实验大题》专题突破系列,共8页。试卷主要包含了探究性实验题的分类,探究性实验题的解法思路,预备知识等内容,欢迎下载使用。