




2022天津南开区高二上学期期末考试化学试题含解析
展开2021~2022学年度第一学期南开区期末考试试卷
高二年级化学学科
第Ⅰ卷(选择题,共45分)
可能用到的相对原子质量:H-1 C-12 N-14 O-16
一、选择题(本题包括15小题,每小题3分,共45分。每小题只有一个选项符合题意)
1. 向水中加入下列溶质,能促进水电离的是
A. B. NaOH
C. NaCl D.
2. 下列溶液一定显酸性的是
A. 含有 B. pH<7
C. D. 滴加酚酞溶液不变红
3. 下列各组离子,能在溶液中大量共存的是
A. 、、、 B. 、、、
C. 、、、 D. 、、、
4. 科学家通过观察金星的酸性云层,分析出金星存在磷化氢气体,从而推测金星可能存在生命的迹象。下列关于P元素的说法中,不正确的是
A. 第一电离能:P<S B. 原子半径:S<P
C. 非金属性:P<S D. 电负性:P<S
5. 某基态原子的价层电子的轨道表示式为 ,下列说法正确的是
A 最外层有4个电子
B. 有2种能量不同的电子
C. s电子的电子云轮廓图是圆形
D. 有5种空间运动状态不同的电子
6. 下列事实与盐类水解无关的是
A. 用制备
B. 铝盐、铁盐作净水剂
C. 实验室配制溶液时,加少量铁粉
D. 向沸水中滴入饱和溶液制胶体
7. 下列关于冰融化为水的过程判断正确的是
A B.
C. D.
8. 合成氨工业中采用循环操作,主要原因是
A. 降低氨的沸点 B. 提高氮气和氢气的利用率
C. 增大化学反应速率 D. 提高平衡混合物中氨的含量
9. 碘在不同状态下与氢气反应的热化学方程式如下所示。
①
②
下列说法正确的是
A.
B 比热稳定性更好
C. 1mol固态碘升华时
D. ①的反应物总能量比②的反应物总能量低
10. 已知: 。若断裂、需要吸收的能量分别为436kJ、945.6kJ,则断裂需要吸收的能量为
A. 391kJ B. 737kJ
C. 1173kJ D. 1474kJ
11. 在容积不变的密闭容器中,A与B反应生成C,其化学反应速率分别用、、表示。已知:、,则该反应可表示为
A. B.
C. D.
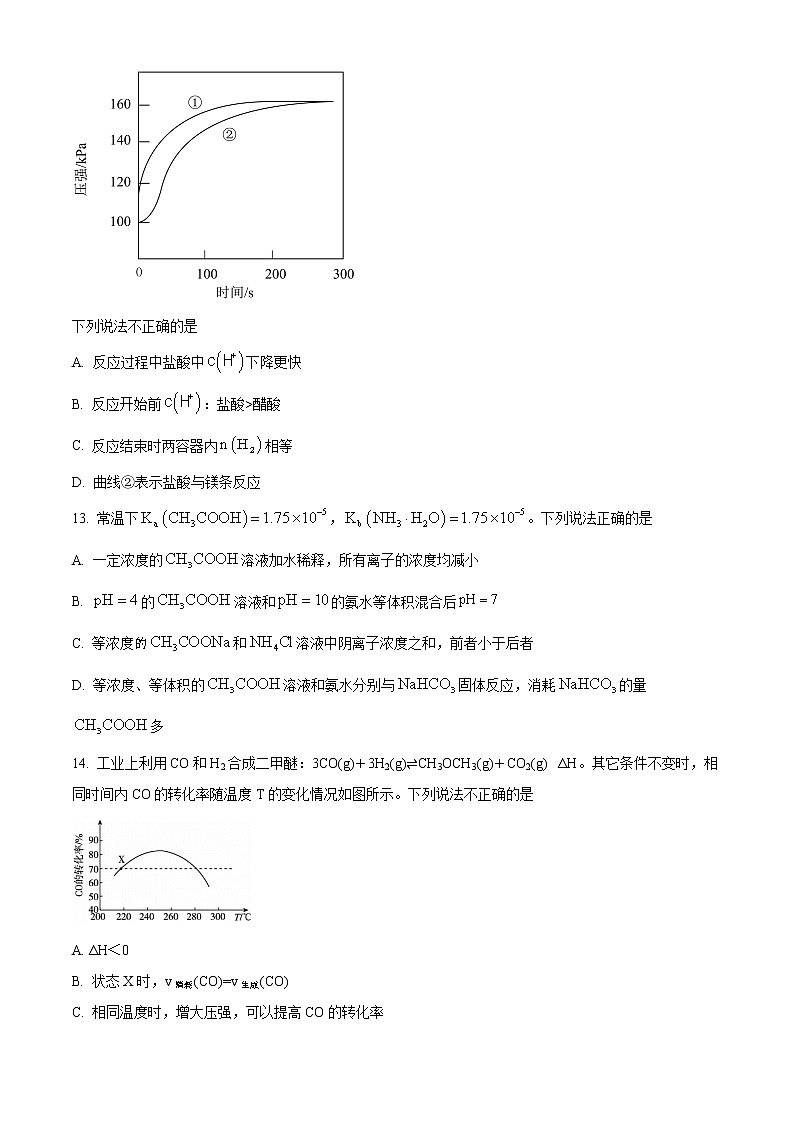
12. 将等浓度、等体积的盐酸与醋酸分别与足量的镁条反应,测得密闭容器中压强随时间的变化曲线如下图所示。
下列说法不正确的是
A. 反应过程中盐酸中下降更快
B. 反应开始前:盐酸>醋酸
C. 反应结束时两容器内相等
D. 曲线②表示盐酸与镁条反应
13. 常温下,。下列说法正确的是
A. 一定浓度的溶液加水稀释,所有离子的浓度均减小
B. 的溶液和的氨水等体积混合后
C. 等浓度和溶液中阴离子浓度之和,前者小于后者
D. 等浓度、等体积的溶液和氨水分别与固体反应,消耗的量多
14. 工业上利用CO和H2合成二甲醚:3CO(g)+3H2(g)⇌CH3OCH3(g)+CO2(g) ΔH。其它条件不变时,相同时间内CO的转化率随温度T的变化情况如图所示。下列说法不正确的是
A. ΔH<0
B. 状态X时,v消耗(CO)=v生成(CO)
C. 相同温度时,增大压强,可以提高CO的转化率
D. 状态X时,选择合适催化剂,可以提高相同时间内CO的转化率
15. 如图为氯碱工业的简易装置示意图,其中两电极均为惰性电极。 下列说法正确的是
A. a 处得到的是浓 NaOH 溶液
B. 适当降低阳极电解液的 pH 有利于 Cl2 逸出
C. 粗盐水中含有的少量 Ca2+和 Mg2+可用 NaOH 除去
D. 若电路中通过 0.2mol 电子,理论上可在 b 处得到标准状况下 1.12L 气体
第Ⅱ卷(非选择题,共55分)
可能用到的相对原子质量:H-1 C-12 N-14 O-16
二、(本题包括1小题,共13分)
16. 铜单质及其化合物应用十分广泛。回答下列问题:
(1)Cu位于元素周期表中第四周期第_______族,属于_______(填“d”或“ds”)区。
(2)基态Cu原子的电子排布式为_______。
(3)若要在铁制品表面镀铜,电镀液用硫酸铜溶液,则铜应与电源的_______(填“正”或“负”)极相连。
(4)利用电解法可将含有Fe、Zn、Ag、Pt等杂质的粗铜提纯,电解时阴极反应式为_______,电解后电解槽底部会形成含有少量_______等金属的阳极泥。
(5)写出以石墨棒为电极,电解足量溶液的总反应方程式:_______。
(6)在某温度下,向含有固体的饱和溶液中加入少量硫酸铜,则的溶解度_______(填“增大”、“减小”或“不变”,下同),_______,_______。
三、(本题包括1小题,共13分)
17. 氢能是一种极具发展潜力的清洁能源,以下反应是目前大规模制取氢气的重要方法之一: 。回答下列问题:
(1)欲提高CO的平衡转化率,理论上可以采取的措施为_______。
a.通入过量CO b.升高温度 c.加入催化剂 d.通入过量水蒸气
(2)800℃时,该反应的平衡常数,在容积为1L的密闭容器中进行反应,测得某一时刻混合物中CO、、、的物质的量分别为1mol、3mol、1mol、1mol。
①写出该反应的平衡常数表达式_______。
②该时刻反应的进行方向为_______(填“正向进行”、“逆向进行”或“已达平衡”)。
(3)830℃时,该反应的平衡常数,在容积为1L的密闭容器中,将2molCO与混合加热到830℃。反应达平衡时CO的转化率为_______。
(4)下图表示不同温度条件下,CO平衡转化率随着的变化趋势。判断、的大小关系:_______,判断理由为_______。
(5)以氢气为燃料的氢氧燃料电池,碱性电解质溶液时,负极反应式为_______。
四、(本题包括1小题,共14分)
18. 化学是一门以实验为基础的学科。回答下列问题:
Ⅰ.中和反应反应热的测定。
测定50mL 0.50mol/L盐酸和50mL 0.55mol/L NaOH溶液中和反应时放出的热量。
(1)采用稍过量的NaOH溶液的原因是_______。
(2)若两种溶液的密度均为,反应后生成溶液的比热容,反应过程中测得体系温度升高3℃,则该反应放出_______kJ热量。
Ⅱ.温度对化学平衡的影响。
(3)在生成的反应中,存在如下平衡: 。取两个封装有和混合气体的圆底烧瓶,将它们分别浸在盛有热水、冷水的大烧杯中。片刻后,比较两个烧瓶里气体的颜色,浸在_______(填“热水”或“冷水”)中的颜色更深,产生这一现象的原因是_______。
ⅢI.简易原电池反应。
(4)培养皿内装有含NaCl饱和溶液的琼脂,再滴入5~6滴酚酞溶液和溶液,混合均匀,铁钉用砂纸磨光,缠上铜丝放入培养皿中。一段时间后,可观察到没有缠铜丝的铁钉附近产生_______色的_______(填化学式)沉淀;铜丝周围的现象是_______,发生的电极反应式为_______。
五、(本题包括1小题,共15分)
19. 在25℃时对氨水进行如下操作。回答下列问题:
(1)向氨水中加入少量水,则溶液中将_______(填“增大”、“减小”或“不变”)
(2)向0.1mol/L20mL氨水中逐滴加入0.1mol/L VmL盐酸。
①若使氨水恰好被中和,则所得溶液的pH_______7(填“>”、“<”或“=”),用离子方程式表示其原因:_______。
②若所得溶液,则此时加入盐酸的体积V_______20mL(填“>”、“<”或“=”),溶液中、、、的大小关系为_______。
③若加入盐酸的体积,则此时溶液中_______mol/L。
(3)向溶液中加入1mL 0.1mol/L氨水,有白色沉淀产生,继续加入4滴溶液,观察到白色沉淀变为红褐色。试用离子方程式解释白色沉淀变为红褐色的原因:_______。
(4)向溶液中滴加氨水产生蓝色沉淀,若所得溶液,已知,则溶液中_______mol/L。
天津市南开区南开中学2021-2022学年高二上学期期末检测化学试题(含答案解析): 这是一份天津市南开区南开中学2021-2022学年高二上学期期末检测化学试题(含答案解析),文件包含精品解析天津市南开区南开中学2021-2022学年高二上学期期末检测化学试题原卷版docx、精品解析天津市南开区南开中学2021-2022学年高二上学期期末检测化学试题解析版docx等2份试卷配套教学资源,其中试卷共27页, 欢迎下载使用。
天津市南开区2023届高三一模化学试题Word版含解析: 这是一份天津市南开区2023届高三一模化学试题Word版含解析,共24页。
2022-2023学年天津市南开区高二上学期阶段性质量监测化学试题含解析: 这是一份2022-2023学年天津市南开区高二上学期阶段性质量监测化学试题含解析,共22页。试卷主要包含了 下列物质属于强电解质的是, 25℃时,水中存在电离平衡, 溶液中存在如下平衡, 已知反应, 下列叙述不正确的是, 下列叙述正确的是等内容,欢迎下载使用。












