
人教版 (2019)必修 第二册第一节 认识有机化合物备课课件ppt
展开碳在地壳中的含量很低,但是含有碳元素的有机化合物却分布极广。有机化合物不仅构成了生机勃勃的生命世界,也是燃料、材料、食品和药物的主要来源。 目前,人们在自然界发现和人工合成的物质已超过1亿种,其中绝大多数都是有机化合物,而且新的有机化合物仍在源源不断地被发现或合成出来。有机化合物为什么如此繁多?它们的结构和性质具有哪些一般特点?
让我们一起走进奇妙的有机世界
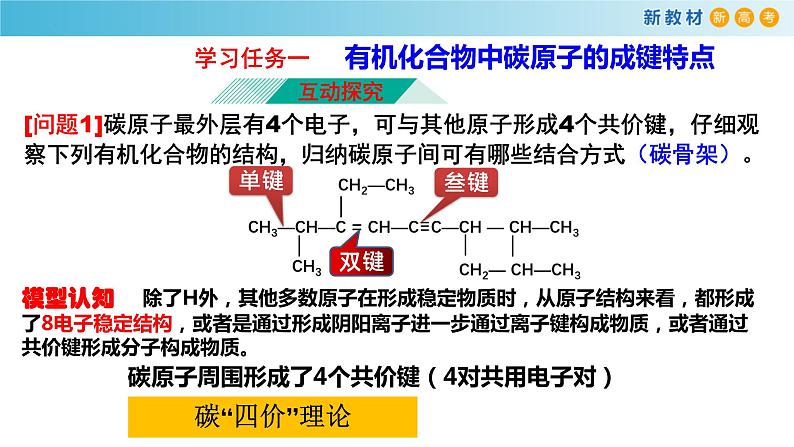
[问题1]碳原子最外层有4个电子,可与其他原子形成4个共价键,仔细观察下列有机化合物的结构,归纳碳原子间可有哪些结合方式(碳骨架)。
学习任务一 有机化合物中碳原子的成键特点
模型认知 除了H外,其他多数原子在形成稳定物质时,从原子结构来看,都形成了8电子稳定结构,或者是通过形成阴阳离子进一步通过离子键构成物质,或者通过共价键形成分子构成物质。
碳原子周围形成了4个共价键(4对共用电子对)
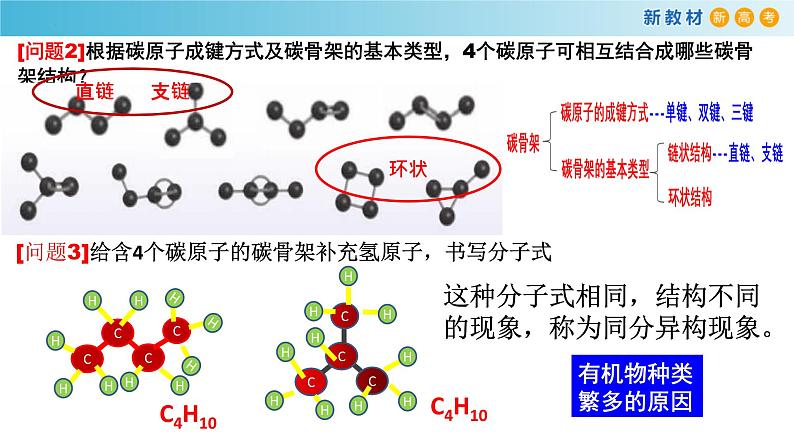
[问题3]给含4个碳原子的碳骨架补充氢原子,书写分子式
这种分子式相同,结构不同的现象,称为同分异构现象。
[问题2]根据碳原子成键方式及碳骨架的基本类型,4个碳原子可相互结合成哪些碳骨架结构?
直链 支链
两个碳原子之间可以单键、双键、三键结合,多个碳原子之间可以碳链或碳环结合。
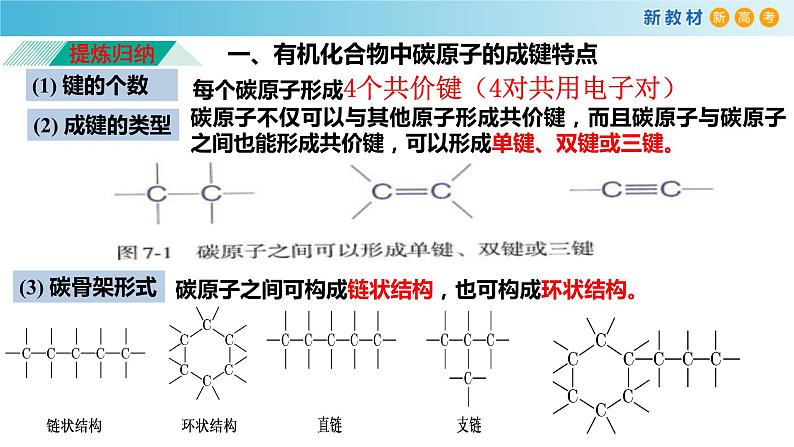
一、有机化合物中碳原子的成键特点
每个碳原子形成4个共价键(4对共用电子对)
碳原子之间可构成链状结构,也可构成环状结构。
碳原子不仅可以与其他原子形成共价键,而且碳原子与碳原子之间也能形成共价键,可以形成单键、双键或三键。
[名师点拨] (1)呈直链状的有机物分子不能理解成所有的碳原子都处在同一条直线上,如果有机物分子链状碳骨架结构中仅存在碳碳单键,则含3个及以上碳原子的分子呈锯齿状。(2)链状碳骨架结构中的碳原子最少是1个,环状碳骨架结构中的碳原子最少是3个(构成环)。(3)碳骨架结构中,碳原子余下的价键可以与氢原子或氧原子等结合,从而使碳原子最外层达到8电子稳定结构。
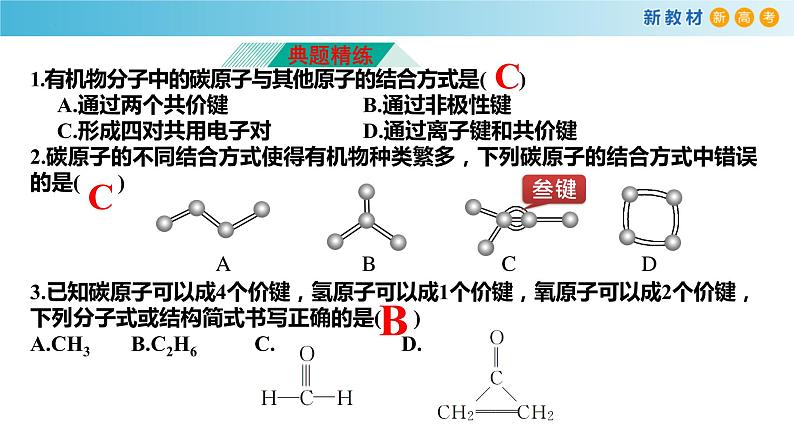
1.有机物分子中的碳原子与其他原子的结合方式是( ) A.通过两个共价键 B.通过非极性键 C.形成四对共用电子对 D.通过离子键和共价键
2.碳原子的不同结合方式使得有机物种类繁多,下列碳原子的结合方式中错误的是( )
3.已知碳原子可以成4个价键,氢原子可以成1个价键,氧原子可以成2个价键,下列分子式或结构简式书写正确的是( )A.CH3 B.C2H6 C. D.
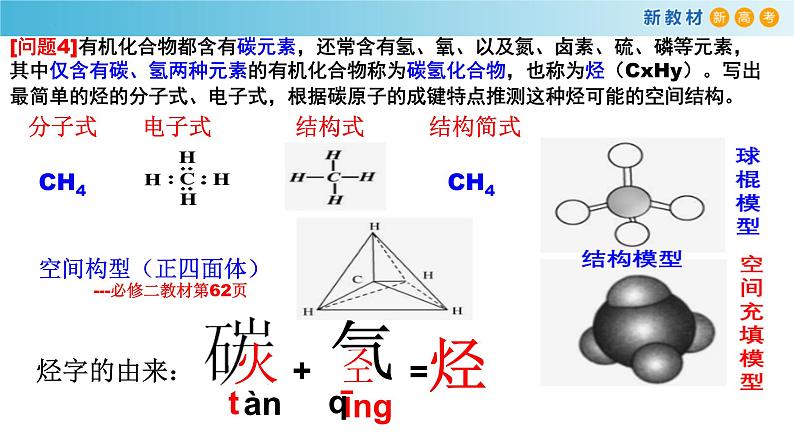
[问题4]有机化合物都含有碳元素,还常含有氢、氧、以及氮、卤素、硫、磷等元素,其中仅含有碳、氢两种元素的有机化合物称为碳氢化合物,也称为烃(CxHy)。写出最简单的烃的分子式、电子式,根据碳原子的成键特点推测这种烃可能的空间结构。
[问题5]与甲烷结构相似的有机化合物还有很多,根据碳原子的成键特点和下表中的有关信息,填写表格空白处:
CH4 C2H6 C3H8 C4H10
CH4 CH3CH3 CH3CH2CH3 CH3CH2CH2CH3
用结构式表示碳原子较多的复杂有机物时,书写很不方便,这时我们可以省略有机物中的某些单键(双键、三键和支链单键保留),用结构简式来表示。
结构式的简单表达式——结构简式
①依据乙烷、丙烷和丁烷的球棍模型,分别写出它们的分子式,并由此归纳这类有机物的分子组成通式。
提示:分子式分别为C2H6、C3H8、C4H10;这类有机物的分子组成通式为CnH2n+2(n代表碳原子数)。
[问题6]下图是四种烷烃的球棍模型:其中黑球代表碳原子,灰球代表氢原子。
②结合四种有机物的分子球棍模型,总结这类有机物的组成和分子结构特点。
提示:均由C、H两种元素组成,其结构特点有:①每个碳原子都形成4个共价单键;②碳原子之间以碳碳单键结合成链状,四种有机物为烷烃。
[名师点拨] (1)甲烷分子中的4个C—H极性键完全相同,5个原子不在同一平面上,其中最多有3个原子在同一平面上。(2)甲烷分子的电子式和结构式均表示分子中原子的成键方式,但不能表示分子真实的空间结构;球棍模型和空间充填模型则能表示分子中原子间的连接方式、原子的相对大小及空间分布等。
学习任务二 链状烷烃的结构
结构式是表达原子之间共用电子对情况的平面模型,并不能把物质的空间结构真实表达出来。实际上甲烷中的5个原子并不是处于同一平面。
2.烷烃 (1)概念 有机化合物只含有碳和氢两种元素,分子中的碳原子之间都以单键结合,碳原子的剩余价键均与氢原子结合,使碳原子的化合价都达到“饱和”。这样的一类有机化合物称为饱和烃,也称为烷烃。
(2)分子结构特点①分子结构
注意:烷烃中碳原子间结合成链状,链状不是“直线状”,而是呈锯齿状,链上也可以分出支链。例如:
烷烃包含链状烷烃和环状烷烃,高中阶段一般不探讨环烷烃的有关结构和性质,没特别注明我们讲的烷烃都是特指链状烷烃(但可以有支链)。
烃 → 饱和烃 → 烷烃 → 链状烷烃 → 环状烷烃
②分子组成通式链状烷烃的分子组成通式为CnH2n+2。
链状烷烃分子中的共价键数为(2n+2)+(n-1)=3n+1。
写出下列烷烃的分子式:(1)含有38个碳原子的烷烃的分子式 (2)含有38个氢原子的烷烃的分子式 (3)相对分子量为128的烷烃的分子式(4)碳、氢原子个数比为2∶5的烷烃的分子式为
3.链状烷烃的命名——习惯命名法
CH3CH2CH2CH2CH3
(1) 1-10个C原子的直链烷烃: 称为 甲、乙、丙、丁、戊、己、庚、辛、壬、癸 烷;(2) 11个C原子以上的直链烷烃:如:C11H24 称为十一烷;(3) 若碳原子数相同,结构不同(带支链)的烷烃:用正、异、新表示。
1.如图所示均能表示甲烷的分子结构,下列说法错误的是( )A.Ⅰ将各原子看成了质点,为立体结构示意图B.Ⅱ为电子式,表示甲烷分子中有8个电子C.Ⅲ为球棍模型,棍代表甲烷分子内含有的共价键D.Ⅳ为空间充填模型,能表示出甲烷的空间构型及各原子的相对大小
2.下图为正丁烷的球棍模型。下列说法正确的是 ( )A.正丁烷的分子式为C4H8B.分子中4个碳原子在同一条直线上C.分子中含有4个碳碳单键D.分子中共含有13个共价键
高中人教版 (2019)第一节 认识有机化合物评课课件ppt: 这是一份高中人教版 (2019)第一节 认识有机化合物评课课件ppt,共29页。PPT课件主要包含了考纲要求,一有机化合物,结构式,正四面体,烷烃的结构,链状烷烃和环状烷烃,链状烷烃的命名,十二烷,同系物,同分异构体等内容,欢迎下载使用。
人教版 (2019)必修 第二册第一节 认识有机化合物备课ppt课件: 这是一份人教版 (2019)必修 第二册第一节 认识有机化合物备课ppt课件,共19页。PPT课件主要包含了学习任务一烃,C2H2,HC≡CH,直线型键角1800,2按碳骨架的不同,苯的特殊结构的理解,有机玻璃是塑料,2橡胶,3纤维等内容,欢迎下载使用。
人教版 (2019)必修 第二册实验活动8 搭建球棍模型认识有机化合物分子结构的特点教学演示ppt课件: 这是一份人教版 (2019)必修 第二册实验活动8 搭建球棍模型认识有机化合物分子结构的特点教学演示ppt课件,共31页。PPT课件主要包含了īng,tīng,C6H14,C7H16,C14H30,C4H10等内容,欢迎下载使用。