科粤版九年级下册7.2 物质溶解的量学案及答案
展开7.2 物质溶解的量
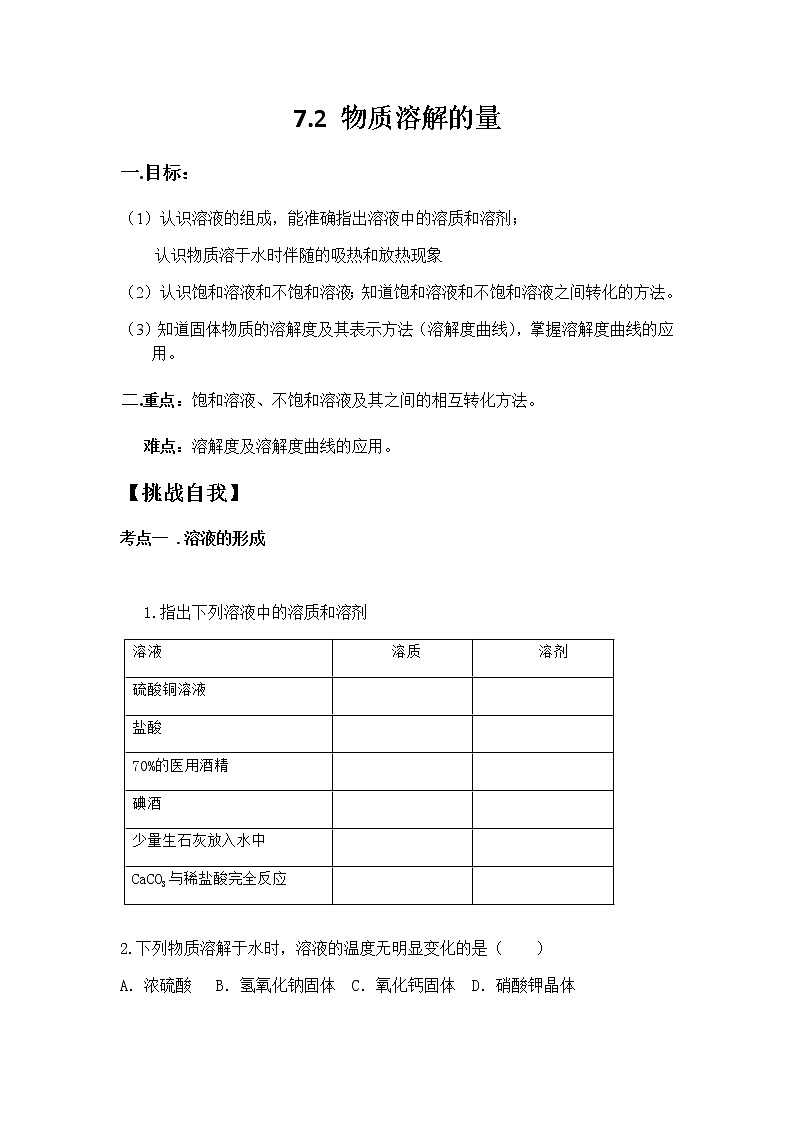
一.目标:
(1)认识溶液的组成,能准确指出溶液中的溶质和溶剂;
认识物质溶于水时伴随的吸热和放热现象
(2)认识饱和溶液和不饱和溶液;知道饱和溶液和不饱和溶液之间转化的方法。
(3)知道固体物质的溶解度及其表示方法(溶解度曲线),掌握溶解度曲线的应用。
二.重点:饱和溶液、不饱和溶液及其之间的相互转化方法。
难点:溶解度及溶解度曲线的应用。
【挑战自我】
考点一 .溶液的形成
1.指出下列溶液中的溶质和溶剂
溶液 | 溶质 | 溶剂 |
硫酸铜溶液 |
|
|
盐酸 |
|
|
70%的医用酒精 |
|
|
碘酒 |
|
|
少量生石灰放入水中 |
|
|
CaCO3与稀盐酸完全反应 |
|
|
2.下列物质溶解于水时,溶液的温度无明显变化的是( )
A.浓硫酸 B.氢氧化钠固体 C.氧化钙固体 D.硝酸钾晶体
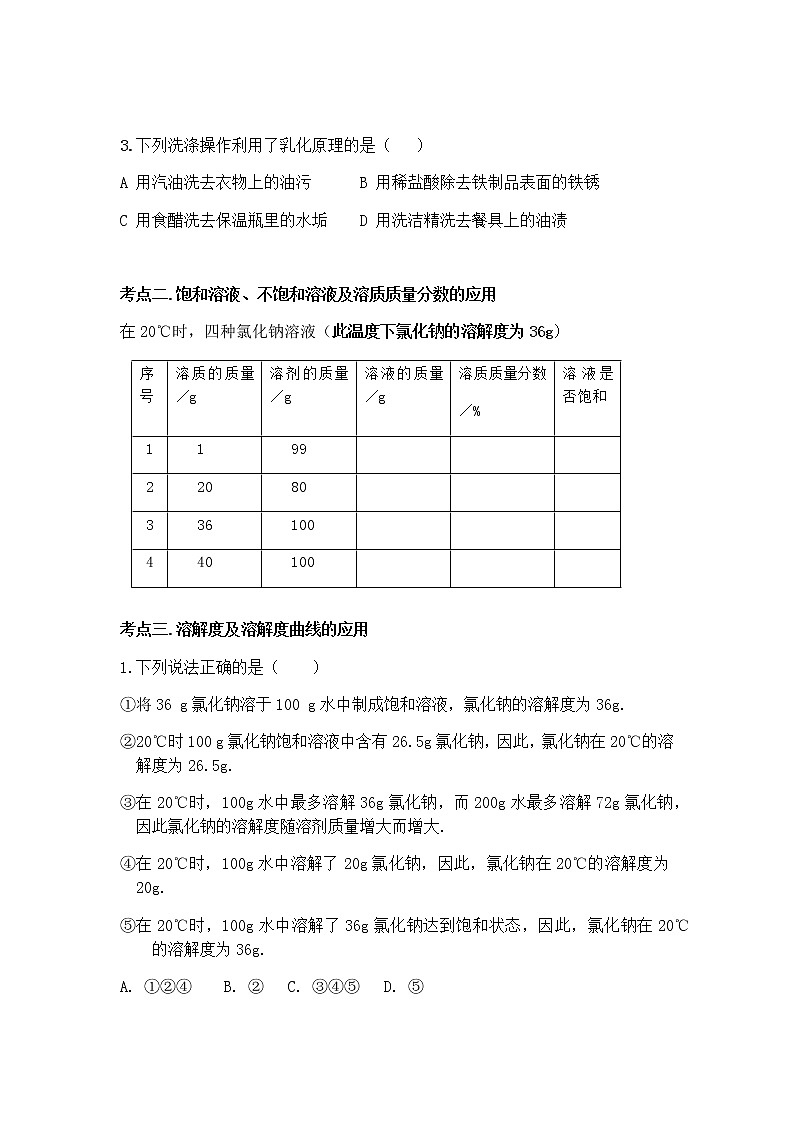
3.下列洗涤操作利用了乳化原理的是( )
A 用汽油洗去衣物上的油污 B 用稀盐酸除去铁制品表面的铁锈
C 用食醋洗去保温瓶里的水垢 D 用洗洁精洗去餐具上的油渍
考点二.饱和溶液、不饱和溶液及溶质质量分数的应用
在20℃时,四种氯化钠溶液(此温度下氯化钠的溶解度为36g)
序号 | 溶质的质量/g | 溶剂的质量/g | 溶液的质量/g | 溶质质量分数 /% | 溶液是否饱和 |
1 | 1 | 99 |
|
|
|
2 | 20 | 80 |
|
|
|
3 | 36 | 100 |
|
|
|
4 | 40 | 100 |
|
|
|
考点三.溶解度及溶解度曲线的应用
1.下列说法正确的是( )
①将36 g氯化钠溶于100 g水中制成饱和溶液,氯化钠的溶解度为36g.
②20℃时100 g氯化钠饱和溶液中含有26.5g氯化钠,因此,氯化钠在20℃的溶解度为26.5g.
③在20℃时,100g水中最多溶解36g氯化钠,而200g水最多溶解72g氯化钠,因此氯化钠的溶解度随溶剂质量增大而增大.
④在20℃时,100g水中溶解了20g氯化钠,因此,氯化钠在20℃的溶解度为20g.
⑤在20℃时,100g水中溶解了36g氯化钠达到饱和状态,因此,氯化钠在20℃的溶解度为36g.
A. ①②④ B. ② C. ③④⑤ D. ⑤
2. 如右图,M、N点表示的意义分别为
M :_______________________________
N :_______________________________
3.根据右图的溶解度曲线,请回答(1)20℃时,往50g水中加入20g硝酸钾晶体,充分搅拌后得到溶液质量为______ g。
(2)20℃时,欲配制等质量的两种物质的饱和溶液,所需水的质量关系是NaCl _______ KNO3 (填写“>”、“<”或“=”,下同) 。
4. A、B、C三种固体物质(均不含结晶水)的溶解度曲线如右图示,下列说法不正确的是( )
A.t1℃,将A、B、C各a g放入100g水中,充分搅拌,所得溶液溶质质量分数均相等
B.将t3℃时A、B、C的饱和溶液分别降温到t2℃时,所得溶液中溶质质量分数的关系为A> B > C
C. t2℃时,三种物质的溶液中溶质的质量分数相等
D.从A与少量C的混合物中提纯A,可用降温结晶的方法
当堂检测:
1. 要想把一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,具体措施有:①加入氢氧化钙 ②升高温度、③降低温度、④加入水、 ⑤蒸发水后再恢复到原温度、⑥加入生石灰。其中措施正确的是( )。
A.②④⑥ B.③④ C.①③⑤⑥ D.①②⑤⑥
2.⑴将一定质量的锌粒放入一定量的稀硫酸中,恰好完全反应后,所得溶液中:溶质是______,溶剂是_____。
⑵ 若将一定质量的锌粒放入过量稀硫酸中,完全反应后, 所得溶液中:溶质是_______,溶剂是_______。
⑶ 若将一定质量的锌粒放入稀硫酸中,完全反应后锌粒有剩余,所得液体中溶质是_____,溶剂是______。
3.A、B、C三只烧杯中分别装入等质量的水,在相同温度下,向三只烧杯中分别加入25g、15g、5g同种固体物质,充分溶解后,静置,现象如图所示,回答下列问题(填烧杯编号):
(1)A、B、C三只烧杯中的溶液一定是不饱和溶液的是 。
(2)A、B、C三只烧杯中溶液的溶质质量分数的大小关系是 。
4.右图是a、b、c三种物质的溶解度曲线,
a与c的溶解度曲线相交于P点。据图回答:
(1).P点的含义是 。
(2).t2℃时30g a物质加入到50g水中不断搅拌,
能形成80g溶液吗? (填写“能”或“不能”)
⑶.t2℃时a、b、c三种物质的溶解度按由小到大的顺序排列是 (填写物质序号)。
(4).将t1℃时a、c饱和溶液升高到t2℃时,有晶体析出的是___,有晶体析出的是___。
(5).t2℃时,将b物质的不饱和溶液转变成饱和溶液可采取的方法有____________________。
(6).t1℃时a、b、c三种物质恰好饱和的溶液的温度升高到t2℃时的三种溶液的溶质质量分数大小关系是( )
A. c>D.b B. a=b>c C. a>b>c D.b>a>c
(7).要从b溶液中分离b,你认为采用下列哪种方法更合理( )
A蒸发溶、B降温结晶
科粤版7.2 物质溶解的量导学案: 这是一份科粤版<a href="/hx/tb_c12502_t4/?tag_id=42" target="_blank">7.2 物质溶解的量导学案</a>,文件包含第72课物质溶解的量-九年级化学下册同步精品讲义科粤版教师版docx、第72课物质溶解的量-九年级化学下册同步精品讲义科粤版学生版docx等2份学案配套教学资源,其中学案共30页, 欢迎下载使用。
初中化学科粤版九年级下册第七章 溶液7.4 结晶现象导学案: 这是一份初中化学科粤版九年级下册第七章 溶液7.4 结晶现象导学案,共2页。学案主要包含了学习过程设计,[布置作业],【反思与收获】等内容,欢迎下载使用。
科粤版九年级下册8.5 化学肥料学案及答案: 这是一份科粤版九年级下册8.5 化学肥料学案及答案,共4页。学案主要包含了自主预习,合作探究,训练巩固,作业,教学反思/学后心得等内容,欢迎下载使用。













