

初中化学第四节 酸碱中和反应课后练习题
展开
这是一份初中化学第四节 酸碱中和反应课后练习题,共11页。试卷主要包含了单选题,判断题,填空题,综合应用题等内容,欢迎下载使用。
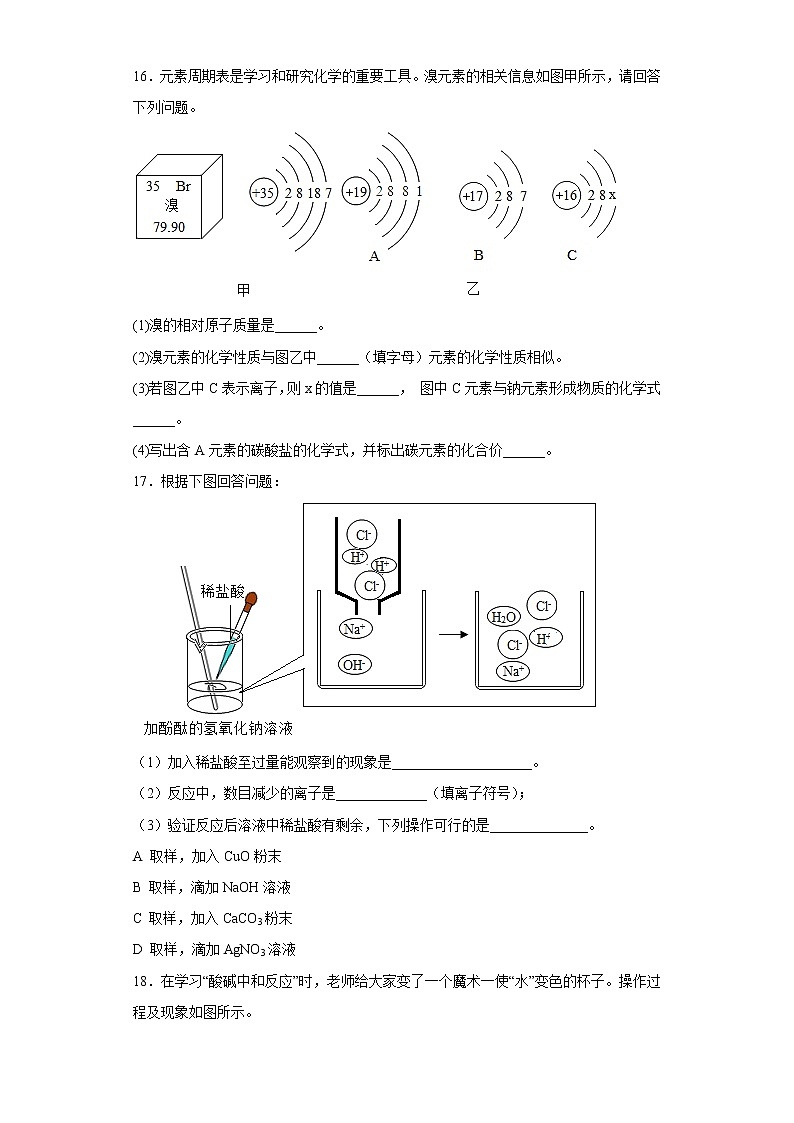
7.4酸碱中和反应同步练习鲁教版化学九年级下册学校:___________姓名:___________班级:___________考号:___________ 一、单选题1.分类思想是化学研究中常用的方法。现有:①水蒸气②石灰水③原油④食盐⑤氢氧化钠⑥液态氧。对上述物质的分类全部正确的是A.盐—②④ B.纯净物—①④⑥ C.碱—②⑤ D.混合物—②③④2.某化学小组利用数字化传感器探究稀盐酸和氢氧化钠溶液的反应过程,测得烧杯中溶液的pH随滴加液体体积变化的曲线如图所示。下列说法错误的是A.该实验是将氢氧化钠溶液滴入稀盐酸中B.a点所示溶液中,溶质只有NaClC.b点表示稀盐酸和氢氧化钠溶液恰好完全反应D.向点c所示溶液中滴加紫色石蕊溶液,溶液变蓝色3.我国神舟载人飞船供氧系统中含有下列物质,其中属于氧化物的是A.O2 B.CO2 C.NaOH D.Na2CO34.“一带一路”赋予古丝绸之路崭新的时代内涵。古代染坊常用下列物质中的一种盐来处理丝绸,这种盐是A.熟石灰 B.碳酸钾 C.乙醇 D.烧碱5.下列指定反应的化学方程式正确的是A.镁条燃烧:B.铜绿分解:C.氨水中和硫酸:D.酒精完全燃烧:6.下列常用来改良酸性土壤的物质是A.熟石灰B.硫酸C.烧碱D.食盐7.黄蜂的毒液呈碱性,若被黄蜂蜇了,涂抹下列物质可缓解疼痛的是A.食盐水(pH≈7 ) B.牙膏(pH≈9) C.肥皂(pH≈10 ) D.米醋(pH≈3)8.下图是生活中常见洗涤用品的 pH, 混用会降低去污效果的组合是A.洁厕灵和消毒液 B.肥皂水和炉具清洁剂C.消毒液和肥皂水 D.消毒液和炉具清洁剂9.推理是化学学习的重要方法,下列推理正确的是A.酸雨的pH小于5.6,则pH小于5.6的雨水一定是酸雨B.中和反应生成盐和水,则生成盐和水的反应一定是中和反应C.碱溶液能使酚酞溶液变红,则能使酚酞溶液变红的一定是碱溶液D.溶液具有均一性和稳定性,则具有均一性和稳定性的液体一定是溶液10.有关中和反应的说法一定正确的是( )A.反应物均须溶于水B.有沉淀生成C.有气体生成D.有盐生成 二、判断题11.碳酸氢钠是酸不是盐。( )12.酸溶液显酸性,所以显酸性的溶液一定是酸溶液( )13.组成中含有碳酸根离子的盐称为碳酸盐。____14.H+和OH-能结合成H2O,故H2O由H+和OH-构成( )15.所有生成盐和水的化学反应都是中和反应。( ) 三、填空题16.元素周期表是学习和研究化学的重要工具。溴元素的相关信息如图甲所示,请回答下列问题。(1)溴的相对原子质量是______。(2)溴元素的化学性质与图乙中______(填字母)元素的化学性质相似。(3)若图乙中C表示离子,则x的值是______, 图中C元素与钠元素形成物质的化学式______。(4)写出含A元素的碳酸盐的化学式,并标出碳元素的化合价______。17.根据下图回答问题:(1)加入稀盐酸至过量能观察到的现象是____________________。(2)反应中,数目减少的离子是_____________(填离子符号);(3)验证反应后溶液中稀盐酸有剩余,下列操作可行的是______________。A 取样,加入CuO粉末B 取样,滴加NaOH溶液C 取样,加入CaCO3粉末D 取样,滴加AgNO3溶液18.在学习“酸碱中和反应”时,老师给大家变了一个魔术一使“水”变色的杯子。操作过程及现象如图所示。老师揭秘:“空”杯子底部事先涂抹了某种无色液体,无色的“水”是事先用两种无色溶液混合而成。请回答下列问题:(1)“空”杯内涂抹的物质可能是_____________溶液。(2)此过程中发生反应的化学方程式可能是_________________________________。(3)最终溶液为无色,能否说明该溶液一定呈中性?_________(选填“能”或“不能”),理由是____________________________________________________。19.如下图所示,在白色点滴板1-6的孔穴中,分别滴加2滴紫色石蕊溶液。(1)孔穴6中溶液变为蓝色,说明碳酸钾溶液显____________(填“酸性”或“碱性”)。(2)溶液变为红色的孔穴有____________(填孔穴序号,下同)。(3)作为空白对照实验的孔穴是____________。(4)再向孔穴4中滴加稀硫酸,溶液变为紫色,用化学方程式解释其原因:____________。20.向盛有一定量澄清石灰水的烧杯中逐滴滴加稀盐酸,用pH传感器测得溶液的pH随加入稀盐酸的质量的变化曲线如图所示:(1)当加入稀盐酸质量为30g时,溶液中溶质的成分为_____________(填化学式)。(2)若把原烧杯中澄清石灰水换为等质量、等溶质质量分数的氢氧化钠溶液进行该实验,则pH传感器测得的曲线可能经过_____________(填“a”“b”或“c”)点。 四、综合应用题21.某品牌炉具清洁剂的有效成分是氢氧化钠,化学兴趣小组的同学测定该炉具清洁剂中氢氧化钠的含量。取100g炉具清洁剂倒入烧杯中,逐次加入质量分数为9.8%的稀硫酸,测出溶液的pH随加入稀硫酸的质量变化关系如图一所示。用温度计测量溶液温度变化如图二所示(不考虑反应过程中热量损失)。试回答:(1)当pH=_________时,溶液中所含的溶质只有Na2SO4。(2)浓硫酸常用作O2、CO2等气体干燥剂,说明浓硫酸具有_________性,此过程发生的是_________变化。(填“物理”或“化学”)(3)根据图二温度变化情况,可以判断该反应是_________反应。(填“吸热”或“放热”)(4)计算该炉具清洁剂中氢氧化钠的质量分数(写出计算过程)。22.硫酸是世界上产量最大、用途最广的酸,被称为“化学工业之母”。化学兴趣小组同学对硫酸进行了多角度的研究。【物质制备】(1)工业上采用接触法制硫酸:先煅烧黄铁矿得到SO2,再将SO2经过一系列变化得到硫酸。SO2中硫元素的化合价是_______________。【物质性质】(2)用温度计的水银球一端蘸取浓硫酸,取出后在空气中放置一段时间,观察到温度计示数上升,是因为浓硫酸能吸收____________,并放出热量。(3)请利用下图提供的仪器与药品,探究稀硫酸与氢氧化钠溶液的反应。①取____________(填“A”或“B”)中的氢氧化钠溶液5mL加入烧杯中,并插入pH计。②从另一试剂瓶中取出稀硫酸逐滴加入①的溶液中,并用____________(填仪器名称)不断搅拌。反应过程中溶液pH变化的部分数据如下表所示:稀硫酸体积/mL02468……溶液pH13.112.812.311.510.4…… ③在pH=12.8时,溶液中的溶质是____________(填化学式)。④滴加稀硫酸过程中,溶液pH不断减小的原因有:a.硫酸与氢氧化钠发生了反应;b.______⑤为证明溶液pH从13.1减小到10.4的过程中,④中原因a起主要作用,需设计的实验方案是____________。【定量研究】(4)某工厂现有含碳酸钠的废水需要处理。为测定废水中碳酸钠的质量分数,化学兴趣小组同学取废水样品100g,加入溶质质量分数为10%的硫酸溶液9.8g,恰好完全反应,反应的化学方程式: (此废水中其他物质不与硫酸反应)。计算废水中碳酸钠的质量分数(写出计算过程)。23.化学调研小组的同学用氢氧化钠和稀盐酸探究中和反应,请你参与以下探究:(1)甲组同学取少量的氢氧化钠溶液于烧杯中,用酸度计测得该溶液的pH,同时插入一支温度计,测量溶液的温度(如图1)。用胶头滴管吸取稀盐酸,逐滴加入盛有氢氧化钠溶液的烧杯中,边滴加边搅拌。此时可观察到的现象是酸度计上显示的数据逐渐________(填“增大”“减小”或“不变”),温度计上显示的数据逐渐升高,由此可知,酸和碱的中和反应属于________(填“吸热”或“放热”)反应。(2)乙组的同学改用固体氢氧化钠与稀盐酸反应来探究中和反应中能量的变化情况,你认为该方案________(填“合理”或“不合理”),原因是________________________________。(3)丙组同学用另外一瓶氢氧化钠溶液进行实验时,当往烧杯中滴加稀盐酸时,发现有少量的气泡冒出,小组同学根据这一现象进行讨论,一致认为其原因可能是氢氧化钠溶液已经变质,原因是________________________________(写化学方程式)。(4)丁组同学借助酚酞试液来判断氢氧化钠溶液与稀盐酸发生中和反应时,在烧杯中加入氢氧化钠溶液后,滴几滴酚酞溶液,然后加入一定量稀盐酸,最后溶液为无色。小金认为溶液显中性。小东认为不一定,小东同学设计以下实验进行了验证,结果否定小金的结论:实验步骤实验现象结论________________________________________________________ (5)戊组同学对本地化工厂排放废水中的盐酸含量进行了测定。取废水50 g,用质量分数为20%的氢氧化钠溶液进行中和,如图2所示。请你计算废水中盐酸的溶质质量分数__________________。(写出具体的计算过程)
参考答案:1.D2.B3.B4.B5.D6.A7.D8.A9.A10.D11.×12.错误13.正确 14.错误15.×16.(1)79.90(2)B(3) 8 Na2S (4) 17. 溶解由红色变为无色 H+、OH- ABC18. NaOH(或氢氧化钠) NaOH +HCl=NaCl+H2O 不能 酚酞在酸性和中性条件下均显无色19. 碱性 2、5 3 2NaOH + H2SO4= Na2SO4+ 2H2O20.(1)CaCl2、HCl(2)a 21.(1)7(2) 吸水 物理(3)放热(4)设该炉具清洁剂中氢氧化钠的质量分数为x, x=4%,答:该炉具清洁剂中氢氧化钠的质量分数为4%。 22.(1)+4 (2)水蒸气 (3) A 玻璃棒 NaOH、Na2SO4 水稀释氢氧化钠溶液 取等质量的pH=13.1的两烧杯氢氧化钠溶液,一杯加入稀硫酸直至pH=10.4,记录加入稀硫酸的质量。另一杯加入蒸馏水直至pH=10.4,记录加入蒸馏水的质量(4)解:加入硫酸的质量为9.8g×10%=0.98g设废水中碳酸钠的质量为x碳酸钠的质量分数为。答:废水中碳酸钠的质量分数是1.06%。 23.(1) 减小 放热(2) 不合理 固体氢氧化钠溶于水会放出热量(3)CO2+2NaOH=Na2CO3+H2O(4) 取少量反应后的溶液于试管中,滴加几滴紫色的石蕊试液 石蕊试液变红色 溶液显酸性(5)解∶设废水中盐酸的溶质质量分数x x=7.3%答∶废水中盐酸的溶质质量分数是7.3%。
相关试卷
这是一份鲁教版九年级下册第七单元 常见的酸和碱第四节 酸碱中和反应巩固练习,共9页。试卷主要包含了选择题,判断题,综合应用题等内容,欢迎下载使用。
这是一份初中化学鲁教版 (五四制)九年级全册4 酸碱中和反应随堂练习题,共14页。试卷主要包含了单选题,填空题,实验题等内容,欢迎下载使用。
这是一份初中化学鲁教版 (五四制)九年级全册4 酸碱中和反应课时训练,共12页。试卷主要包含了单选题,填空题,实验题等内容,欢迎下载使用。











