



人教版 (2019)第四章 物质结构 元素周期律第一节 原子结构与元素周期表示范课课件ppt
展开核能聚变:将两个或更多轻原子核融合成一个较重原子核的核反应。该反应,能放出很大的能量,且污染轻,不会产生有害的放射性垃圾。例如,1g 21 H聚变成 31 H或氦原子放出可使4×108g冰变成水蒸气的热量。
未来的能源---核能聚变
1904年,汤姆孙发现:金属在高压电的条件下,会释放出一种偏离负电荷的粒子。且该粒子的质量约为最轻的原子-----氢原子质量的1/1836。
结论:原子中存在带负电的、质量极小的粒子-----电子。
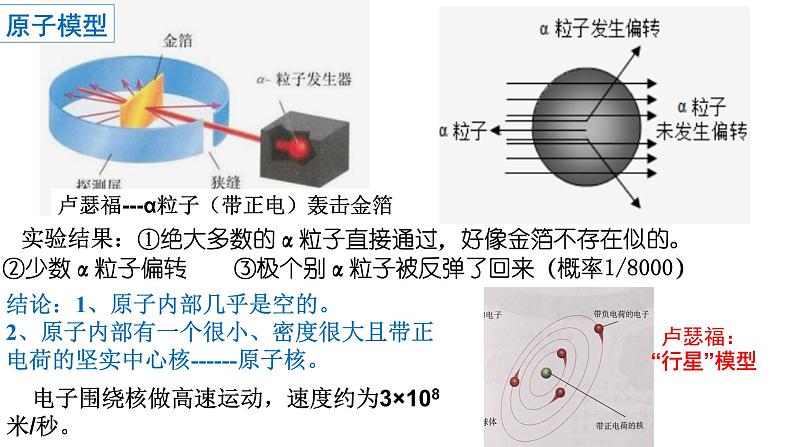
卢瑟福---α粒子(带正电)轰击金箔
实验结果:①绝大多数的α粒子直接通过,好像金箔不存在似的。 ②少数α粒子偏转 ③极个别α粒子被反弹了回来(概率1/8000)
结论:1、原子内部几乎是空的。2、原子内部有一个很小、密度很大且带正电荷的坚实中心核------原子核。
电子围绕核做高速运动,速度约为3×108米/秒。
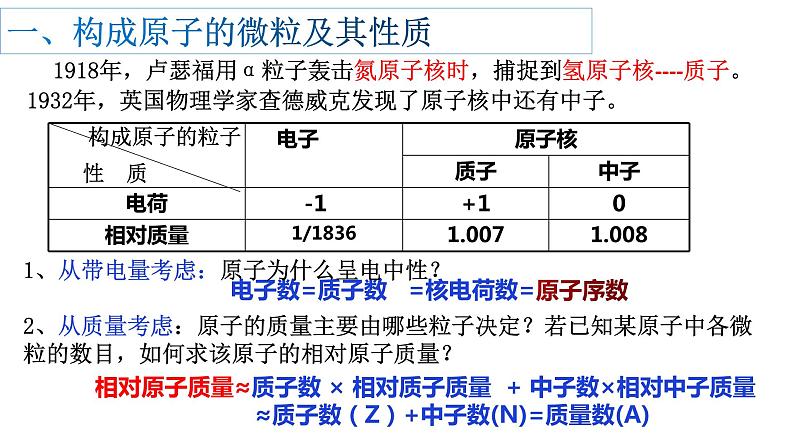
1918年,卢瑟福用α粒子轰击氮原子核时,捕捉到氢原子核----质子。 1932年,英国物理学家查德威克发现了原子核中还有中子。
一、构成原子的微粒及其性质
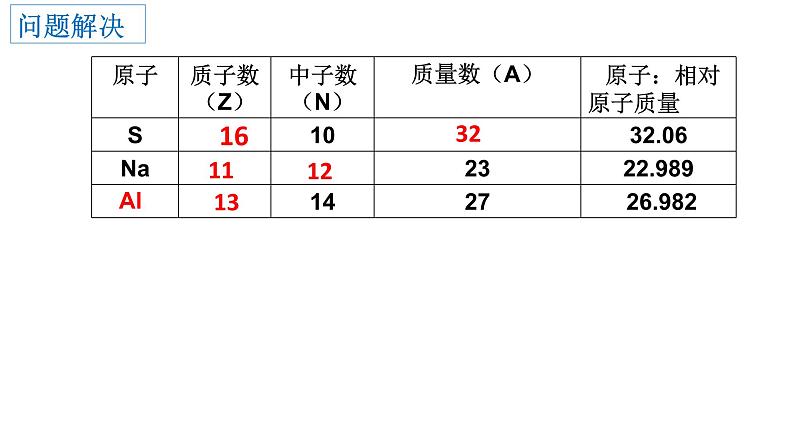
相对原子质量≈质子数 × 相对质子质量 + 中子数×相对中子质量 ≈质子数(Z)+中子数(N)=质量数(A)
1、从带电量考虑:原子为什么呈电中性? 2、从质量考虑:原子的质量主要由哪些粒子决定?若已知某原子中各微粒的数目,如何求该原子的相对原子质量?
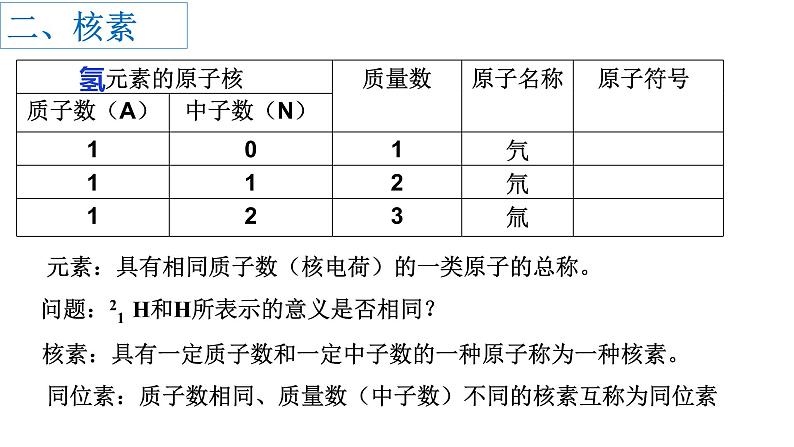
元素:具有相同质子数(核电荷)的一类原子的总称。
问题:21 H和H所表示的意义是否相同?
核素:具有一定质子数和一定中子数的一种原子称为一种核素。
同位素:质子数相同、质量数(中子数)不同的核素互称为同位素
思考:1、离子中质子数和电子数是否相等?离子所带电荷数与离子中含有的质子数和电子数有什么关系?
离子: 质子数≠电子数 电荷数 = 质子数 - 电子数
用符号表示下列各微粒:
2、上述有几种核素?互为同位素的是哪些?
氢元素:氕(H)、氘(D,重氢)、氚(T,超重氢)、、、碳元素:12C、13C、 14C(有放射性)、、、、、、氧元素:16O、17O、18O、、、、、、、铀元素:234U、235U、238U、、、、、、核素分天然同位素和人工合成的同位素用途:1、考古研究员:14C用于考古断代 2、D、T用于制造氢弹, 3、235U是制造原子弹的材料和核反应堆的原料。 4、具有放射性的同位素可用于追踪 5、课后查阅其他用途。
我们把电子运动的这些区域简化为不连续的壳层,也称电子层。
1、K层为最外电子层时,最多能容纳————个电子。K层以外的电子层做最外电子层时,最多能容纳————个电子。 次外电子层最多可容纳————个电子。倒数第三电子层最多可容纳————个电子2、最多容纳能的电子数:K层_____、L层_____、M层_____、N层_____.你能归纳出第n层最多能容纳的电子数:________3、核外电子总是先排____层,排满后,再排____层,即由————往———(填内、外)。4、如何表示原子的核外电子排布?
1、写出Na、S、Ar的原子结构示意图
2、写出Ca(原子序数:20)、Br(原子序数:35)的原子结构示意图
3、写出Na+、K+、O2—、Cl—的离子结构示意图
4、与Ne电子层结构相同的微粒有哪些?与Ar、He呢?
5、某元素原子核外M层电子数是L层电子数的1/2,该元素为:________ 某元素原子的最外层电子数是次外层电子数的2倍,元素为:___ __
1、结合原子结构讨论:为什么钠的最高价是+1?氯的最低价是-1,最高价是+7?2、为什么氯化钠中钠离子和氯离子的比例是1:1, 氯化镁中镁离子和氯离子的比例是1:2?
结论:1、元素化合价与元素原子最外层电子有关,与形成8电子( 单层2电子)稳定结构有关。
元素的主要化合价与原子的最外层电子数的关系: 金属、非金属元素:最高化合价=原子最外层电子数(除O、F) 活泼非金属元素:最低化合价=最外层电子数- 8(除H)
1、电子没有确定的轨迹,不能同时准确地测定电子在某一时刻所处的位置和运动速度,也不能描绘出它的运动轨迹。
2、只能用统计的观点指出它在原子核外空间某处出现机会的多少。“电子云”形象地描述核外电子的运动。
化学人教版 (2019)第四章 物质结构 元素周期律第一节 原子结构与元素周期表完美版课件ppt: 这是一份化学人教版 (2019)<a href="/hx/tb_c161996_t3/?tag_id=26" target="_blank">第四章 物质结构 元素周期律第一节 原子结构与元素周期表完美版课件ppt</a>,共23页。PPT课件主要包含了原子的构成,原子核外电子排布,本节重点,本节难点,原子结构的探索历程,原子核,核外电子,带1个单位正电荷,不带电,带1个单位负电荷等内容,欢迎下载使用。
高中化学人教版 (2019)必修 第一册第四章 物质结构 元素周期律第一节 原子结构与元素周期表教学课件ppt: 这是一份高中化学人教版 (2019)必修 第一册第四章 物质结构 元素周期律第一节 原子结构与元素周期表教学课件ppt,共34页。PPT课件主要包含了素养要求,原子结构,原子核外电子,当堂练习等内容,欢迎下载使用。
高中化学第一节 原子结构与元素周期表备课ppt课件: 这是一份高中化学第一节 原子结构与元素周期表备课ppt课件,共27页。PPT课件主要包含了电子层,“四素”的区别等内容,欢迎下载使用。














