

苏教版 (2019)选择性必修1专题1 化学反应与能量第一单元 化学反应的热效应学案
展开一、能源的充分利用
1.能源定义:能提供能量的自然资源
2.分类
3.我国目前使用的主要能源是化石燃料
4.新能源的特点:资源丰富、可再生、无污染或少污染。
(正确的打“√”,错误的打“×”)
(1)太阳能是可再生的新能源(√)
(2)现在家庭使用的天然气是清洁的新能源(×)
(3)我国目前使用的主要能源是新能源(×)
(4)化石燃料包括氢能、石油、天然气(×)
二、标准燃烧热和热值
1.标准燃烧热
(1)概念:在101 kPa下,1 ml物质完全燃烧的反应热叫做该物质的标准燃烧热。
(2)完全燃烧的标准:N→N2(g)、H→H2O(l)、C→CO2(g)。
(3)单位:标准燃烧热是反应热的一种,单位为kJ·ml-1或kJ/ml。
微点拨:标准燃烧热是反应热的一种类型,标准燃烧热规定可燃物必须是1 ml,生成物必须是稳定产物。
2.热值:1 g物质完全燃烧的反应热叫做该物质的热值。
3.标准燃烧热和热值的意义
标准燃烧热或热值可以衡量燃料燃烧放出热量的大小
(正确的打“√”,错误的打“×”)
(1)在101 kPa下,1 ml纯物质完全燃烧所放出的热量就是其燃烧热(×)
(2)1 ml H2完全燃烧生成1 ml水蒸气时放出的热量为H2的燃烧热(×)
(3)表示燃烧热的热化学方程式可以有无数个(×)
(4)燃烧热的数值与参与反应的可燃物的物质的量成正比(×)
(5)所有物质的燃烧热其ΔH均小于0 (√)
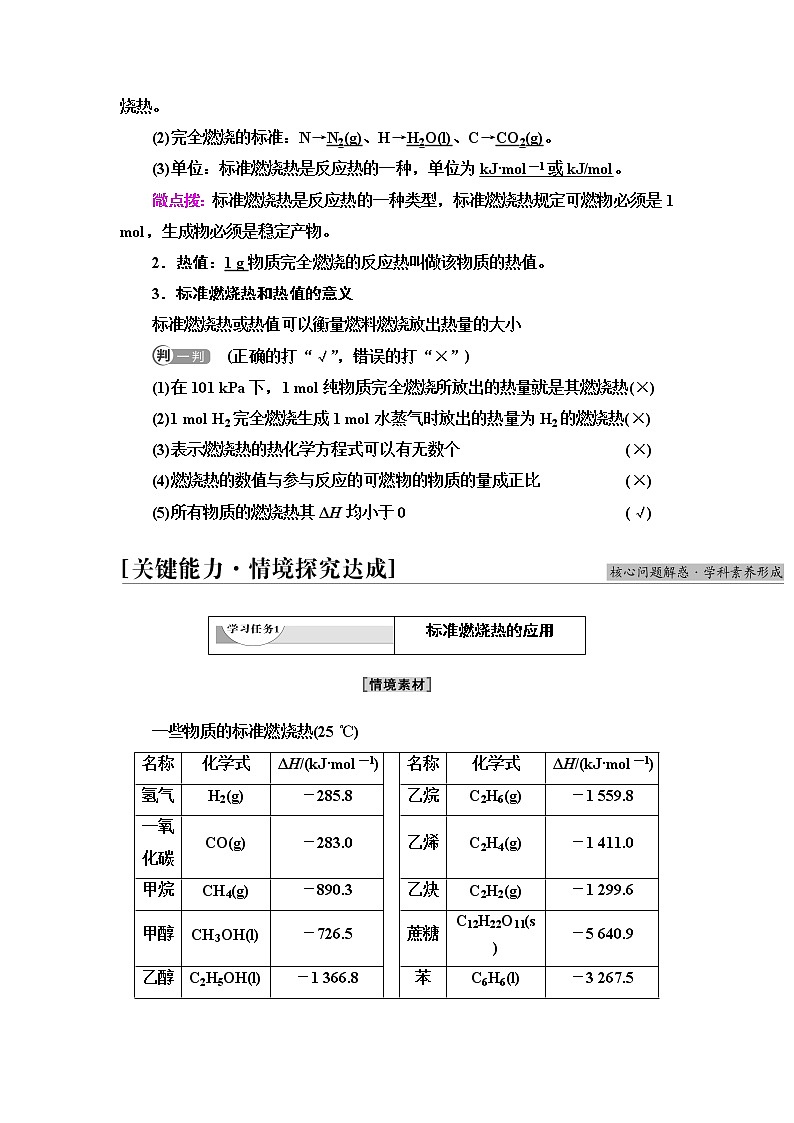
一些物质的标准燃烧热(25 ℃)
[问题1] 由上述表中数据可知甲烷的标准燃烧热为多少?意义是什么?
[提示] 甲烷的标准燃烧热为890.3 kJ·ml-1,或ΔH=-890.3 kJ·ml-1,它表示25 ℃、101 kPa时,1 ml甲烷完全燃烧生成1 ml CO2(g)和2 ml H2O(l)时放出890.3 kJ的热量。
[问题2] 以H2为例,写出表示H2标准燃烧热的热化学方程式?表示标准燃烧热的热化学方程式与一般热化学方程式有什么不同?
[提示] 表示 H2标准燃烧热的热化学方程式为:H2(g)+eq \f(1,2)O2(g)===H2O(l) ΔH=-285.8 kJ·ml-1。书写表示标准燃烧热的热化学方程式时,以燃烧1 ml可燃物为标准来配平其余物质的化学计量数,同时可燃物要完全燃烧且生成指定产物。
[问题3] 如何判断表示标准燃烧热的热化学方程式正误?
[提示] “一看”可燃物的化学计量数是否为1。“二看”元素完全燃烧生成的物质是否为指定产物。“三看”ΔH是否为“-”及单位是否正确。
[问题4] 利用表中数据,计算1 kg CH4在25 ℃、101 kPa时充分燃烧生成液态水放出的热量约为多少?
[提示] 1 kg甲烷的物质的量为62.5 ml,甲烷的标准燃烧热为890.3 kJ·ml-1,说明1 ml CH4在25 ℃、101 kPa时充分燃烧生成液态水放出的热量为890.3 kJ,则62.5 ml甲烷在25 ℃,101 kPa时充分燃烧生成液态水放出的热量为:890.3 kJ·ml-1×62.5 ml≈5.56×104 kJ。
1.标准燃烧热及表示标准燃烧热的热化学方程式
(2)燃烧热是以1 ml物质完全燃烧所放出的热量来定义的,因此在书写表示燃烧热的热化学方程式时,应以燃烧1 ml物质为标准来配平其余物质的化学计量数,故在其热化学方程式中常出现分数。
2.利用燃烧热可计算一定量燃料燃烧能放出多少热量,Q=n(燃料)×标准燃烧热
3. 反应热和标准燃烧热的比较
4.标准燃烧热和中和热的比较
1.下列说法正确的是( )
A.1 ml硫酸与1 ml Ba(OH)2完全中和所放出的热量为中和热
B.25 ℃、101 kPa时,1 ml S和2 ml S的标准燃烧热相等
C.CO是不稳定的氧化物,它能继续和氧气反应生成稳定的CO2,所以CO的燃烧反应一定是吸热反应
D.101 kPa时,1 ml碳燃烧所放出的热量为碳的标准燃烧热
B [A项,1 ml H2SO4与1 ml Ba(OH)2反应生成2 ml H2O,同时还有BaSO4沉淀生成,不符合中和热的定义;B项,标准燃烧热与可燃物的物质的量无关;C项,CO的燃烧属于放热反应;D项,1 ml碳燃烧不一定生成1 ml CO2。]
2.25 ℃、101 kPa下,碳、氢气、甲烷和葡萄糖的标准燃烧热依次是393.5 kJ·ml-1、285.8 kJ·ml-1、890.3 kJ·ml-1、2 800 kJ·ml-1,则下列热化学方程式正确的是( )
A.C(s)+eq \f(1,2)O2(g)===CO(g)
ΔH=-393.5 kJ·ml-1
B.2H2(g)+O2(g)===2H2O(g)
ΔH=571.6 kJ·ml-1
C.CH4(g)+2O2(g)===CO2(g)+2H2O(g)
ΔH=-890.3 kJ·ml-1
D.eq \f(1,2)C6H12O6(s)+3O2(g)===3CO2(g)+3H2O(l)
ΔH=-1 400 kJ·ml-1
D [根据标准燃烧热的定义,碳的燃烧产物应是CO2;氢气燃烧是放热反应(ΔH<0)且生成液态水;25 ℃时甲烷的燃烧产物是CO2(g)和H2O(l)。]
1.如图为“能源分类相关图”,四组能源选项中全部符合图中阴影部分的是( )
A.煤炭、石油、潮汐能
B.水能、生物质能、天然气
C.太阳能、风能、沼气
D.地热能、海洋能、核能
C [太阳能、风能、沼气这三种能源既是新能源、可再生能源,又是来自太阳的能源。]
2.下面均是正丁烷与氧气反应的热化学方程式(25 ℃,101 kPa):
①C4H10(g)+eq \f(13,2)O2(g)===4CO2(g)+5H2O(l)
ΔH=-2 878 kJ·ml-1
②C4H10(g)+eq \f(13,2)O2(g)===4CO2(g)+5H2O(g)
ΔH=-2 658 kJ·ml-1
③C4H10(g)+eq \f(9,2)O2(g)===4CO(g)+5H2O(l)
ΔH=-1 746 kJ·ml-1
④C4H10(g)+eq \f(9,2)O2(g)===4CO(g)+5H2O(g)
ΔH=-1 526 kJ·ml-1
由此判断,正丁烷的标准燃烧热ΔH为( )
A.-2 878 kJ·ml-1 B.-2 658 kJ·ml-1
C.-1 746 kJ·ml-1 D.-1 526 kJ·ml-1
A [标准燃烧热是指在25 ℃、101 kPa时,1 ml纯物质完全燃烧生成稳定氧化物时所放出的热量。因此正丁烷完全燃烧产物应为CO2(g)和H2O(l),所以正丁烷的标准燃烧热为ΔH=-2 878 kJ·ml-1。]
3.下列关于热化学反应的描述中正确的是( )
A.已知H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ·ml-1,则H2SO4和Ba(OH)2反应的反应热ΔH=2×(-57.3)kJ·ml-1
B.燃料电池中将甲醇蒸气转化为氢气的热化学方程式是CH3OH(g)+eq \f(1,2)O2(g)===CO2(g)+2H2(g) ΔH=-192.9 kJ·ml-1,则CH3OH(g)的燃烧热为192.9 kJ·ml-1
C.已知2H2O(g)===2H2(g)+O2(g) ΔH=+571.6 kJ·
ml-1,则H2(g)的燃烧热是285.8 kJ·ml-1
D.葡萄糖的燃烧热是2 800 kJ·ml-1,则eq \f(1,2)C6H12O6(s)+3O2(g)===3CO2(g)+3H2O(l) ΔH=-1 400 kJ·ml-1
D [A项中H2SO4与Ba(OH)2反应除有H+与OH-反应放热外,生成BaSO4沉淀亦放热,故ΔH<2×(-57.3)kJ·ml-1;B项中甲醇未完全生成稳定的氧化物,H元素应生成H2O(l);C项可表示为H2(g)+eq \f(1,2)O2(g)===H2O(g) ΔH=-285.8 kJ·ml-1,而水为气态,所以不是H2的燃烧热;D项燃烧热是指1 ml葡萄糖完全燃烧放出的热量,热化学方程式中C6H12O6(s)的化学计量数为eq \f(1,2),则ΔH=-1 400 kJ·ml-1。]
4.已知下列两个热化学方程式:2H2(g)+O2(g)===2H2O(l) ΔH=-571.6 kJ·ml-1
C3H8(g)+5O2(g)===3CO2(g)+4H2O(l) ΔH=-2 220 kJ·ml-1
请根据上面两个热化学方程式,回答下列问题:
(1)H2的标准燃烧热为______________,C3H8的标准燃烧热为________。
(2)1 ml H2和2 ml C3H8组成的混合气体完全燃烧释放的热量为____________________。
(3)现有H2和C3H8的混合气体共5 ml,完全燃烧时放热3 847 kJ,则在混合气体中H2和C3H8的体积比是________________。
[解析] (1)根据标准燃烧热的概念知H2、C3H8的标准燃烧热分别为285.8 kJ·ml-1、2 220 kJ·ml-1。
(2)完全燃烧释放的总能量的计算式为Q放=1 ml×285.8 kJ·ml-1+2 ml×2 220 kJ·ml-1=4 725.8 kJ。
(3)设H2、C3H8的物质的量分别为n1、n2,则有
eq \b\lc\{\rc\ (\a\vs4\al\c1(n1+n2=5 ml,n1×285.8 kJ·ml-1+n2×2 220 kJ·ml-1=3847 kJ))
解得n1=eq \f(15,4) ml,n2=eq \f(5,4) ml,在相同p、T时,V(H2)∶V(C3H8)=n(H2)∶n(C3H8)=3∶1。
[答案] (1)285.8 kJ·ml-1 2 220 kJ·ml-1
(2)4 725.8 kJ (3)3∶1
5.适量H2(g)在1 ml O2(g)中完全燃烧,生成2 ml H2O(l),放出571.6 k的热量。请写出表示H2标准燃烧热的热化学方程式____________________。
[解析] 根据题意知,氢气在1 ml O2(g)完全燃烧放出571.6 kJ的热量,则1 ml氢气完全燃烧放出的能量为285.8 kJ,氢气和氧气都是气态,水是液态,则表示H2标准燃烧热的热化学方程式为:H2(g)+eq \f(1,2)O2(g)===H2O(l) ΔH=-285.8 kJ·ml
[答案] H2(g)+eq \f(1,2)O2(g)===H2O(l) ΔH=-285.8 kJ·ml
学 习 任 务
1.通过了解化学在解决能源危机中的重要作用,培养科学态度与社会责任的化学核心素养。
2.通过在理解反应热的基础上,从宏观上理解辨识燃烧热的概念,学会关于燃烧热的相关计算,培养宏观辨识与微观探析的化学核心素养。
3.通过学习反应热大小的比较方法,培养证据推理与模型认知的化学核心素养。
标准燃烧热的应用
名称
化学式
ΔH/(kJ·ml-1)
名称
化学式
ΔH/(kJ·ml-1)
氢气
H2(g)
-285.8
乙烷
C2H6(g)
-1 559.8
一氧
化碳
CO(g)
-283.0
乙烯
C2H4(g)
-1 411.0
甲烷
CH4(g)
-890.3
乙炔
C2H2(g)
-1 299.6
甲醇
CH3OH(l)
-726.5
蔗糖
C12H22O11(s)
-5 640.9
乙醇
C2H5OH(l)
-1 366.8
苯
C6H6(l)
-3 267.5
反应热
燃烧热
能量的变化
放热或吸热
放热
ΔH的大小
放热时,ΔH<0;
吸热时,ΔH>0
ΔH<0
反应物的量
不限
1 ml纯物质
生成物
无要求
指定产物
热化学方程式
有无数个
唯一
燃烧热
中和热
相同点
能量变化ΔH及其单位
放热反应
ΔH<0,单位均为kJ·ml-1
不同点
反应物的量
1 ml
不一定为1 ml
生成物的量
不确定
生成水的量为1 ml
表示方法
燃烧热为a kJ·ml-1或
ΔH=-a kJ·
ml-1
中和热为57.3 kJ·
ml-1
或ΔH=-57.3 kJ·ml-1
2021学年专题1 化学反应与能量第一单元 化学反应的热效应导学案: 这是一份2021学年专题1 化学反应与能量第一单元 化学反应的热效应导学案,共15页。学案主要包含了反应热 焓变,热化学方程式,化学反应过程中能量变化的原因等内容,欢迎下载使用。
高中化学第三单元 金属的腐蚀与防护导学案及答案: 这是一份高中化学第三单元 金属的腐蚀与防护导学案及答案,共13页。学案主要包含了金属的电化学腐蚀,金属的电化学防护等内容,欢迎下载使用。
化学选择性必修3第一单元 醇和酚学案设计: 这是一份化学选择性必修3第一单元 醇和酚学案设计,共9页。学案主要包含了酚的概念及其代表物的结构,苯酚的性质和应用等内容,欢迎下载使用。













