
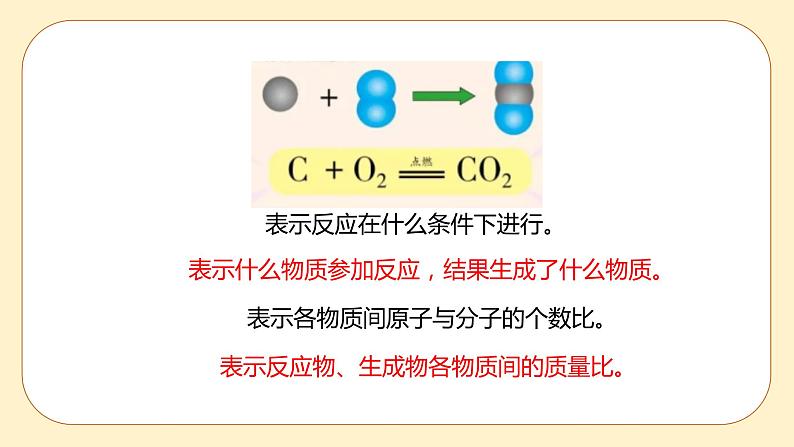








初中科学浙教版八年级下册第3节 化学方程式评优课ppt课件
展开3.3 化学方程式第2课时
一、选择题
1.“84 消毒液”可用于新冠状病毒肺炎的防疫,制备其主要成分次氯酸钠(NaClO)的化学方程式为:2NaOH+Cl2=NaClO+NaCl+X。则 X 的化学式是( )
A.ClO2 B.H2 C.H2O D.Na2O
2.《本草纲目》中记载:“(火药)乃焰消(KNO3)、硫磺、杉木炭所合,以为烽燧铳机诸点燃药者。”该反应的原理为:2KNO3+S+3C=K2S+N2↑+3X↑。下列说法正确的是( )
A.生成物X的化学式是CO2 B.火药是纯净物
C.该反应过程中会吸收大量热 D.反应后氮元素的化合价升高
3.将一个干冷的烧杯罩在打火机火焰的上方,烧杯内壁上出现细小的水珠;将烧杯迅速倒转过来,倒入少量澄清石灰水,振荡,石灰水变浑浊。由此可推断打火机液体中( )
A.一定含有碳、氢两种元素,可能含有氧元素 B.一定含有碳、氢、氧三种元素
C.一定含有碳、氢两种元素,肯定没有氧元素 D.无法判断
4.ClO2是安全消排剂,可由如下反应制取:2NaC1O2+Cl2= xClO2+2NaCl。则下列说法正确的是( )
A.ClO2的化学名称为氯化二氧
B.ClO2中氯元素的化合价为+2价
C.制取ClO2的反应属于化合反应
D.制取ClO2的反应中,x=2
5.在4P+5O22P2O5反应中,反应物和生成物各物质之间的质量比为( )
A.31∶32∶142 B.4∶5∶2 C.62∶80∶142 D.4∶10∶20
6.火柴头原本是一种不被磁铁吸引的物体,但火柴头烧过之后,却能被磁铁吸引。原因是很多火柴头用氧化铁着色,点燃后会与木棒中的碳反应产生四氧化三铁和二氧化碳等。由此作出的推测不合理的是( )
A.Fe3O4与Fe2O3磁性不同,体现它们物理性质不同
B.Fe3O4中铁的质量分数大于Fe2O3
C.火柴头燃烧的方程式为C+O2+6Fe2O34Fe3O4+CO2
D.火柴头原本不被磁铁吸引是因为不易被磁化
7.钴(Co)的化合物在锂电池中有很好的应用。如LiCoO2(钴酸锂)在酸性介质中会发生如下化学反应:2LiCoO2+H2O2+3H2SO4=Li2SO4+2CoSO4+4X+O2↑,该反应中Li元素的化合价始终为+1价。则下列说法正确的是( )
A.生成物X的化学式为LiOH B.LiCoO2中钴的化合价为+3价
C.生成物X会对环境造成污染 D.该反应中,只有Co元素的化合价发生变化
8.在“新型冠状病毒”的疫情防控过程中,场室常用“84消毒液”进行消毒。但如果将洁厕灵和“84消毒液”同时使用,则会发生如图所示的化学反应,下列说法正确的是( )
A.该反应属于分解反应
B.反应物和生成物中,属于氧化物的有2种
C.生成的有毒气体是Cl2
D.生成的有毒气体是ClO
9.加热158克高锰酸钾,当得到2克氧气时,剩余固体的成分是( )
A.K2MnO4和MnO2 B.KMnO4和MnO2
C.KMnO4、K2MnO4和MnO2 D.KMnO4和K2MnO4
10.物质M在4.8g氧气中恰好完全燃烧,反应方程式为M+3O2=RO2+2SO2,测得RO2和SO2的质量分别为2.2g和6.4g,下列判断中正确的是( )
A.参加反应的M的质量为4.3g
B.M的相对分子质量为76
C.M中含有R元素、S元素和O元素
D.产物为气态时都是空气污染物
二、填空题
11.金属Al既能与酸发生化学反应也能与碱溶液发生化学反应,与NaOH溶液反应的化学方程式为:2Al+2NaOH+2H2O =2NaAlO2+3X↑
(1)根据质量守恒定律,试推断X的化学式为___________。
(2)NaAlO2中Al的化合价为___________。
12.我国发明的新型钛合金,为“奋斗者”号下潜万米海底、从事科考任务解决了材料难题。工业制取金属钛的主要反应式是:
①2FeTiO3+6C+7Cl22FeCl3+2TiCl4+6CO
②2Mg+TiC142___________?___________+Ti
(1)TiCl4中Ti元素的化合价为___________。
(2)写出反应式②中“?”处的化学式为___________。
(3)工业生产中产生的废气、废水、废渣要统一进行处理,达到相应标准后才可以进行排放。请对①过程中产生的有毒气体的处理提出一种合理的意见:___________。
13.我国稀土资源丰富,某种稀土储氢材料(用M表示)的储氢原理可表示为 。M的化学式为___________。
14.配平下列化学方程式:
(1)______KClO3=______KCl+______O2↑
(2)______KMnO4=______K2MnO4+______MnO2+O2↑
(3)CH4+______O2=______H2O+______CO2
15.怎样才能让月球拥有大气层呢?科学家们分析月壤后发现,其主要成分包括SiO2、Al2O3、Fe2O3等。有人设计如图方案,给月球制造大气。
(1)电解器中,石墨用作反应物的同时,还充当电极,这是利用了它的___________(填一种物理性质);
(2)以A12O3为例,若电解中生成的两种气体(分子数为1:1)和一种金属单质(如图),则反应的化学方程式为___________。
16.人类早期发现的所有糖类分子式中氢和氧的比例和水一样,是2:1,将糖类都称为“碳水化合物”,后来发现,有些氢、氧原子个数比并不是2:1,如鼠李糖C6H12O5, 请据此回答下列问题:
(1)鼠李糖中氢、氧原子个数之比为___________。
(2)鼠李糖在氧气中充分燃烧,生成的水和二氧化碳质量比为___________。
17.发射神舟十三号载人飞船的运载火箭,使用液态四氧化二氮和偏二甲肼(C2H8N2)作为推进剂。四氧化二氮是一种无机物,为黄褐色液体或气体,有刺激性气味,具有强烈氧化性,常被用于作为火箭推进剂组分中的氧化剂。
(1)四氧化二氮中N元素的质量分数为__________(结果保留到小数点后一位)
(2)N2O4在物质分类中属于化合物中的__________,其中氮元素的化合价__________价。
(3)四氧化二氮和偏二甲肼发生的反应方程式为:C2H8N2+2N2O4=2CO2↑+3_____+4H2O↑,请在横线上把反应方程式补充完整。
三、探究题
18.为缓解旱情,乐清市开展了人工增雨作业,利用碘化银()进行人工降雨的基本原理是碘化银在高空分解生成银单质和碘单质(),形成人工冰核,这些冰核经过水汽凝聚形成冰晶,冰晶发展到一定程度将会下降形成雨滴.
(1)写出碘化银分解的化学反应方程式:______
(2)上述“冰晶下降形成雨滴”涉及到的物态变化是______
19.国家发改委废止《食盐专营许可证管理办法》,意味着食盐的经营将向私营企业开放。我国的食盐大多为加碘盐,某兴趣小组开展了食盐中碘含量的测定探究。
【查阅资料】
①在食盐中以碘酸钾()的形式存在。
②国家规定:食盐中碘含量(以I计)标准为20毫克/千克~50毫克/千克。
③碘酸钾与碘化钾反应生成碘单质,反应方程式为:
④质碘(I2)难溶于水,碘与碘化钾溶液混合后生成易溶的KI3。KI3仍保持碘单质的化学性质。
⑤淀粉溶液遇碘变蓝,淀粉的量充足时,颜色深浅度随碘含量变化而变化。
【实验探究】
步骤1:配制准备以下各种试剂:10克/100毫升食盐溶液、0.0254克/升碘溶液、10克/升淀粉溶液、196克/升稀硫酸、1.66克/升碘化钾溶液、蒸馏水。
步骤2:取10支5毫升的小试管,贴上编号标签,按表要求分别滴入碘溶液、蒸馏水和淀粉溶液,观察溶液颜色的变化情况,并有序放置在试管架上,留作对比用。
试管编号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
碘溶液滴数 | 27 | 24 | 21 | 18 | 15 | 12 | 9 | 6 | 3 | 0 |
蒸馏水滴数 | 0 | 3 | 6 | 9 | 12 | 15 | 18 | 21 | 24 | 27 |
淀粉溶液滴数 | 3 | 3 | 3 | 3 | 3 | 3 | 3 | 3 | 3 | 3 |
步骤3:……
【数据处理】小组学生经过计算,得出100毫升食盐溶液中含有碘酸钾0.428毫克。
请回答下列问题:
(1)中碘元素的化合价为______;
(2)步骤1中,配置碘溶液时为了促进碘在水中的溶解,可以往水中加入适量的______;
(3)步骤2中,碘溶液用量的递减和蒸馏水用量的递增,其目的是______;
(4)1千克食盐所含的碘酸钾______(选填“符合”或“不符合”)标准。
参考答案:
1.C
【解析】
【详解】
由化学方程式可知,反应前出现了2个钠原子、2个氧原子、2个氢原子和2个氯原子,反应后出现了2个钠原子、2个氯原子和1个氧原子,根据质量守恒定律,尚缺的2个氢原子和1个氧原子存在于X中,则X的化学式为H2O,故选C。
2.A
【详解】
A、由反应前后原子种类和个数不变可知,X化学式为CO2,符合题意。
B、火药由多种物质组成,属于混合物,不符合题意。
C、该反应过程中会放出大量热,不符合题意。
D、反应后氮元素的化合价由+5变成0价,化合价降低,不符合题意。
故选A。
3.A
【解析】
【详解】
烧杯内壁出现水珠说明有水生成,将烧杯迅速倒转过来,倒入少量澄清石灰水,振荡,石灰水变浑浊证明有二氧化碳生成。根据质量守恒定律,反应前后元素种类不变,可知,打火机液体中一定含有碳、氢两种元素,可能含有氧元素。
故选A。
4.D
【解析】
【详解】
A. 由两种元素组成的物质,从后往前读,中间加化字,ClO2的化学名称为二氧化氯,此选项错误;
B. ClO2中氧元素的化合价为-2,根据化合物中各元素化合价的代数和为零,氯元素的化合价为+4价,此选项错误;
C. 两种或两种以上的物质发生化学反应生成另一种物质的反应是化合反应,制取ClO2的反应生成物有两种,不属于化合反应,此选项错误;
D. 根据化学反应前后各种原子个数相等,制取ClO2的反应中,x=2,此选项正确。
故选D。
5.C
【解析】
【详解】
由化学方程式:4P+5O22P2O5可知,反应中磷、氧气和五氧化二磷的质量之比为=(4×31):(5×32):(2×142)=62:82:142,故选C。
6.C
【详解】
A、磁性属于物理性质,Fe3O4与Fe2O3磁性不同,体现它们的物理性质不同,故选项说法正确。
B、在Fe2O3、Fe3O4中,将化学式变形得FeO1.5、FeO1.3,其它原子的相对质量之和越小的,在该化合物中铁元素的质量分数就越大,变形后FeO1.3中原子的相对质量之和小,则Fe3O4中铁的质量分数大于Fe2O3,故选项说法正确。
C、很多火柴头用氧化铁着色,点燃后会与木棒中的碳反应产生四氧化三铁和二氧化碳,反应的化学方程式为C+6Fe2O34Fe3O4+CO2,故选项说法错误。
D、火柴头原本是一种不被磁铁吸引的物体,火柴头不被磁铁吸引的是因为不易被磁化,故选项说法正确。
故选C。
7.B
【详解】
A、反应前后锂原子都是2个,钴原子都是2个,反应前氧原子是18个,反应后应该是18个,其中4个包含在未知物质中,反应前氢原子是8个,反应后应该是8个,包含在未知物质中,反应前后硫原子都是3个,生成物X的化学式为H2O,该选项说法不正确。
B、LiCoO2中锂元素化合价是+1,氧元素化合价是-2,根据化合物中元素化合价代数和为零可知,钴的化合价为+3价,该选项说法正确。
C、水不污染环境,该选项说法不正确。
D、该反应中,Co元素、O元素的化合价发生变化,该选项说法不正确。
故选B。
8.C
【解析】
【分析】
根据质量守恒定律可知该反应的化学方程式为:2HCl+NaClO═Cl2+NaCl+H2O。
【详解】
A、由多种物质反应生成一种物质的反应叫作分解反应,该反应是由两种物质反应生成三种物质,不属于分解反应,错误;
B、反应物和生成物中,属于氧化物只有H2O,错误;
C、根据质量守恒定律,反应前后原子的种类和数目不变,反应前氢原子的个数为2,氯原子的个数为3,钠原子的个数为1,氧原子的个数为1,反应后氢原子的个数为2,氯原子的个数为1,钠原子的个数为1,氧原子的个数为1,所以有毒气体是Cl2,正确;
D、有毒气体是Cl2,错误。
故选C。
9.C
【解析】
【详解】
设高锰酸钾完全反应生成的氧气的质量为x
=
x=16g
因为16g>2g,所以高锰酸钾未完全反应,那么剩余固体中有剩余的高锰酸钾,还有生成的锰酸钾和二氧化锰,故选C。
10.B
【解析】
【分析】
【详解】
A.根据质量守恒定律知道参加反应的X的质量为2.2克+6.4克-4.8克=3.8克,故选项错误。
B.设X的相对分子质量是a,
列比例式得:a:96=3.8g:4.8g,解得a=76,故选项正确。
C.由质量守恒定律知X中含有R、S元素,不含氧元素,故选项错误。
D.因不知R的元素种类,所以无法判断RO2是否是空气污染物,故选项错误。
故选B.
11. H2 +3价
【解析】
【详解】
(1)由化学方程式可知,反应前出现了2个铝原子、2个钠原子、4个氧原子和6个氢原子,反应后出现了2个钠原子、2个铝原子和4个氧原子,根据质量守恒定律可知,反应后尚缺的6个氢原子存在于3X中,即1个X分子中含有2个氢原子,则X的化学式为H2,故填H2。
(2)化合物中,钠元素的化合价为+1价,氧元素的化合价为-2价,设NaAlO2中Al的化合价为x,根据化合物中个元素的化合价的代数和为零,则+1+x+(-2)×2=0,x=+3,故填+3价。
12. +4 点燃法(合理即可)
【解析】
【详解】
(1)化合物中氯元素的化合价为-1价,设Ti元素的化合价为x,根据化合物中各元素的化合价的代数和为零,则x+(-1)×4=0,x=+4,故填+4。
(2)由化学方程式可知,反应前出现了2个镁原子、1个钛原子和4个氯原子,反应后出现了1个钛原子,由质量守恒定律可知,“?”处含有1个镁原子与2个氯原子,则此处的化学式为MgCl2,故填MgCl2。
(3)由化学方程式可知,①过程中产生的有毒气体一氧化碳,直接排放会污染空气,在排放前,可将气体采用点燃的方法转化为二氧化碳后在排放,故填点燃法。
13.LaNi5
【解析】
【分析】
【详解】
由所给反应方程式及反应前后原子种类和个数不变可知,M中含有一个La原子和五个Ni原子,化学式为LaNi5。
14. 2 2 3 2 1 1 2 2 1
【解析】
【详解】
(1)氯酸钾的化学式中有3个氧原子,而氧气的化学式中有2个氧原子,二者的最小公倍数为6,即在氯酸钾前面写2,氧气前面写3,先配平氧原子,最后在氯化钾前面写2配平钾原子和氯原子,即三种物质的化学计量数由左至右分别为2、2、3,故填2、2、3。
(2)高锰酸钾的化学式中有1个钾原子,而锰酸钾的化学式中有2个钾原子,二者的最小公倍数为2,即在高锰酸钾前面写2,锰酸钾前面写1,从而配平钾原子,观察发现,此时只要在二氧化锰前面写1,锰原子和氧原子就配平了,即三种物质的化学计量数由左至右分别为2、1、1,故填2、1、1。
(3)甲烷的化学式中有4个氢原子,水的化学式中有2个氢原子,二者的最小公倍数为4,即在水的化学式前写2,先配平氢原子。甲烷化学式中有一个碳原子,而二氧化碳化学式中也有一个碳原子,即在二氧化碳前面写1,配平碳原子,此时左边有两个氧原子,而右边有4个氧原子,即在氧气的化学式前面写2配平氧原子,即由左至右,三种物质的化学计量数为分别为2、2、1,故填2、2、1。
15. 导电性 Al2O3+2C2Al+CO↑+CO2↑
【解析】
【详解】
(1)石墨具有导电性,可用作电极,故填导电性。
(2)由图可知,氧化铝与石墨在通电的条件下反应生成铝、一氧化碳和二氧化碳,且生成的一氧化碳与二氧化碳的分子数为1:1,故反应的化学方程式写为:Al2O3+2C2Al+CO↑+CO2↑。
16. 12:5 9:22
【解析】
【详解】
(1)根据化学式可知,鼠李糖中氢、氧原子个数之比为:12:5。
(2)鼠李糖在氧气中充分燃烧化学方程式为
所以生成的水和二氧化碳质量比:216:528= 9:22。
17. 氧化物 +4 N2
【解析】
【详解】
(1)四氧化二氮中N元素的质量分数为:。
(2)四氧化二氮(N2O4)是由一种物质组成的,属于纯净物,该纯净物是由氮元素与氧元素组成的纯净物,属于化合物中的氧化物。四氧化二氮中氧元素化合价是-2,根据化合物中元素化合价代数和为零可知,氮元素的化合价为+4。
(3)根据质量守恒定律,化学反应前后元素种类以及原子个数不变,反应前后碳原子数是2个,氢原子数是8个,氧原子数是8个,反应前氮原子数是6个,反应后应该也是6个,包含在未知物质中,所以横线上的化学式为N2。
18. 2AgI═2Ag+I2 熔化
【解析】
【详解】
(1)碘化银在高空分解生成银单质和碘单质(),化学方程式为:2AgI═2Ag+I2;
(2)冰晶下降形成雨滴是固态的水熔化为液态的水。
19. +5 碘化钾 配制浓度不同,质量相同的碘溶液 符合
【解析】
【详解】
(1)碘酸钾中,钾元素的化合价是+1,氧元素的化合价是-2,设碘元素的化合价为x,根据化合物中元素化合价代数和为零,有:+1+x+(-2)×3=0,x=+5;
(2)步骤1中,配制碘溶液时为了促进碘在水中的溶解,可以往水中加入适量的碘化钾;
(3)步骤2中,碘溶液用量的递减和蒸馏水用量的递增,其目的是配制浓度不同,质量相同的碘溶液;
(4)1千克食盐所含的碘酸钾质量为:0.428mg×=42.8mg,42.8mg碘酸钾中碘元素的质量为:42.8mg××100%=25.4mg,该含量符合国家标准。
初中科学浙教版八年级下册第3章 空气与生命第3节 化学方程式获奖ppt课件: 这是一份初中科学浙教版八年级下册<a href="/kx/tb_c94226_t3/?tag_id=26" target="_blank">第3章 空气与生命第3节 化学方程式获奖ppt课件</a>,文件包含33化学方程式2pptx、33化学方程式2教学设计表格式doc、33化学方程式2学案含答案doc、化学方程式书写的依据是质量守恒wmv、化学方程意义mp4、标条件wmv等6份课件配套教学资源,其中PPT共32页, 欢迎下载使用。
初中浙教版第3节 化学方程式完美版ppt课件: 这是一份初中浙教版第3节 化学方程式完美版ppt课件,文件包含ZJ版八下33化学方程式2pptx、ZJ版八下33化学方程式2课后小练doc、化学方程式配平mp4等3份课件配套教学资源,其中PPT共25页, 欢迎下载使用。
初中科学浙教版八年级下册第3节 化学方程式优质ppt课件: 这是一份初中科学浙教版八年级下册第3节 化学方程式优质ppt课件,文件包含33化学方程式第1课时课件pptx、33化学方程式第1课时练习docx等2份课件配套教学资源,其中PPT共21页, 欢迎下载使用。













