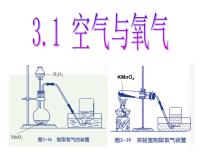





科学八年级下册第1节 空气与氧气精品ppt课件
展开3.1 空气与氧气 第4课时
一、选择题
1.化学实验操作的正确性、规范性是实验成功的关键,同时也反映了实验者的化学素养,下列实验操作示意图中,正确的是( )
A.取用固体药品
B.加热立即收集
C.收满后移出集气瓶
D.结束时停止加热
2.下列装置中(如图所示)不能用来收集氧气的是( )
A. B.
C. D.
3.如图是利用高锰酸钾制取氧气的实验装置,下列操作可能导致收集到的氧气不纯的是( )
A.加热前:集气瓶中装半瓶水 B.加热时:试管口要略向下倾斜
C.等冒出连续、均匀的气泡开始收集 D.实验结束时先移除导管再熄灭酒精灯
4.实验室常用如图甲、乙的发生装置制取氧气,小雪又设达了如图丙、丁的装置用于制取氧气,相关叙述合理的是( )
A.装置甲的试管口要略向下倾斜,是为防止高锰酸钾受热分解产生的水冷凝后倒流
B.使用装置乙分解双氧水制取氧气时,需定期向烧瓶中添加二氧化锰粉末
C.关闭止水夹a并向下压丙中注射器的活塞,放手后若活塞回到原处则装置气密性良好
D.利用装置丁进行实验室分解双氧水制取氧气,可实现“随开随用、随关随停”
5.实验室制取氧气的过程,大致分为以下六个主要操作:①点燃酒精灯,给试管加热;②熄灭酒精灯;③检查装置的气密性;④将氯酸钾和二氧化锰的混合物装入试管里,用带导管的胶塞塞紧,并将它固定在铁架台上;⑤用排水法收集氧气;⑥将导管从水面下取出。正确的操作顺序是( )
A.③④①⑤②⑥ B.③④①⑤⑥② C.④①③⑤②⑥ D.④①③⑤⑥②
6.如图是实验室制取、收集、验满、验证氧气性质的装置或操作,其中正确的是( )
A.制取氧气 B.收集氧气
C.验满 D.性质检验
7.实验室用加热高锰酸钾和排水法制取氧气的实验中,下列操作说法正确的是( )
A.应向试管中加入大量药品,以产生更多氧气 B.应先给试管均匀预热,后集中药品部位加热
C.导管冒出气泡时应立即收集,以免氧气浪费 D.结束时应先熄灭酒精灯,后将导管移出水面
8.木炭燃烧实验如图所示,则下列说法正确的是( )
A.②中木炭发出耀眼的白光
B.②中氧气为无色气体,密度比空气小
C.③中澄清石灰水会变浑浊
D.对比①②现象可证明,氧气具有可燃性
9.利用加热高锰酸钾的方法,验证化学反应中质量守恒定律。如图,小科将适量高锰酸钾装入试管,塞入一团棉花并测出试管、棉花与药品的总质量为。加热使之充分反应后,测得量筒中气体体积为V,再次测得反应装置与物质总质量为,已知常温常压下氧气密度为,根据实验数据计算发现:,与质量守恒定律不符。造成这一实验结果的原因分析不正确的是( )
A.导管口连续均匀冒气泡时才收集气体 B.试管中高锰酸钾没有完全分解
C.未调节量筒内外液面相平就读数 D.未注意到量筒中原本存在的少量空气
10.实验室制取气体选择收集方法时,下列性质:
①颜色;②密度;③溶解性;④可燃性;⑤能否与水反应。必须考虑的是( )
A.①②③ B.②③④ C.③④⑤ D.②③⑤
二、填空题
11.小吴同学发现自己居住的香格里拉小区正在进行燃气管道改造。就是把原来的普通燃气供应改造为更加清洁的天然气供应。小吴同学经过查询发现了以下信息:天然气的主要成分为甲烷(),实验室用加热无水醋酸钠和碱石灰固体混合物制取甲烷。标准状况下,甲烷密度比空气密度小,难溶于水。
(1)A装置图中,仪器①的名称是________。
(2)实验室制取甲烷所需的发生装置是________,收集甲烷所需的装置是________(选填装置图编号)。
12.下图是实验室制取气体的常用装置,请回答下列问题:
(1)仪器a的名称是___________。
(2)选用双氧水和二氧化锰制取氧气时,应选用___________(选填*A"或“B")作为气体发生装置。
(3)选用D装置作为氧气收集装置,氧气从___________(选填“a"或“b")管进入。
13.下列是实验室制取气体常见的发生装置和收集装置。
(1)写出仪器名称:①___________ ; ②___________。
(2)实验室用过氧化氢和二氧化锰制取氧气,若要控制产生氧气的速率,应选用的发生装置是_______。
(3)用加热高锰酸钾制取氧气并用排水法收集的实验中,操作步骤先后顺序不正确的有哪些________。
A.先检查装置气密性,再加入药品
B.先对试管预热,再集中加热
C.先点燃酒精灯加热,再将集气瓶装满水倒置在水槽中
D.先熄灭酒精灯,再将导管撤离水槽
(4)若用右图所示的装置排空气法收集氢气,需要将氢气从装置的_______导管口通入。(选填“a”或“b”)
14.请你根据下列实验装置图回答:
(1)实验室用高锰酸钾制取O2应选用的发生装置是___________。(用编号表示)
(2)实验室若用块状固体和液体且无需加热来制取气体,改用F装置(多孔隔板用来放块状固体)代替B装置的优点是___________。
三、探究题
15.为了研究能使带火星的木条复燃的氧气含量最小值,某兴趣小组用如图装置,以及实验室提供的实验所需器材和药品进行实验。(器材和药品:量筒、氯酸钾、二氧化锰若干克)。
(1)若空气中氧气的含量以20%来计算,现在要制取一瓶氧气体积分数为60%气体,请你写书实验步骤______。
(2)以下该小组两位同学所做的实验记录:
小明同学是一次性先收集7瓶不同氧气体积分数的气体,然后逐一检验是否能使带火星的木条复燃。实验结果记录,如表甲。
| 第1瓶 | 第2瓶 | 第3瓶 | 第4瓶 | 第5瓶 | 第6瓶 | 第7瓶 |
氧气含量 | 30% | 40% | 50% | 60% | 70% | 80% | 90% |
带火星的木条 | 不复燃 | 复燃 | 复燃 | 复燃 | 复燃 | 复燃 | 复燃 |
表甲
小王同学是先收集一瓶气体,检验他能否使带火星的木条,分析后在依次收集下一瓶气体再进行实验。实验结果记录如表乙:
| 第1瓶 | 第2瓶 | 第3瓶 | 第4瓶 | 第5瓶 |
氧气含量 | 60% | 40% | 30% | 35% | 32.5% |
带火星的木条 | 复燃 | 复燃 | 不复燃 | 复燃 | 不复燃 |
表乙
根据实验结果,你认为哪位同学的方法更好? 并说出你的依据。______。
16.小明发现二氧化锰催化过氧化氢分解的实验中,反应速度逐渐变慢,查阅资料得知:其原因是过氧化氢的溶质质量分数减小以及二氧化锰的催化能力降低,为了探究二氧化锰催化能力降低的影响因素,进行如下实验
【材料准备】取三份质量均为2克的二氧化锰分别催化40毫升溶质质量分数为10%、20%、30%的过氧化氢溶液分解,实验后回收二氧化锰,并分别标为A,B,C;另取多次催化分解10%过氧化氢实验后回收的二氧化锰,标为D
【实验步骤】
②连接实验装置并检查气密性;
②取未使用过的二氧化锰0.5克,加入锥形瓶中,再加入10毫升溶质质量分数为5%的过氧化氢溶液,记录收集120毫升气体所需的时间;
③再分别取A,B、C,D组二氧化锰各0.5克,重复上述实验;
④多次实验取平均值,记录数据如下:
组别 | 未使用过的二氧化锰 | A | B | C | D |
收集气体时间/秒 | 17.9 | 23.2 | 27.7 | 32.3 | 37.8 |
(1)实验时,长颈漏斗下端管口应在液面以下,其目的是______;
(2)实验中,通过比较收集相同体积气体所需的时间外,还可以通过比较______来反映二氧化锰的催化能力;
(3)由表中数据可知,引起回收的二氧化锰催化能力下降的因素是______
17.如图是实验室制取常见气体的装置图,据图回答问题:
(1)以过氧化氢溶液为原料制取并收集氧气,应选用的装置是___________(填装置标号,下同),反应的化学方程式为___________;
(2)实验室常用加热无水醋酸钠与碱石灰固体混合物来制取甲烷气体。要制取并收集甲烷(密度比空气小,难溶于水),可选用的发生和收集装置依次是___________;
(3)小明在学习了“用过氧化氢制取氧气”的知识后,进行如下实验:
a、按图组装实验仪器并进行气密性检查。
b、取10毫升溶质质量分数为3%的过氧化氢溶液和0.03克二氧化锰装入容器,塞紧橡皮塞,按上压强测量仪(如图)
c、倾斜装置,使过氧化氢溶液和二氧化猛充分混合,用压强测量仪测量容器内的气压。
d、分别用0.06克、0.09克和0.12克相同的二氧化锰重复上述实验,整理相关数据如图
①实验中,小明用___________来反映产生氧气的多少;
②本实验除了研究“二氧化锰质量对过氧化氢分解产生氧气质量的影响”外,在此基础上还可以研究的问题是___________。
③实验结束后,小明回收了二氧化锰。如果要证明二氧化锰是过氧化氢分解的催化剂,还需验证二氧化锰的___________保持不变。
参考答案:
1.A
【解析】
【分析】
【详解】
A、取用粉末状固体药品时,先将试管横放,然后用药匙或纸槽将药品送入试管底部,然后慢慢竖起,选项正确;
B、排水法收集气体时,应等气泡连续均匀冒出时再开始收集,选项错误;
C.收集满氧气后,在水面下用玻璃片把瓶口盖住再拿出水面,选项错误;
D.为防止水倒流,引起试管的炸裂,实验结束后要先把导管从水槽中移出,再熄灭酒精灯,选项错误。
故选A。
2.D
【解析】
【分析】
根据氧气密度比空气大,难溶于水的性质,可以选择向上排空气法和排水法来收集。
【详解】
A、该装置是一个多功能装置,若从长导管进气,则属于向上排空气法,可以收集氧气;若从短导管进气,则属于向下排空气法,可以收集氢气、甲烷等,故A项正确。
B、该装置是排水法收集气体,可以收集氧气,故B项正确。
C、该装置是向上排空气法收集气体,可以收集氧气,故C项正确。
D、该装置是向下排空气法收集气体,不可以用来收集氧气,故D项错误。
故选D。
3.A
【解析】
【分析】
【详解】
A、加热前,集气瓶中装半瓶水,即集气瓶中含有空气,再利用排水法收集的氧气中含有空气,得到不纯的氧气,选项正确;
B、加热时,试管口要略向下倾斜,可以防止水分倒流造成试管炸裂,不会导致收集的氧气不纯,选项错误;
C、等冒出连续、均匀的气泡开始收集,此时收集的气体是纯净的氧气,选项错误;
D、实验结束时先移除导管再熄灭酒精灯,可以防止水分倒吸造成试管炸裂,不会导致收集的氧气不纯,选项错误,故选A。
4.C
【解析】
【分析】
【详解】
A、装置甲的试管口要略向下倾斜,是为防止试管口处的冷凝水倒流,导致试管发生炸裂,高锰酸钾受热分解后不生成水,选项错误;
B、二氧化锰是分解双氧水制取氧气的催化剂,反应前后,其质量和化学性质保持不变,所以使用装置乙分解双氧水制取氧气时,不需定期向烧瓶中添加二氧化锰粉末,选项错误;
C、关闭止水夹a并向下压丙中注射器的活塞,放手后若活塞回到原处则装置气密性良好,选项正确;
D、装置丁中,双氧水与二氧化锰不能实现分离,不可能实现“随开随用、随关随停”,选项错误;
故选C。
5.B
【解析】
【分析】
【详解】
加热氯酸钾和二氧化锰的混合物制取氧气的实验步骤是检查装置的气密性,将氯酸钾和二氧化锰的混合物装入试管里,用带导管的胶塞塞紧,并将它固定在铁架台上,点燃酒精灯,给试管加热,用排水法收集氧气,将导管从水面下取出,熄灭酒精灯,即正确的实验步骤是③④①⑤⑥②,故选B。
6.B
【解析】
【分析】
【详解】
A.制取氧气时,为了防止药品中的水分冷凝后流到试管底部引起炸裂,所以试管口应该略向下倾斜,故A错误。
B.收集氧气时,因为氧气的密度大于空气,所以通入氧气的导管口应该伸到集气瓶底部,故B正确。
C.验满时,应该将带火星的小木条伸到集气瓶口处,不应该深入瓶内,故C错误。
D.性质检验时,将铁丝放入氧气燃烧,为了防止高温熔融物滴落瓶底引起炸裂,所以瓶底应该放入沙子或水,故D错误。
故选B。
7.B
【解析】
【分析】
【详解】
A.应向试管中加入适量药品,将试管底部铺满即可,故A错误。
B.应先给试管均匀预热,后集中药品部位加热,防止试管炸裂,故B正确。
C.导管冒出气泡时不应该立即收集,这时气体中存在空气,故C错误。
D.结束时应先将导管移出水面,再熄灭酒精灯,防止水被倒吸进试管造成炸裂,故D错误。
故选B。
8.C
【解析】
【详解】
A. ②中木炭在氧气中燃烧发出白光,此选项错误;
B. ②中氧气为无色气体,密度比空气大,此选项错误;
C. 木炭燃烧生成二氧化碳,二氧化碳能使澄清石灰水变浑浊,所以③中澄清石灰水会变浑浊,此选项正确;
D. 对比①②现象可证明,氧气浓度越大,木炭燃烧越剧烈,此选项错误。
故选C。
9.B
【解析】
【分析】
【详解】
A、导管口连续均匀冒气泡时才收集气体导致部分氧气没有收集起来,会造成m1-m2≠ρV,故A正确。
B、试管中高锰酸钾没有完全分解不会造成m1-m2≠ρV,故B错误。
C、未调节量筒内外液面相平就读数会造成氧气的体积读数不准确,造成m1-m2≠ρV,故C正确。
D、未注意到量筒中原本存在的少量空气,会造成氧气体积偏大,造成m1-m2≠ρV,故D正确。
故选B。
10.D
【解析】
【分析】
【详解】
实验室制取气体收集方法的选择是根据:一般考虑气体物理性质中的密度和溶解性,化学性质中看它是否与水发生化学反应;难溶于水或不易溶于水且不与水反应的气体可用排水法收集;密度比空气大的气体(不能与空气中的成分反应)可用向上排空气法收集,密度比空气小的气体(不能与空气中的成分反应)可用向下排空气法收集。故必须要考虑的是②③⑤,故选D。
11. 试管 A C##E
【解析】
【详解】
(1)A装置图中,仪器①的名称是试管。
(2)实验室用加热无水醋酸钠和碱石灰固体混合物制取甲烷,所以实验室制取甲烷所需的发生装置是A,收集甲烷所需的装置是C(甲烷难溶于水)或E(甲烷密度比空气小)。
12. 长颈漏斗 A a
【解析】
【分析】
【详解】
(1)仪器a的名称是长颈漏斗。
(2)实验室用过氧化氢和二氧化锰混合物制取氧气,该反应是固液不加热型,发生装置选A。
(3)氧气的密度比空气略大,用装置D收集氧气,气体应从导管口a端通入。
13. 长颈漏斗 集气瓶 C CD b
【解析】
【详解】
(1)①为长颈漏斗;②为集气瓶。
(2)如果用双氧水和二氧化锰制氧气就不需要加热,分液漏斗可以控制反应的速率,故选择C装置。
(3)实验室用高锰酸钾制取氧气并用排水法收集的操作,叙述正确的是:先检查装置的气密性,再加入药品进行制取;先均匀预热,再对着药品部位集中加热;先等着导管口排出的气泡连续均匀后,再将导管伸入盛水的集气瓶中进行收集;先熄灭酒精灯,再将导管从水槽中取出,故不正确的选CD。
(4)由于氢气的密度比空气的小,用如图所示的装置收集氢气,氢气应从b端进入。
14. A 可控制反应的发生或停止
【解析】
【分析】
高锰酸钾加热生成锰酸钾、二氧化锰和氧气。
【详解】
(1)高锰酸钾加热生成锰酸钾、二氧化锰和氧气,用高锰酸钾制氧气就需要加热,为固体加热型制取气体,故选A。
(2)多孔隔板使固体物质在隔板上,当反应进行时隔板上的固体与液体接触,反应进行;当把止水夹关闭时,产生的气体是压强增大,把液体压入长颈漏斗,隔板上的固体与液体分离,反应停止,故用F装置(多孔隔板用来放块状固体)代替B的装置优点是可以控制反应的发生和停止。
【点睛】
多孔隔板可以控制反应的发生和停止。
15. 先向集气瓶中倒入一半体积的水,再用排水法收集满氧气即可 小王;更能准确的知道木条复燃时,氧气的浓度
【解析】
【详解】
(1)设集气瓶的体积为x,加入水的体积为y,则:y+(x-y)×20%=x×60%,解得:x:y=2:1;故操作步骤为:先向集气瓶中倒入一半体积的水,再用排水法收集满氧气即可;
(2)分析两组数据可知,小王同学的方法更好;对比两组数据可知,小王同学的方法更能准确的知道木条复燃时,氧气的浓度。
16. 防止生成的气体沿长颈漏斗逸散到空气中 相同的时间内收集的气体的体积 二氧化锰的使用次数和过氧化氢溶液的质量分数
【解析】
【分析】
【详解】
(1)实验时,长颈漏斗下端管口应在液面以下,可用防止生成的气体沿长颈漏斗逸散到空气中,导致无法收集气体,故填防止生成的气体沿长颈漏斗逸散到空气中。
(2)反映二氧化锰的催化能力,除通过比较收集相同体积气体所需的时间外,还可以比较相同的时间内收集的气体的体积来判断反应速率大小,进而比较二氧化锰的催化能力,故填相同的时间内收集的气体的体积。
(3)由图可知,过氧化氢溶液的质量分数相同时,二氧化锰的使用次数越少,生成等量的氧气所需要的时间越短,过氧化氢溶液的质量分数越大,生成等量的氧气所需要的时间越短,所以引起回收的二氧化锰催化能力下降的因素是二氧化锰的使用次数和过氧化氢溶液的质量分数,故填二氧化锰的使用次数和过氧化氢溶液的质量分数。
17. AC或AE 2H2O2 2H2O+O2↑ BD或BE 用容器内压强的大小 二氧化锰的质量对反应速率的影响 质量和化学性质
【解析】
【分析】
【详解】
(1)以过氧化氢溶液为原料制取并收集氧气,不需要加热,适合用装置A作发生装置;氧气的密度比空气大,不易溶于水,可用排水法和向上排空气法收集,应选用的装置组合为:AC或AE;过氧化氢在二氧化锰的催化作用下生成水和氧气,化学方程式为:2H2O2 2H2O+O2↑;
(2)实验室常用加热无水醋酸钠与碱石灰固体混合物来制取甲烷气体,反应条件是加热,反应物是固体,适合用装置B作发生装置;甲烷密度比空气小,难溶于水,可用向下排空气法和排水法收集,所以可选用的发生和收集装置依次是BD或BE;
(3)①实验中,容器内气体的压强越大,说明产生的氧气越多,压强越小,说明产生的氧气越少,因此小明是用容器内压强的大小来反映产生氧气的多少;
②由图中数据可知,二氧化锰的质量大小能够影响反应的速率,但是不影响产生氧气的质量,因此本实验除了研究“二氧化锰质量对过氧化氢分解产生氧气质量的影响外”还可以研究的问题是二氧化锰的质量对反应速率的影响;
③由于催化剂只是改变其他物质的反应速率,在反应前后本身的质量和化学性质都没有发生改变。所以要验证二氧化锰是过氧化氢分解的催化剂,还需验证二氧化锰的质量和化学性质在反应前后保持不变。
科学八年级下册第1节 空气与氧气一等奖课件ppt: 这是一份科学八年级下册<a href="/kx/tb_c94224_t3/?tag_id=26" target="_blank">第1节 空气与氧气一等奖课件ppt</a>,文件包含31氧气制取实验4pptx、31空气与氧气4教学设计表格式doc、31空气与氧气4学案含答案doc、检查装置气密性mp4、铝粉在空气中燃烧mp4、高锰酸钾制氧气mp4等6份课件配套教学资源,其中PPT共26页, 欢迎下载使用。
科学八年级下册第1节 空气与氧气精品ppt课件: 这是一份科学八年级下册第1节 空气与氧气精品ppt课件,文件包含31空气与氧气第3课时课件pptx、31空气与氧气第3课时练习docx等2份课件配套教学资源,其中PPT共21页, 欢迎下载使用。
初中科学浙教版八年级下册第1节 空气与氧气完整版课件ppt: 这是一份初中科学浙教版八年级下册第1节 空气与氧气完整版课件ppt,文件包含31空气与氧气第2课时课件pptx、31空气与氧气第2课时练习docx等2份课件配套教学资源,其中PPT共21页, 欢迎下载使用。