












化学九年级下册课题 2 金属的化学性质备课课件ppt
展开课题2 金属的化学性质
第1课时 金属与氧气和酸的反应
【学习目标】
1.知识与技能:知道铁、铝、铜等常见金属与氧气的反应,能用金属活动性顺序对有关的置换反应进行简单地判断。
2.过程与方法:初步学会运用观察、实验等方法获取信息,并能用图表和化学语言表达有关的信息。
3.情感态度与价值观:通过对五彩纷呈的化学现象的观察,激发学生的好奇心和求知欲,发展学生学习化学的兴趣。
【学习重点】
常见金属的化学性质。
【学习难点】
认识金属与盐酸、稀硫酸及与某些化合物溶液的置换反应。
一、情景导入 生成问题
1.导语:大家熟悉的金属铁、铜、铝,你知道它们的哪些化学性质?你能否用化学方程式表示出来?如何从化学的角度,解释“真金不怕火炼”?
2.出示学习目标,由学生对学习目标进行解读。
二、自学互研 生成能力
阅读教科书P9,写出镁、铝、铁、铜等金属与氧气反应的化学方程式。比较上述各反应的条件及现象,按金属活动性由强到弱的顺序将其排列。
提示:镁、铝、铁、铜等金属与氧气反应的化学方程式:2Mg+O2===2MgO;4Al+3O2===2Al2O3;3Fe+2O2Fe3O4;2Cu+O22CuO;点拨:根据金属与氧气反应的难易程度及反应的剧烈程度,可以判断出金属活动性的强弱顺序,即:镁>铝>铁>铜。
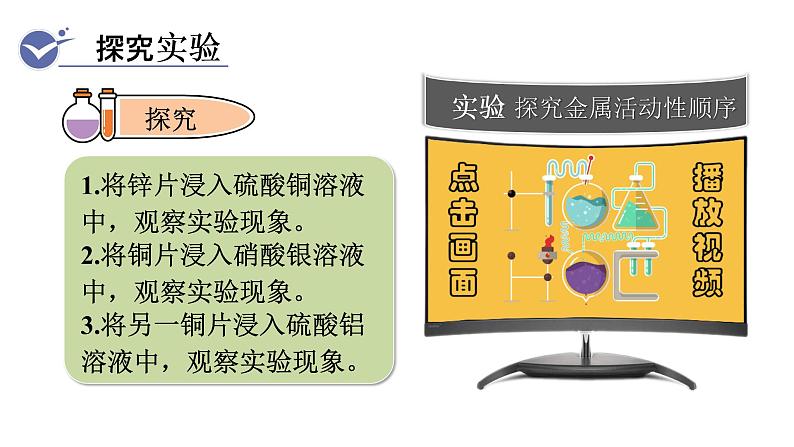
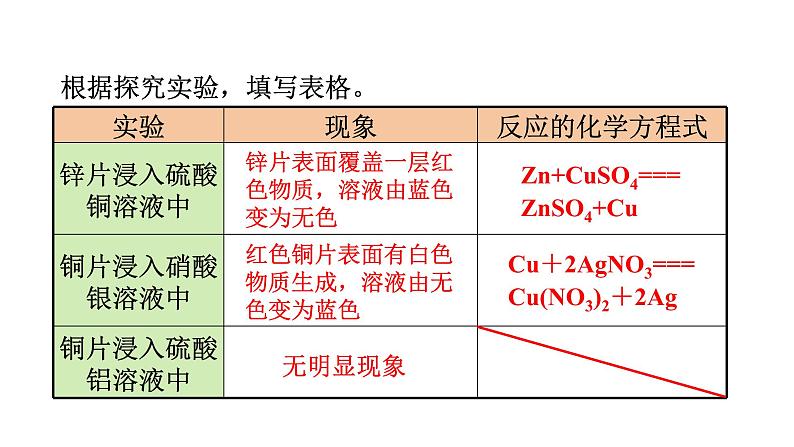
1.实验探究:学生分组阅读并完成教科书P10中的“探究”。
金属 | 现象 | 反应的化学方程式 | ||
稀盐酸 | 稀硫酸 | 稀盐酸 | 稀硫酸 | |
镁 | 反应很剧烈, 产生大量气泡 | 反应很剧烈, 产生大量气泡 | Mg+2HCl===MgCl2+H2↑ | Mg+H2SO4===MgSO4+H2↑ |
锌 | 反应剧烈, 产生大量气泡 | 反应剧烈, 产生大量气泡 | Zn+2HCl===ZnCl2+H2↑ | Zn+H2SO4===ZnSO4+H2↑ |
铁 | 反应较剧烈, 产生大量气泡 | 反应较剧烈, 产生大量气泡 | Fe+2HCl===FeCl2+H2↑ | Fe+H2SO4===FeSO4+H2↑ |
铜 | 无明显现象 | 无明显现象 | \ | \ |
2.思考与讨论:
(1)上述实验过程中,为什么金属颗粒的大小要基本相同、酸的用量及酸的溶质质量分数要相等?
点拨:根据金属与酸是否能发生反应及反应的剧烈程度,来判断金属的活动性强弱,在比较的过程中要注意控制好变量(即反应条件),要保证在相同的反应条件下进行,实验结果才有意义。
方法指导:创景设疑,帮助学生明确本节课的学习目标。 提示:教会学生看书,独学时对于书中的问题一定要认真探究,书写答案。
点拨:铝在常温下就可以跟空气中的氧气发生反应,使其表面生成一层致密的氧化铝薄膜,从而使铝具有较强的抗腐蚀性能,其化学性质较活泼而非不活泼。
点拨:这是对比实验,要注意控制好变量,即反应条件:金属颗粒大小、酸的用量及溶质质量分数,要保证在相同条件下进行比较,才能得出有价值的结果。
提示:(1)铁与稀盐酸、稀硫酸反应生成的是亚铁化合物(含亚铁离子,溶液呈浅绿色);(2)置换反应中元素的化合价发生改变。 |
(2)上述四种金属中能跟酸反应的有几种?反应剧烈程度如何?不跟酸反应的有几种?由此排列出四种金属的活动性强弱顺序。
点拨:详见1中表格;金属活动性的强弱顺序:镁>锌>铁>铜。
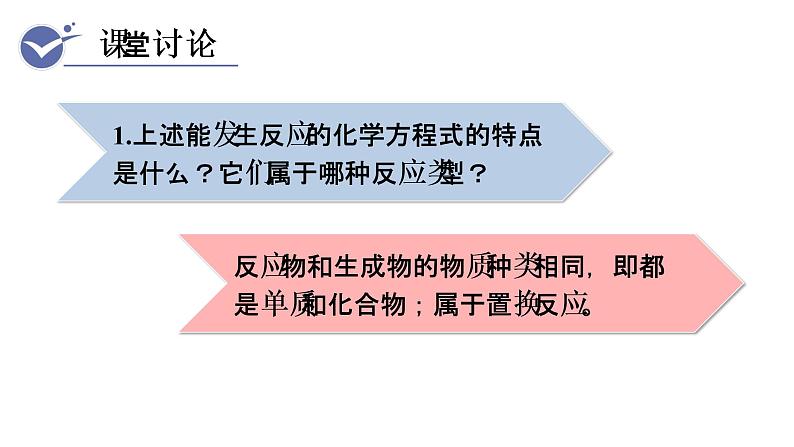
3.(1)比较能与酸反应的化学方程式,找出反应物、生成物的共同特点,总结什么叫置换反应。
点拨:置换反应是由一种单质与一种化合物反应,生成另一种单质和另一种化合物的反应。
(2)试写出一个前面曾经学习过的置换反应的化学方程式。
点拨:C+2CuO2Cu+CO2↑
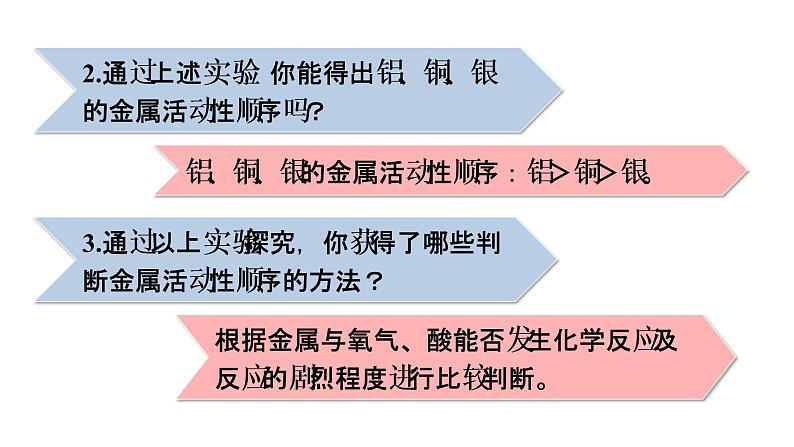
4.通过上述探究活动,你获得了什么结论?
点拨:通过上述探究活动可以得出,镁、锌、铁的金属活动性比铜的强,它们都能置换出盐酸或稀硫酸中的氢。
三、交流展示 生成新知
知识模块一:金属与氧气的反应
知识模块二:金属与盐酸、稀硫酸的反应
第1课时 金属与氧气和酸的反应
一、金属的化学性质
1.大多数金属可与氧气反应;
不同的金属与氧气反应的难易程度不同。
2.金属+酸→盐+氢气↑;
金属活动性:Mg>Al>Zn>Fe>Cu。
二、置换反应
AB+C===A+CB
本课以多层次科学探究为主线,渗透了建构主义的教学思想,以“猜金属”“玩卡片”创设情景,互动评价激励探究热情,以“学生发展”为本,进行有意义的知识建构,符合学生的心理特点,学生学习兴趣盎然,主动参与,体验深刻。主要的缺陷是时间较为紧张,课堂上学生极为兴奋,控制探究的进程较难。课堂各种活动亦应做好更充分的准备,多媒体应用尽可能贴切,实验探究安排尽可能合理(如在金属与盐酸、稀硫酸反应的教学版块,将学生分为两组分别进行以节省课堂时间),教学效果可能会更好。
点拨:根据金属与氧气、酸反应的难易程度及反应的剧烈程度可以判断金属活动性的强弱顺序,即:镁>铝>铁>铜。
强调:金属能置换出盐酸或稀硫酸中的“氢”,而非“氢气”。
及时总结所学知识,养成梳理知识的良好习惯,受益终身。 |
初中化学人教版九年级下册课题 2 金属的化学性质试讲课课件ppt: 这是一份初中化学人教版九年级下册<a href="/hx/tb_c9862_t3/?tag_id=26" target="_blank">课题 2 金属的化学性质试讲课课件ppt</a>,共27页。PPT课件主要包含了金属与氧气反应,你知道吗,金属与酸反应,你有什么发现,置换反应,活动性Fe﹥Cu,金属与盐溶液反应等内容,欢迎下载使用。
人教版九年级下册课题 2 金属的化学性质说课课件ppt: 这是一份人教版九年级下册课题 2 金属的化学性质说课课件ppt,共37页。PPT课件主要包含了真金不怕火炼,火眼金睛,金属与氧气反应,综合上述可得,你知道吗,金属与酸反应,你有什么发现,置换反应,活动性Fe﹥Cu,金属与盐溶液反应等内容,欢迎下载使用。
初中化学人教版九年级下册课题 2 金属的化学性质课文ppt课件: 这是一份初中化学人教版九年级下册课题 2 金属的化学性质课文ppt课件,共15页。PPT课件主要包含了学习目标,探究活动,活动探究,反应化学方程式,上述反应有什么特点,友情提示等内容,欢迎下载使用。














