





2020-2021学年第二单元 硫及其化合物的相互转化课文内容ppt课件
展开在古代中国,稀硫酸被称为“绿矾油”。《黄帝九鼎神丹经诀》卷九中就记载着“炼石胆取精华法”,即干馏石胆(胆矾)而获得硫酸。绿矾油是一种无色黏稠液体,可用于除掉兵器上的铁锈。实验室模拟此过程:可以用FeSO4·7H2O加强热,用加冰水混合物的U形管冷凝即可,用NaOH吸收SO2,理论可得29.5%的H2SO4。上述过程硫的化合价如何变化?你能预测生成的含铁化合物是什么吗?试写出反应的化学方程式。
1.了解含硫物质在自然界中的存在与转化,熟悉自然界中常见的含硫物质的类别及硫元素的化合价。2.根据硫元素化合价分析含硫物质的性质,并能设计实验实现不同价态硫元素的相互转化。
1.能从物质的类别、元素的价态的角度,预测分析硫及其化合物的性质及转化规律。(宏观辨识与微观探析)2.能运用氧化还原反应和酸碱反应规律,设计不同价态硫元素转化的反应原理,并结合实验药品设计实验进行探究。(科学探究与创新意识)
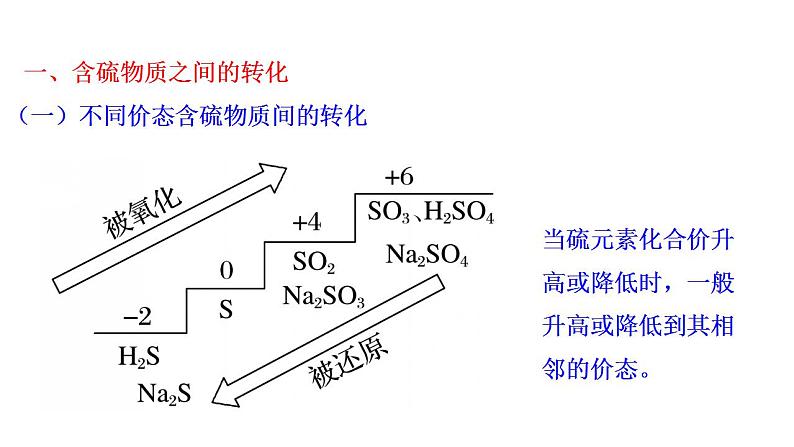
一、含硫物质之间的转化
(一)不同价态含硫物质间的转化
当硫元素化合价升高或降低时,一般升高或降低到其相邻的价态。
自然界中不同价态硫元素之间的转化大气中SO2主要有三个来源:化石燃料的燃烧、火山爆发和微生物的分解作用。在自然状态下,大气中的SO2,一部分被绿色植物吸收;一部分则与大气中的水结合,经过一系列反应形成H2SO4,随降水落入土壤或水体中,以硫酸盐的形式被植物的根系吸收,转变成蛋白质等有机物,进而被各级消费者所利用,动植物的遗体被微生物分解后,又能将硫元素释放到土壤或大气中,这样就形成一个完整的循环。
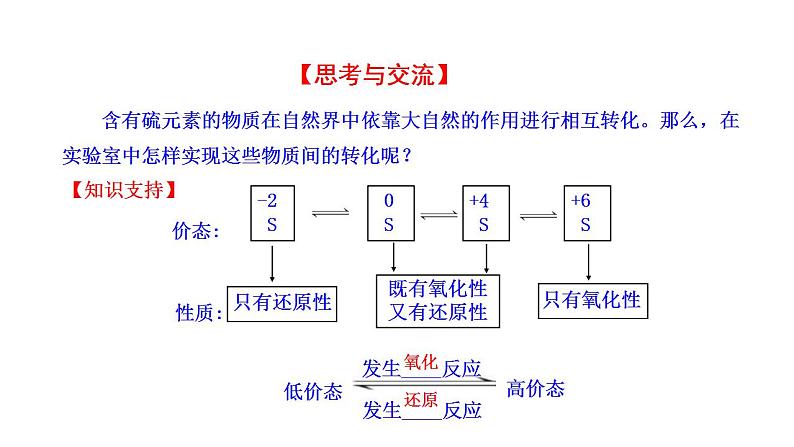
含有硫元素的物质在自然界中依靠大自然的作用进行相互转化。那么,在实验室中怎样实现这些物质间的转化呢?
1、硫单质与金属反应:(1)与钠反应:____________________ ; (2)与铜在加热条件下反应:_______________;(3)与铁在加热条件下反应: ______________ 。
2Na + S == Na2S
(1)与氢气反应:_________________________。
化合价变化:0价→ -2价,发生还原反应,表现弱氧化性。
化合价变化:0价→ +4价,发生氧化反应,表现还原性。
(2)与氧气反应:__________________________。
2、硫单质与非金属反应:
3、在常温下,硫单质能与汞化合生成硫化汞(HgS)。因此,为了除去不慎洒落的汞,人们常将硫黄粉撒在汞的表面。4、长期暴露在空气中的亚硫酸钠会慢慢变成硫酸钠5、实验室中用过量氢氧化钠溶液吸收二氧化硫生成亚硫酸钠。6、二氧化硫在催化剂、加热的条件下与氧气反应生成三氧化硫
Hg + S == HgS
2Na2SO3 + O2 == 2Na2SO4
SO2 + 2NaOH== Na2SO3 + H2O
2SO2 + O2 2SO3
不同价态硫元素间转化的思维模型
溴水、HNO3、Fe3+ 、H2O2KMnO4(H+)、
Cu、C、HI、H2S
Cl2、O2、 KMnO4(H+)
不同价态硫元素间的相互转化
(二)同种价态含硫物质间的转化
图中物质之间的转化可以通过不同的化学反应来实现。可以是元素化合价发生改变的氧化还原反应(图中横向箭头表示的转化),也可以是元素化合价不变的非氧化还原反应(图中纵向箭头表示的转化)
写出上表中①-④表示的物质间转化的化学方程式①________________________________②________________________________③________________________________④________________________________
SO2 + H2O ⇌H2SO3
2H2SO3 + O2 == H2SO4
SO3 + H2O == H2SO4
SO3 + 2NaOH == Na2SO4 + H2O
【整理归纳】硫及其化合物的转化
[思考]请同学们完成上述涉及到的方程式:
相同价态含硫化合物间--非氧化还原反应转化不同价态含硫化合物间--氧化还原反应转化
① 2H2S+SO2=3S↓+ H2O ②S +O2 = SO2③ 2SO2+O2 2SO3 ④ SO3 + H2O = H2SO4⑤ 2NaOH+SO2=Na2SO3+H2O ⑥ H2O+SO2 ⇌H2SO3 ⑦2Na2SO3+O2=2Na2SO4⑧2NaOH+H2SO4 = Na2SO4+H2O ⑨BaCl2+H2SO4 = BaSO4↓+2HCl
H2S H2SO3 H2SO4 BaSO4 FeS S SO2 SO3 CuSO4
Cl2、H2O2、O2
KMnO4、HNO3、Fe3+
Cl2、O2、SO2、Fe3+、 HNO3 、 KMnO4
1.下列关于硫的叙述中不正确的是( )A.在自然界中既有化合态的硫又有游离态的硫B.游离态的硫存在于火山喷口附近或地壳的岩层里C.实验室常用酒精除去附着在试管壁上的硫黄D.硫是黑火药的主要成分之一
解析:硫在自然界中既能以化合态(主要为硫化物和硫酸盐)又能以游离态(火山喷口附近或地壳岩层)的形式存在。硫单质俗称硫黄,是一种黄色或淡黄色固体,难溶于水,微溶于酒精,易溶于二硫化碳,常用二硫化碳除去试管内壁附着的硫单质。
2.下列转化需要加入氧化剂才能实现的是( )A.H2S→SO2 B.H2SO4→SO2C.SO42- →BaSO4 D.SO32- →SO2
3.硫在自然界中的循环过程如下图所示,下列说法不正确的是( )
A.石油和煤等化石燃料中含有硫元素B.大气中的二氧化硫只来源于火山喷 发产生的气体C.地壳中的硫元素常以硫化物和硫酸 盐的形式存在D.动植物遗体被微生物分解后,可产 生SO42-和SO2
4.A、B、C、D、E五种物质中含有同一种元素,A是淡黄色固体,其相互转化关系如图所示,回答下列问题:
(1)写出B、E的化学式:B____、E_______。
(2)写出C→D的化学方程式:____________________。
(3)将足量的物质C通入BaCl2溶液中,下列说法正确的是______(填序号)。①溶液没有明显变化②溶液中出现白色沉淀③若通入Cl2,则溶液中出现白色沉淀
2SO2+O2 2SO3
高中化学苏教版 (2019)必修 第一册专题4 硫与环境保护第一单元 含硫化合物的性质教学课件ppt: 这是一份高中化学苏教版 (2019)必修 第一册专题4 硫与环境保护第一单元 含硫化合物的性质教学课件ppt,共14页。PPT课件主要包含了温故知新,游离态和化合态,NaHSO3,回顾思考,硫单质的性质,物理性质,化学性质,与金属反应,跟非金属反应,跟碱溶液反应等内容,欢迎下载使用。
高中化学苏教版 (2019)必修 第一册专题4 硫与环境保护第二单元 硫及其化合物的相互转化精品课件ppt: 这是一份高中化学苏教版 (2019)必修 第一册专题4 硫与环境保护第二单元 硫及其化合物的相互转化精品课件ppt,共22页。PPT课件主要包含了学习目标,课程导入,学习探究,归纳总结,学习小结,当堂检测等内容,欢迎下载使用。
高中化学苏教版 (2019)必修 第一册第二单元 硫及其化合物的相互转化多媒体教学ppt课件: 这是一份高中化学苏教版 (2019)必修 第一册第二单元 硫及其化合物的相互转化多媒体教学ppt课件,共38页。













