





人教版九年级下册课题2 化学肥料优秀ppt课件
展开1、掌握几种常见离子的检验方法(重点)2、学会氮肥的简易鉴别.3、掌握物质分离、提纯的方法.(难点)
如何鉴别 NH3.H2O、NH4HCO3、(NH4)2SO4、 NH4Cl、 NH4NO3、 CO(NH2)2 (尿素) 六种氮肥?
首先来学习 CO32-、SO42-、Cl-、NH4+ 四种常见离子的检验
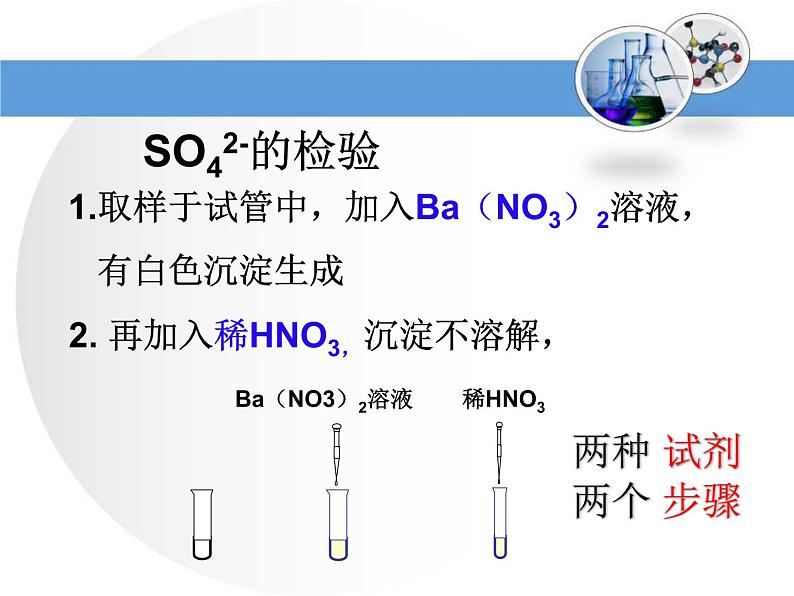
1.取样于试管中,加入Ba(NO3)2溶液, 有白色沉淀生成
2. 再加入稀HNO3,沉淀不溶解,
两种 试剂 两个 步骤
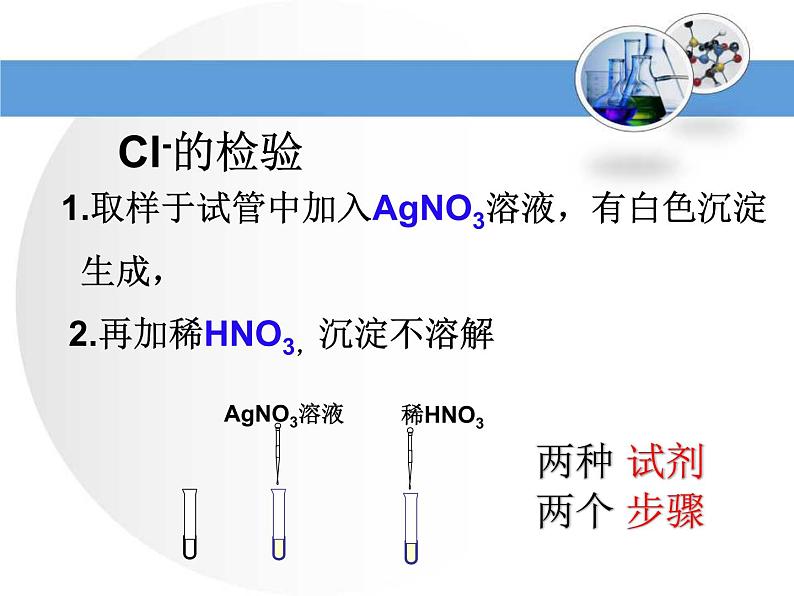
1.取样于试管中加入AgNO3溶液,有白色沉淀 生成,
2.再加稀HNO3,沉淀不溶解
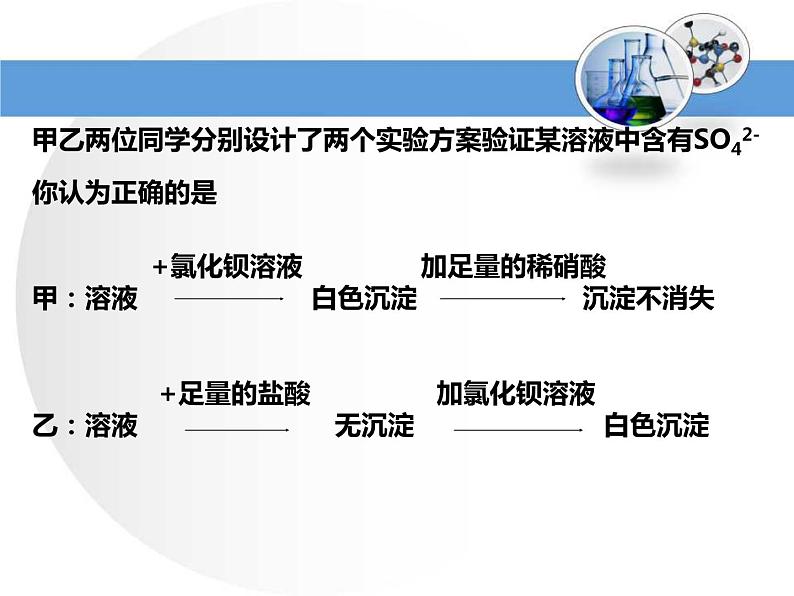
甲乙两位同学分别设计了两个实验方案验证某溶液中含有SO42-你认为正确的是 +氯化钡溶液 加足量的稀硝酸甲:溶液 白色沉淀 沉淀不消失 +足量的盐酸 加氯化钡溶液乙:溶液 无沉淀 白色沉淀
甲乙两位同学分别设计了两个实验方案验证某溶液中含有SO42-你认为正确的是 +氯化钡溶液 加足量的稀硝酸甲:溶液 白色沉淀 沉淀不消失 +足量的盐酸 加氯化钡溶液乙:溶液 无沉淀 白色沉淀
1.取样于试管中加入NaOH溶液,微热,有 气泡产生,
2.在试管口放一张湿润的红色石蕊试纸,湿润 的红色的石蕊试纸变蓝
铵盐(铵态氮肥)遇碱放出有刺激性气味的氨气。
氮肥中氨水是液态,碳酸氢铵有强烈的氨味,据此可直接将它们与其它氮肥相区别.
其它氮肥可按下列步骤鉴别:
如何鉴别 NH3.H2O、NH4HCO3、(NH4)2SO4、 NH4Cl、 NH4NO3、 CO(NH2)2 六种氮肥?
NH4Cl、 (NH4)2SO4、NH4NO3
加Ba(NO3)2溶液
NH4NO3 、NH4Cl
1.下列鉴别物质的方法中错误的是( )A.NH4NO3和NaOH固体:溶于水,比较温度变化 情况B.NH4NO3和(NH4)2SO4固体:加熟石灰混合研磨 后闻气味C.NH4Cl和尿素[CO(NH2)2]两种化肥:用熟石 灰粉末混合研磨闻气味D.磷矿粉[有效成分Ca3(PO4)2]和碳酸氢铵 (NH4HCO3):加水,搅拌,观察溶解情况
2.下列各组物质的溶液,不用其他试剂,只用观 察和组内物质相互混合的方法,不能将它们一 一鉴别的是( )A.HCl NaOH FeCl3 NaClB.H2SO4 NaCl Na2CO3 CaCl2C.NaNO3 HCl CaCl2 KOHD.MgCl2 KOH Cu(NO3)2 Na2SO4
3.下列实验方案正确的是( )A.制备:用加热KCl和MnO2混合物的方法制O2B.鉴别:用Na2CO3溶液鉴别稀盐酸、NaOH溶液和 Ba(OH)2溶液C.除杂:用溶解、蒸发的方法除去粗盐中的难 溶性杂质D.检验:用内壁涂有澄清石灰水的烧杯罩在甲 烷燃烧的火焰上方,检验有水生成
粗盐——————————氯化钠
除去不溶性杂质: 泥沙等除去可溶性杂质: MgCl2,CaCl2,Na2SO4等
不溶性杂质:泥沙等可溶性杂质:MgCl2,CaCl2,Na2SO4等
粗盐提纯(一) 除去不溶性杂质(泥沙等) (1)溶解 (2)过滤 (3)蒸发 (4)洗涤干燥
过滤---物质的分离和提纯 方法之一
1.适用于固体与液体混合物的分离。2.实验仪器:铁架台、烧杯、漏斗、 玻璃棒、滤纸
蒸发——物质的分离和提纯 方法之二
1.适用于分离溶于溶剂中的溶质。
2.主要仪器:蒸发皿、酒精灯、 玻璃棒,铁架台。
粗盐提纯(二)除去可溶性杂质 ( MgCl2,CaCl2,Na2SO4等)
除去可溶性杂质( CaCl2、MgCl2、 Na2SO4等)
思考:应选择加入什么试剂? (资料:一些物质的溶解性)
Na2SO4+BaCl2=BaSO4↓+2NaCl
MgCl2+2NaOH=Mg(OH)2↓+2NaCl
CaCl2+Na2CO3=CaCO3↓+2NaCl
用化学方法除杂时: 为了使杂质能除得比较干净,所加试剂一般要过量,试剂过量则又可能引入新杂质。为此要考虑加入试剂的顺序,即:要使前一过量试剂在后续除杂操作中除去。
Na2CO3+BaCl2=BaCO3↓+2NaCl
NaOH+HCl=NaCl+H2O
Na2CO3+2HCl=2NaCl+H2O+CO2 ↑
(3)BaCl2——Na2CO3——NaOH——过滤——稀盐酸
(1)BaCl2——NaOH——Na2CO3——过滤——稀盐酸
(2)NaOH——BaCl2——Na2CO3——过滤——稀盐酸
1、只要Na2CO3加在BaCl2之后, Na2CO3除去 CaCl2 和过量的BaCl2 。 2、过滤之后再加入稀盐酸。
可能的除杂方案(加入的试剂顺序)
除去难溶性杂质(泥沙等) 和可溶性杂质 (Ca2+ ,Mg2+, SO42-)的方法与步骤
1、取样、溶解;2、加入过量的BaCl2溶液 ,除去SO42- 。3、加入过量的NaOH溶液,除去Mg2+ 。
除去难溶性杂质(泥沙等)和可溶性杂质 (Ca2+ ,Mg2+, SO42-)的方法与步骤
4、加入过量的Na2CO3溶液,除去Ca2+ ,Ba2+ 。5、将第4步中的混合液过滤,向滤液中加入稍过 量的稀HCl,除去CO32-和OH-,用PH试纸调试。6、加热蒸发。
物质的提纯:把混合物中的杂质除去得到 纯净物的过程。
(1)不增——不能增加新杂质;
(2)不减——不减少被提纯的物质;
(3)易分离——被提纯的物质与杂质容易分离
除去杂质的步骤(固体):
(若试剂不只一种,要考虑试剂的加入顺序)
溶解——加入除杂试剂——过滤——蒸发。
物质提纯方法 一. 物理方法: (1)过滤法:用于可溶性物质和不溶性物质的分离。
(2)结晶法:
溶解度受温度影响不大的固体用蒸发结晶(如氯化钠等);
溶解度受温度升高而增大的固体用降温结晶法(如硝酸钾等);
物质提纯方法一. 物理方法:
(3)蒸馏与分馏:它是利用几种互溶的液体各自沸 点差别较大的性质来分离物质的 一种方法。如从石油中分离各种 馏分,再如C2H5OH和H2O混合物的分离.
(4)吸附(如活性炭、木炭等物质的吸附作用);
(5)干燥(浓硫酸、氢氧化钠等物质干燥气体)。
物质提纯方法二. 化学方法: 加入化学试剂,让杂质转化为 被提纯的物质 , 或转化为 沉淀、气体 或 水 除去。
注意:为了使杂质能除得比较干净,所加试剂 一般要过量,试剂过量则又可能引入新 的杂质.为此要设计加入试剂的顺序,即: 要使前一过量试剂在后续除杂操作中除去。
1.粗盐中含有少量的MgCl2、CaCl2、Na2SO4等杂质, 为了将杂质除干净,先向粗盐溶液中分别加入 过量的①NaOH、②Na2CO3、③BaCl2溶液,过滤, 再加入④稀盐酸 使溶液的pH=7,将最后所得溶 液进行蒸发可得到精盐,加入溶液的先后顺序 错误的是( )
A.②③①④ B.③②①④
C.①③②④ D.③①②④
3. 除去下列物质或溶液中杂质(括号内为杂质) 的方法,合理可行的是( ) A.氧化钙(碳酸钙) 加水、过滤 B.碳酸钾(氢氧化钾) 通入足量二氧化碳气体 C.硫酸(硫酸钠) 加入适量氯化钡试剂、过滤 D.氯化亚铁(氯化铜)加足量铁粉、过滤
初中化学人教版九年级下册第十一单元 盐 化肥课题2 化学肥料教课ppt课件: 这是一份初中化学人教版九年级下册第十一单元 盐 化肥课题2 化学肥料教课ppt课件,共9页。PPT课件主要包含了学习目标,学习重难点,强烈气味,白色晶体,灰白色粉末,有刺激性气味气体放出,无气体放出等内容,欢迎下载使用。
初中化学人教版九年级下册课题2 化学肥料教学演示ppt课件: 这是一份初中化学人教版九年级下册课题2 化学肥料教学演示ppt课件,共21页。PPT课件主要包含了说说看,教学目标,化学肥料,复合肥料,自主学习,常见的化肥,常见的氮肥,知识积累,常见的磷肥,混合物等内容,欢迎下载使用。
人教版九年级下册课题2 化学肥料评优课ppt课件: 这是一份人教版九年级下册课题2 化学肥料评优课ppt课件,文件包含课题2化学肥料课件pptx、课题2化学肥料导学案doc、课题2化学肥料教案doc、常用化肥的简易鉴别mp4等4份课件配套教学资源,其中PPT共41页, 欢迎下载使用。













