
2022秦皇岛青龙满族自治县一中高三上学期周测四化学试题缺答案
展开
这是一份2022秦皇岛青龙满族自治县一中高三上学期周测四化学试题缺答案,共7页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
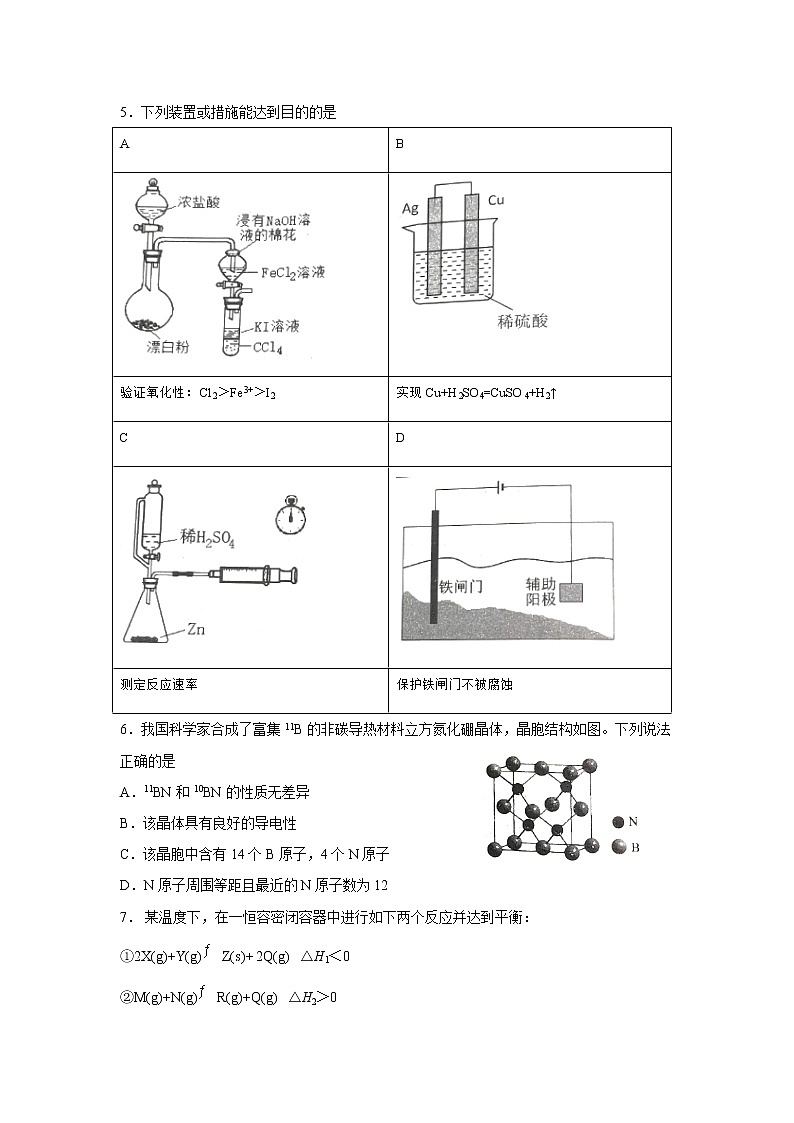
化学试卷一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项符合题目要求。1.下列说法正确的是A.丝绸、宣纸及尼龙的主要成分均为合成纤维B.港珠澳大桥使用的超高分子量聚乙烯纤维吊装缆绳,具有质量轻、强度大、耐磨、耐腐蚀的优点C. “嫦娥五号”使用的太阳能电池阵和锂离子电池组,均可将化学能转变成电能D.“奋斗者号”潜水器使用的固体浮力材料,由空心玻璃微球填充高强树脂制成,属于无机非金属材料2.我国自主设计生产的长征系列运载火箭使用偏甲肼(C2H8N2)作燃料,N2O4作氧化剂。下列相关的化学用语正确的是A.该反应的化学方程式:C2H8N2+N2O4=2CO2+N2+4H2OB.偏二甲肼的结构简式:C.N2的结构式:N=N D.甲基的电子式:3.短周期元素X、 Y、Z、M原子序数依次增大,Z的基态原子2p轨道半充满,M的最高正价与最低负价绝对值之差为4,它们组成的一种分子结构如图。下列说法正确的是A.电负性:X>Y>ZB.原子半径:Y>Z>XC.分子中Z原子的杂化方式均为sp2D.Y、Z、M的最高价氧化物的水化物均为强酸 4.下列说法错误的是A.CH4分子球棍模型: B.基态Si原子价电子排布图:C.第一电离能:N>O>C D.石墨质软的原因是其层间作用力微弱5.下列装置或措施能达到目的的是AB验证氧化性:Cl2>Fe3+>I2实现Cu+H2SO4=CuSO4+H2↑CD测定反应速率保护铁闸门不被腐蚀6.我国科学家合成了富集11B的非碳导热材料立方氮化硼晶体,晶胞结构如图。下列说法正确的是A.11BN 和10BN的性质无差异B.该晶体具有良好的导电性C.该晶胞中含有14个B原子,4个N原子D.N原子周围等距且最近的N原子数为127. 某温度下,在一恒容密闭容器中进行如下两个反应并达到平衡:①2X(g)+Y(g)Z(s)+ 2Q(g) △H1<0②M(g)+N(g)R(g)+Q(g) △H2>0下列叙述错误的是A.加入适量Z,①和②平衡均不移动 B.通入稀有气体Ar,①平衡正向移动C.降温时无法判断Q浓度的增减 D.通入Y,则N的浓度增大8.中药透骨草中一种抗氧化性活性成分结构如下。下列说法正确的是A.在一定条件下能发生氧化反应、取代反应和消去反应B.苯环上的一溴代物共5种C.1 mol 该化合物最多与4 mol NaOH反应D.该分子中最多有7个碳原子共面9.在N-羟基邻苯二甲酰亚胺(NHPI)介质中,可实现醇向醛的转化,原理如图。下列说法错误的是A.理论上NHPI的总量在反应前后不变B.海绵Ni电极作阳极C.总反应为+ H2↑D.每消耗1 mmol苯甲醇,产生22.4 mL氢气10.下列各实验的现象及结论都正确的是选项实验现象结论A浓硫酸滴入蔗糖中,产生的气体导入澄清石灰水蔗糖变 黑、体积膨胀,澄清石灰水变浑浊浓硫酸具有脱水性和强氧化性B铜粉加入稀硫酸中,加热;再加入少量硝酸钾固体加热时无明显现象,加入硝酸钾后溶液变蓝硝酸钾起催化作用C过量铁粉加入稀硝酸中,充分反应后,滴加KSCN溶液有无色气泡产生, 溶液呈血红色稀硝酸能将Fe氧化成Fe3+D将Na粒投入MgCl2溶液析出银白色固体固体为Mg11.苯乙烯与溴苯在一定条件下发生Heck反应:+溴苯用量(mmol)100100100100100100100催化剂用量(mmol)2222222反应温度(℃)100100100100120140160反应时间(h)10121416141414产率(%)81.284.486.6 86.293.596.689.0根据上表数据,下列说法正确的是A.最佳反应温度为100 ℃ B.最佳反应时间为16hC.温度过高时催化剂活性可能降低 D.反应产物是顺式结构12.实验室用TiCl4水解法制备纳米TiO2的简易流程如下,下列说法错误的是A.TiCl4 发生水解反应,可生成TiO2·xH2OB.氨水的作用可用勒夏特列原理解释C.可用AgNO3溶液检验沉淀是否洗涤干净D.制得的TiO2纳米颗粒能产生丁达尔现象13.Hg-Hg2SO4标准电极常用于测定其它电极的电势,测知Hg-Hg2SO4电极的电势高于Cu电极的电势。以下说法正确的是A.K2SO4溶液可用CCl4代替B.Hg-Hg2SO4电极反应为Hg2SO4 -2e-=2Hg+C.若把Cu-CuSO4体系换作Zn-ZnSO4体系,电压表的示数变大D.微孔瓷片起到阻隔离子通过的作用14.下列说法正确的是A.向AgCl浊液中加入KBr溶液,沉淀颜色变为浅黄色,即可证明Ksp(AgCl)>Ksp(AgBr)B.常温下向NaOH溶液中滴入HCOOH溶液至pH=5时:c(HCOO-)>c(Na+)C.常温下等物质的量浓度的四种溶液①NH3·H2O ②NH4HSO4 ③(NH4)2CO3 ④NH4Cl,c()的关系为②>④>③>①D.等物质的量浓度的NaHCO3与Na2CO3混合溶液:3c(Na+)=2[c()+c()+c (H2CO3)]15.天然水体中的H2CO3与空气中的(CO2保持平衡。已知Ksp(CaCO3)=2.8×10-9, 某溶洞水体中lgc(X) (X为H2CO3、、或Ca2+) 与pH的关系如图所示。下列说法正确的是A.曲线①代表 B.H2CO3的一级电离常数为10-8.3C.c(Ca2+)随 pH升高而增大 D.pH=10.3 时,c(Ca2+)=2.8×10-7.9 mol·L-1二、非选择题:16.(14 分)高锰酸钾生产过程中产生的废锰渣(主要成分为MnO2、KOH、MgO和Fe2O3)可用于制备MnSO4晶体,工艺流程如下:该工艺条件下金属离子开始沉淀和完全沉淀的pH如下表所示:金属离子Fe3+Fe2+Mn2+Mg2+开始沉淀pH2.107.459.279.60完全沉淀pH3.208.9510.8711.13回答以下问题:(1) MnSO4中阴离子的空间构型为__________________。(2)提高“反应Ⅰ”速率可采取的措施是__________ (除“加热”外,任写一种),滤渣A的主要成分为___________(填化学式)。(3) “反应Ⅱ”中硫铁矿(FeS2)的作用为_________________。(4)“反应Ⅲ”的离子方程式为_________________________。(5)“调pH”步骤中,应调节pH不低于_______________。(6)取0.1510 g MnSO4固体,溶于适量水中,加硫酸酸化,用过量NaBiO3(难溶于水)将其完全氧化为,过滤,洗涤,洗涤液并入滤液后,加入0.5360 g Na2C2O4固体,充分反应后,用0.0320 mol/L KMnO4溶液滴定,用去20.00 mL,计算样品中MnSO4的质量分数_________(保留三位有效数字)。
相关试卷
这是一份河北省秦皇岛市青龙满族自治县部分学校2023-2024学年高三上学期10月联考化学试题(含答案),共15页。试卷主要包含了选择题,填空题等内容,欢迎下载使用。
这是一份2021邯郸大名县一中高二上学期第八周周测化学试题含答案
这是一份2021郑州一中高三上学期第三次周测化学试题PDF版含答案









