
2021-2022学年四川省成都市某校期中_(化学)试卷人教版
展开
这是一份2021-2022学年四川省成都市某校期中_(化学)试卷人教版,共8页。试卷主要包含了选择题,解答题等内容,欢迎下载使用。
1. 下列物品是用有机合成材料制作的是( )
A.塑料桶B.铅笔芯C.纯羊毛衫D.铝合金门窗
2. 下列做法与“爱成都·迎大运·提升环境质量”理念不相符的是( )
A.地铁公交出行B.建筑工地喷雾除尘
C.废气达标排放D.推广使用一次性餐具
3. 健康饮食、幸福生活,下列说法正确的是( )
A.蔬菜水果中富含维生素,缺乏维生素C,会引起坏血病
B.鱼肉含有蛋白质、脂肪等营养物质,可代替主食
C.高温可以灭菌,霉变的米饭蒸煮后可以继续食用
D.锌是人体所需微量元素,缺乏会引起贫血
4. 安全无小事,人人需谨慎。下列说法错误的是( )
A.炒菜时油锅着火,用锅盖盖灭
B.家用电器着火,用水浇灭
C.加热试管里的液体,液体体积不超过试管容积的1/3
D.浓硫酸沾到皮肤上,用大量水冲洗后涂碳酸氢钠溶液
5. 下列说法错误的是( )
A.硬水易产生水垢,可用肥皂水区别硬水和软水
B.利用洗洁精的乳化作用,可洗去餐具上的油污
C.蔗糖能无限制地溶解在一定量的水中
D.合理使用农药化肥,减少水体污染
6. 下列物质的用途主要由物理性质决定的是( )
A.氮气用于制作氮肥B.氧气用于医疗急救
C.生石灰用作干燥剂D.活性炭用于冰箱除味
7. 下列宏观事实对应的微观解释正确的是( )
A.水结成冰−−−分子停止运动
B.液化石油气压缩进钢瓶−−−分子体积变小
C.食盐溶液能导电−−−溶液中有自由移动的离子
D.NaOH、CaOH2溶液具有相似的化学性质−−−都含有氢元素和氧元素
8. 我国的5G通信芯片主要由氮化镓(GaN)材料制成。结合图示,下列说法正确的是( )
A.镓属于非金属元素
B.镓原子质量是69.72g
C.在化学反应中氮原子可得到电子形成N3−
D.GaN中镓元素和氮元素的质量比为31:7
9. 下列化学用语书写正确的是( )
A.硅元素:SIB.氧化铝:Al2O3
C.2个氦原子: He2D.3个铵根离子:3NH3+
10. 我国科学家成功实现了用CO2和CH4合成醋酸,反应过程如下图所示。相关说法正确的是( )
A.反应物、生成物均为有机物
B.反应前后保持不变的粒子是分子
C.CH4是天然气的主要成分,是最理想的清洁燃料
D.醋酸可使紫色石蕊溶液变成红色
11. 除去用海水晒制的粗盐中的难溶性杂质的实验有下图所示步骤。下列说法正确的是( )
A.实验操作步骤是①②③B.②中出现大量固体时停止加热
C.提纯后的盐为纯净物D.③中玻璃棒靠在单层滤纸处
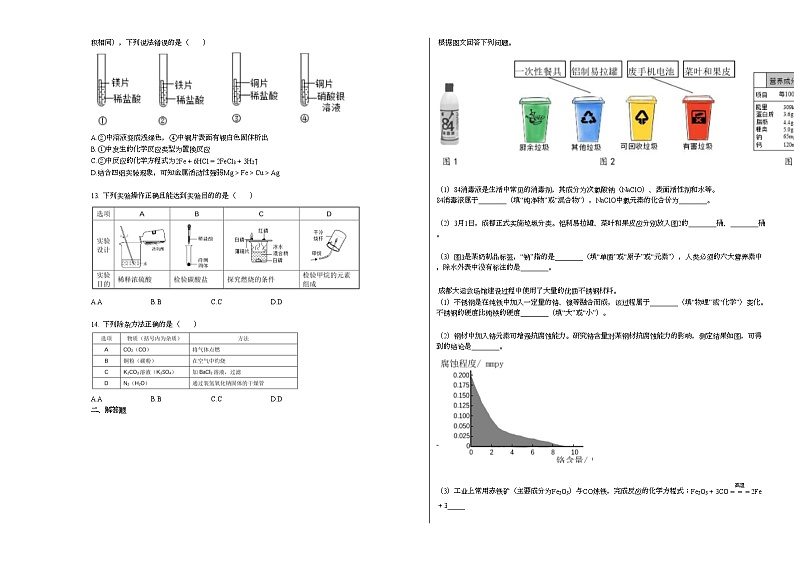
12. 小明设计如下实验探究铁、铜、镁、银的金属活动性(金属片均已打磨,形状大小相同,盐酸浓度和体积相同),下列说法错误的是( )
A.②中溶液变成浅绿色,④中铜片表面有银白色固体析出
B.①中发生的化学反应类型为置换反应
C.②中反应的化学方程式为2Fe+6HCl=2FeCl3+3H2↑
D.结合四组实验现象,可知金属活动性强弱Mg>Fe>Cu>Ag
13. 下列实验操作正确且能达到实验目的的是( )
A.AB.BC.CD.D
14. 下列除杂方法正确的是( )
A.AB.BC.CD.D
二、解答题
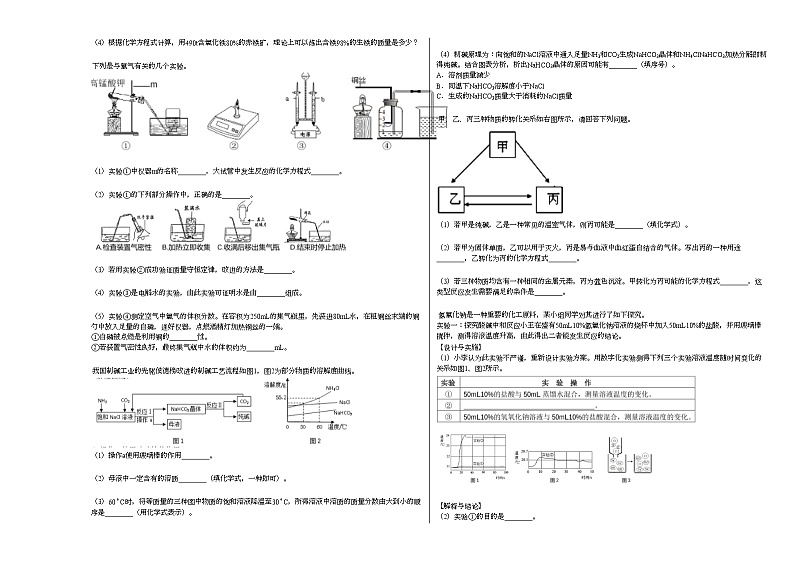
根据图文回答下列问题。
(1)84消毒液是生活中常见的消毒剂,其成分为次氯酸钠(NaClO)、表面活性剂和水等。
84消毒液属于________(填“纯净物”或“混合物”),NaClO中氯元素的化合价为________。
(2)3月1日,成都正式实施垃圾分类。铝制易拉罐、菜叶和果皮应分别放入图2的________桶、________桶。
(3)图3是某奶制品标签,“钠”指的是________(填“单质”或“原子”或“元素”),人类必须的六大营养素中,除水外表中没有标注的是________。
成都大运会场馆建设过程中使用了大量的优质不锈钢材料。
(1)不锈钢是在纯铁中加入一定量的铬、镍等融合而成,该过程属于________(填“物理”或“化学”)变化。不锈钢的硬度比纯铁的硬度________(填“大”或“小”)。
(2)钢材中加入铬元素可增强抗腐蚀能力。研究铬含量对某钢材抗腐蚀能力的影响,测定结果如图,可得到的结论是________。
(3)工业上常用赤铁矿(主要成分为Fe2O3)与CO炼铁,完成反应的化学方程式:Fe2O3+3CO===高温2Fe+3_____
(4)根据化学方程式计算,用490t含氧化铁80%的赤铁矿,理论上可以炼出含铁98%的生铁的质量是多少?
下列是与氧气有关的几个实验。
(1)实验①中仪器m的名称________,大试管中发生反应的化学方程式________。
(2)实验①的下列部分操作中,正确的是________。
(3)若用实验②成功验证质量守恒定律,改进的方法是________。
(4)实验③是电解水的实验,由此实验可证明水是由________组成。
(5)实验④测定空气中氧气的体积分数。在容积为250mL的集气瓶里,先装进80mL水,在粗铜丝末端的铜勺中放入足量的白磷,连好仪器,点燃酒精灯加热铜丝的一端。
①白磷被点燃是利用铜的________性。
②若装置气密性良好,最终集气瓶中水的体积约为________mL。
我国制碱工业的先驱侯德榜改进的制碱工艺流程如图1,图2为部分物质的溶解度曲线。
(1)操作a使用玻璃棒的作用________。
(2)母液中一定含有的溶质________(填化学式,一种即可)。
(3)60∘C时,将等质量的三种图中物质的饱和溶液降温至30∘C,所得溶液中溶质的质量分数由大到小的顺序是________(用化学式表示)。
(4)制碱原理为:向饱和的NaCl溶液中通入足量NH3和CO2生成NaHCO3晶体和NH4ClNaHCO3加热分解即制得纯碱。结合图表分析,析出NaHCO3晶体的原因可能有________(填序号)。
A.溶剂质量减少
B.同温下NaHCO3溶解度小于NaCl
C.生成的NaHCO3质量大于消耗的NaCl质量
甲、乙、丙三种物质的转化关系如右图所示,请回答下列问题。
(1)若甲是纯碱,乙是一种常见的温室气体,则丙可能是________(填化学式)。
(2)若甲为固体单质,乙可以用于灭火,丙是易与血液中血红蛋白结合的气体。写出丙的一种用途________,乙转化为丙的化学方程式________。
(3)若三种物质均含有一种相同的金属元素,丙为蓝色沉淀。甲转化为丙可能的化学方程式________,这类型反应发生需要满足的条件是________。
氢氧化钠是一种重要的化工原料,某小组同学对其进行了如下探究。
实验一:探究酸碱中和反应小王在盛有50mL10%氢氧化钠溶液的烧杯中加入50mL10%的盐酸,并用玻璃棒搅拌,测得溶液温度升高,由此得出二者能发生反应的结论。
【设计与实施】
(1)小李认为此实验不严谨,重新设计实验方案。用数字化实验测得下列三个实验溶液温度随时间变化的关系如图1、图2所示。
【解释与结论】
(2)实验①的目的是________。
(3)结合数据分析,确定酸碱中和反应放出热量的依据是________。
(4)结合图3从微观角度分析中和反应发生的实质________。
实验二:探究二氧化碳与氢氧化钠反应
【查阅资料】
①CaCl2溶液呈中性
②通常状况下,1体积水约能溶解1体积二氧化碳。
小组同学设计如图4实验(铁架台等仪器忽略)来进行探究。
(5)检查装置A的气密性的方法________。
(6)浓硫酸的作用________,B中发生反应的化学方程式________。
【实验操作与分析】
①连接装置,打开K1、K3、K5,关闭K2、K4。
②添加药品,当装置D中收集满CO2时,关闭K3、K3、K5,打开K2。将注射器中的NaOH溶液缓缓推入D中。
③充分反应后,关闭K2,打开K3、K4。风哨振动鸣叫,E中无色溶液倒吸入D中,D中产生沉淀且溶液显红色。
④关闭K4,打开K2、K5.将注射器活塞向上拉,F中溶液倒吸入D中。
(7)风哨振动鸣叫的原因________。步骤③“产生沉淀”的现象不足以证明CO2与NaOH发生了反应,理由是________。
(8)步骤④中,若观察到________(填现象),证明CO2与NaOH发生了反应。
【实验拓展】通过定量实验验证二氧化碳与氢氧化钠反应
用图5装置进行实验(实验前K1、K2、K3均关闭)。打开K1、K2,将A中液体推入B中,关闭K1待反应结束后,打开K3,将B中30mL气体推入C中,关闭K3。
(9)能证明C中反应发生,注射器活塞最终的位置可能是________(填序号)。
A.3mL处 B.20mL处 C.30mL处 D.33mL处
参考答案与试题解析
2021-2022学年四川省成都市某校期中 (化学)试卷
一、选择题
1.
【答案】
A
【考点】
合成材料的使用及其对人和环境的影响
三大合成材料
【解析】
此题暂无解析
【解答】
A
2.
【答案】
D
【考点】
化学与环境保护
【解析】
此题暂无解析
【解答】
D
3.
【答案】
A
【考点】
生命活动与六大营养素
营养素的食物来源
【解析】
此题暂无解析
【解答】
A
4.
【答案】
B
【考点】
实验室安全及常见意外事故的处理方法
【解析】
此题暂无解析
【解答】
B
5.
【答案】
C
【考点】
硬水与软水
乳化现象与乳化作用
水的性质和应用
【解析】
此题暂无解析
【解答】
C
6.
【答案】
D
【考点】
常见物质的性质与用途
【解析】
此题暂无解析
【解答】
D
7.
【答案】
C
【考点】
利用分子与原子的性质分析和解决问题
分子、原子、离子、元素与物质之间的关系
【解析】
此题暂无解析
【解答】
C
8.
【答案】
C
【考点】
元素周期表的特点及其应用
原子结构示意图与离子结构示意图
【解析】
此题暂无解析
【解答】
C
9.
【答案】
B
【考点】
化学符号及其周围数字的意义
【解析】
此题暂无解析
【解答】
B
10.
【答案】
D
【考点】
微粒观点及模型图的应用
【解析】
此题暂无解析
【解答】
D
11.
【答案】
B
【考点】
氯化钠与粗盐提纯
【解析】
此题暂无解析
【解答】
B
12.
【答案】
C
【考点】
金属活动性顺序及其应用
【解析】
此题暂无解析
【解答】
C
13.
【答案】
A
【考点】
实验方案的评价
【解析】
此题暂无解析
【解答】
A
14.
【答案】
D
【考点】
物质净化与除杂的综合应用
【解析】
此题暂无解析
【解答】
D
二、解答题
【答案】
(1)混合物,+1
(2)可回收垃圾,厨余垃圾
(3)元素,维生素
【考点】
纯净物和混合物的概念及判别
有关元素化合价的计算
化学与环境保护
生命活动与六大营养素
【解析】
此题暂无解析
【解答】
(1)混合物;+1
(2)可回收垃圾;厨余垃圾
(3)元素;维生素
【答案】
(1)物理,大
(2)铬含量在0−10%内,钢材抗腐蚀能力随着铬含量增高逐渐提高
(3)CO2
(4)解:理论上可以炼出含铁98%的生铁的质量是x
Fe2O3+3CO===高温2Fe+3CO2
160 2×56
490t×80% x×98%
1602×56=490t×80%x×98%
x=280t
答:理论上可以炼出含铁98%的生铁的质量280t。
【考点】
合金与合金的性质
化学变化和物理变化的判别
书写化学方程式、文字表达式
根据化学反应方程式的计算
【解析】
此题暂无解析
【解答】
(1)物理;大
(2)铬含量在0−10%内,钢材抗腐蚀能力随着铬含量增高逐渐提高
(3)CO2
(4)解:理论上可以炼出含铁98%的生铁的质量是x
Fe2O3+3CO===高温2Fe+3CO2
160 2×56
490t×80% x×98%
1602×56=490t×80%x×98%
x=280t
答:理论上可以炼出含铁98%的生铁的质量280t。
【答案】
(1)铁架台,2KMnO4====△K2MnO4+MnO2+O2↑
(2)A
(3)用集气瓶罩住燃着的蜡烛
(4)氢元素和氧元素
(5)①导热,②115.7
【考点】
书写化学方程式、文字表达式
氧气的实验室制取
实验方案的评价
质量守恒定律及其应用
电解水实验
测定空气里氧气含量的探究
【解析】
此题暂无解析
【解答】
(1)铁架台;2KMnO4====△K2MnO4+MnO2+O2↑
(2)A
(3)用集气瓶罩住燃着的蜡烛
(4)氢元素和氧元素
(5)①导热;②115.7
【答案】
(1)引流
(2)NaHCO3或NH4Cl
(3)NH4Cl>NaCl>NaHCO3
(4)ABC
【考点】
过滤的原理、方法及其应用
固体溶解度的影响因素
【解析】
此题暂无解析
【解答】
(1)引流
(2)NaHCO3或NH4Cl
(3)NH4Cl>NaCl>NaHCO3
(4)ABC
【答案】
(1)CaCO3或NaHCO3
(2)冶炼金属,CO2+C====高温2CO
(3) CuSO4+2NaOH=CuOH2↓+Na2SO4,在水溶液中,有沉淀、气体或水生成
【考点】
物质的鉴别、推断的综合应用
书写化学方程式、文字表达式
复分解反应及其应用
【解析】
此题暂无解析
【解答】
(1)CaCO3或NaHCO3
(2)冶炼金属;CO2+C====高温2CO
(3) CuSO4+2NaOH=CuOH2↓+Na2SO4;在水溶液中,有沉淀、气体或水生成
【答案】
(1)50mL10%的氢氧化钠溶液与50mL蒸馏水混合,测量溶液温度的变化
(2)作对照实验,测量稀释盐酸溶液温度的变化
(3)盐酸、氢氧化钠溶液混合时温度变化远大于稀释盐酸和氢氧化钠溶液温度变化
(4)H+和OH−反应生成水
(5)关闭K1,在A中加水浸过长颈漏斗的最下端,并形成一段水柱,静置一段时间后,观察水柱液面是否下降
(6)干燥二氧化碳或吸水 ,NaHCO3+HCl=NaCl+H2O+CO2↑
(7)D中二氧化碳和氢氧化钠反应导致气压减小,小于外界大气压,空气进入E中,氯化钙也可以与氢氧化钠反应生成氢氧化钙沉淀和氯化钠(或用化学方程式加文字说明)
(8)D中有气泡产生
(9)AB
【考点】
中和反应及其应用
实验方案的评价
检查装置的气密性
检验二氧化碳气体与氢氧化钠是否反应的方法
书写化学方程式、文字表达式
实验现象分析
【解析】
此题暂无解析
【解答】
(1)50mL10%的氢氧化钠溶液与50mL蒸馏水混合,测量溶液温度的变化
(2)作对照实验,测量稀释盐酸溶液温度的变化
(3)盐酸、氢氧化钠溶液混合时温度变化远大于稀释盐酸和氢氧化钠溶液温度变化
(4)H+和OH−反应生成水
(5)关闭K1,在A中加水浸过长颈漏斗的最下端,并形成一段水柱,静置一段时间后,观察水柱液面是否下降
(6)干燥二氧化碳或吸水;NaHCO3+HCl=NaCl+H2O+CO2↑
(7)D中二氧化碳和氢氧化钠反应导致气压减小,小于外界大气压,空气进入E中;氯化钙也可以与氢氧化钠反应生成氢氧化钙沉淀和氯化钠(或用化学方程式加文字说明)
(8)D中有气泡产生
(9)AB
相关试卷
这是一份2021-2022学年湖南株洲市某校九年级期中检测_(化学)试卷人教版,共11页。试卷主要包含了选择题,多选题,解答题等内容,欢迎下载使用。
这是一份2021-2022学年湖南省永州市某校九年级期中考试_(化学)试卷人教版,共10页。试卷主要包含了选择题,解答题等内容,欢迎下载使用。
这是一份2020-2021学年湖南省岳阳市某校2021年某校期中考试_九年级_(化学)试卷人教版,共10页。试卷主要包含了选择题,解答题等内容,欢迎下载使用。









