




高中化学人教版 (2019)必修 第一册实验活动1 配制一定物质的量浓度的溶液多媒体教学课件ppt
展开质量分数9%的氯化钠溶液可作生理盐水。
在初中,同学们学过了配制一定溶质质量分数的溶液,如何配制100g质量分数 9%的NaCl溶液?
托盘天平、烧杯、量筒、玻璃棒
计算→称量→量取→溶解→装瓶
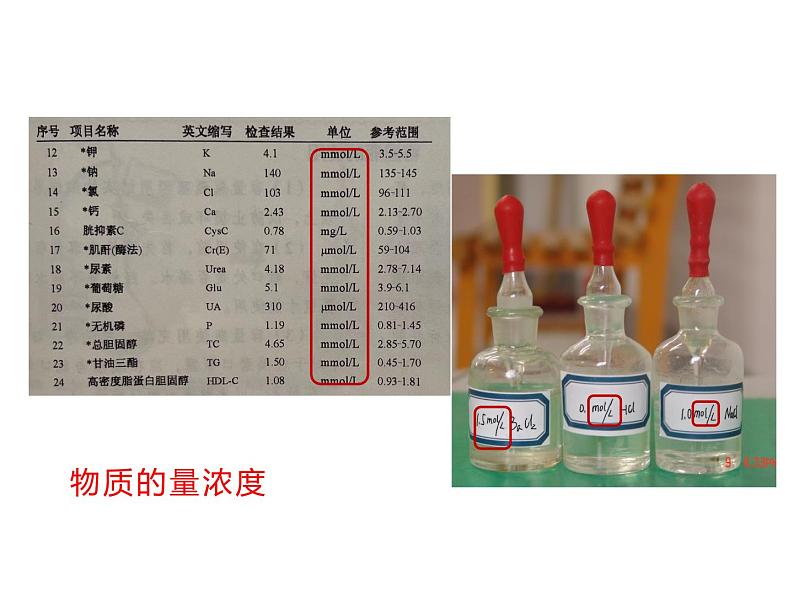
ml/L(或 ml·L-1)
单位体积溶液中所含溶质的物质的量.
1.将3ml的NaOH溶于水中配成5L溶液,求该溶液中NaOH的物质的量浓度
2、将 4gNaOH 固体溶于水配成 50mL 溶液,则NaOH 溶液的物质的量浓度为( )A.2ml/L B.1ml/L C. 0.1ml/L D. 0.05ml/L
将浓硫酸稀释使用,如要配制100mL,2ml/L的稀硫酸溶液,需要18.4ml/L浓硫酸的体积是多少?
稀释前后溶质的物质的量不变:
18.4ml/L×V1= 2ml/L×100mL
C浓V浓= C稀V稀
质量分数与物质的量浓度之间的换算
例:浓硫酸中溶质的质量分数为98%,密度为1.84g/cm3。则该浓硫酸中的物质的量浓度是多少?
= 18.4(ml/L)
任务:配置 100mL 1.00ml·L-1的 NaCl溶液,如何配制?
活动二:学会配制一定物质的量浓度的溶液
思考:我们从任务中可以得到哪些信息? 溶质是什么? 溶剂是什么? 100ml指的是什么?
1.当溶液的凹液面与刻度线相切时,容量瓶中溶液的体积即为容量瓶上所标识的体积。
容量瓶常用规格:50mL , 100mL,250mL, 500mL,1000mL
不能在容量瓶中进行溶解稀释等实验操作,也不能长期存放溶液,室温溶液才能转移入容量瓶
选容量瓶——“大而近”原则 ;例:1.配制80mL的溶液 2.配制180mL的溶液
配制100 mL 1.00 ml·L-1 氯化钠溶液
仪器:
注意:玻璃棒搅拌;要冷却至室温
仪器:
注意:玻璃棒引流
准备:选容量瓶,并检漏
1. 用蒸馏水洗涤玻璃棒和烧杯内壁 2~3次
将洗涤液都注入容量瓶中
轻轻摇动容量瓶使溶液混合均匀
2. 将蒸馏水注入容量瓶至液面离刻度线
改用加 滴蒸馏水至凹液面与刻度线相切
3. 塞好瓶塞,反复上下颠倒,摇匀
活动:溶液的配制误差分析
俯视或仰视容量瓶刻度线对溶液浓度的影响
砸 蛋 做 题
1、 用3mlNaOH配成2L溶液,NaOH的物质的量浓度为( )。
配制溶液时,试剂瓶刚用蒸馏水洗过,会使配制的溶液浓度偏低还是偏高?
某实验中共需要480mL0.5ml·L-1 NaCl的溶液,实验中应该准确称量 gNaCl。
高中人教版 (2019)实验活动1 配制一定物质的量浓度的溶液教课课件ppt: 这是一份高中人教版 (2019)实验活动1 配制一定物质的量浓度的溶液教课课件ppt,共10页。PPT课件主要包含了玻璃棒,冷却至室温,胶头滴管,凹液面与刻度线相切,无影响等内容,欢迎下载使用。
高中化学人教版 (2019)必修 第一册第二章 海水中的重要元素——钠和氯实验活动1 配制一定物质的量浓度的溶液授课ppt课件: 这是一份高中化学人教版 (2019)必修 第一册第二章 海水中的重要元素——钠和氯实验活动1 配制一定物质的量浓度的溶液授课ppt课件,共23页。
人教版 (2019)必修 第一册实验活动1 配制一定物质的量浓度的溶液教学课件ppt: 这是一份人教版 (2019)必修 第一册实验活动1 配制一定物质的量浓度的溶液教学课件ppt,共20页。PPT课件主要包含了自主预习·新知导学,合作探究·释疑解惑等内容,欢迎下载使用。














