

初中化学人教版九年级上册课题2 二氧化碳制取的研究背景图ppt课件
展开实验室制取CO2的思路和装置
石蜡+氧气 二氧化碳+水
不能;制得气体可能不纯
能否用于实验室里制取二氧化碳及理由
列举你所知道的能生成二氧化碳的反应,与同学讨论这些反应能否用于在实验室里制取二氧化碳,并说明理由?
科学家研究发现:凡是含碳酸根离子(CO32-)的化合物都能与稀盐酸(HCl)或稀硫酸 (H2SO4)等在常温下反应生成CO2气体。 生产生活中常见的石灰石、大理石、蛋壳、贝壳、水垢等其主要成分都是碳酸钙(CaCO3),纯碱是碳酸钠(Na2CO3),小苏打是碳酸氢钠(NaHCO3)
实验室制二氧化碳的理想原料
可供选择的原料有:石灰石(主要成分CaCO3)碳酸钠粉末(Na2CO3)稀盐酸(有效成分HCl)稀硫酸(有效成分H2SO4)
注意事项:(1)注意仪器的使用和药品的取用(2)重点比较反应速率的快慢
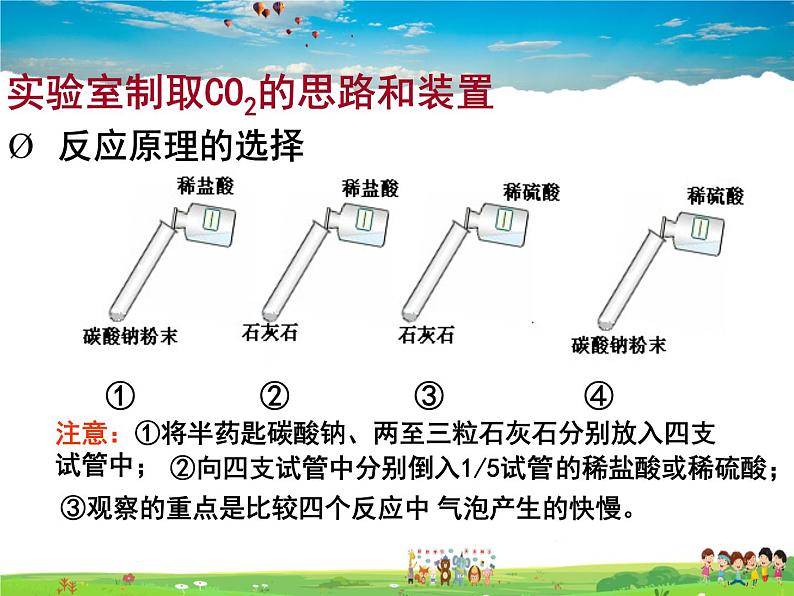
① ② ③ ④
注意:①将半药匙碳酸钠、两至三粒石灰石分别放入四支试管中;
③观察的重点是比较四个反应中
②向四支试管中分别倒入1/5试管
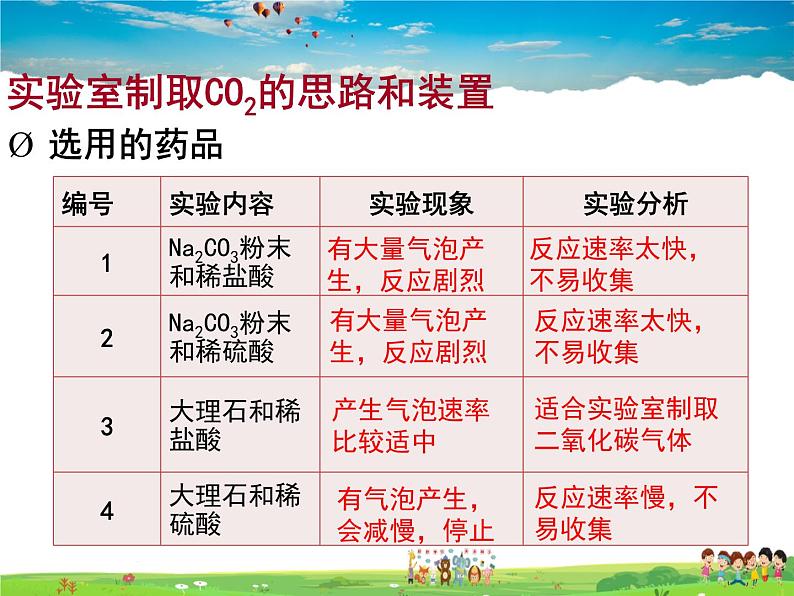
有大量气泡产生,反应剧烈
反应速率太快,不易收集
产生气泡速率比较适中
适合实验室制取二氧化碳气体
有气泡产生,会减慢,停止
反应速率慢,不易收集
实验室制取二氧化碳的反应原理
CaCO3+2HCl=CaCl2+H2CO3
H2CO3=H2O+CO2↑
CaCO3+2HCl = CaCl2+
稀硫酸与大理石(或石灰石)反应
刚开始有大量气泡产生,一时间后,气泡逐渐减少 ,反应逐渐停止。
虽然该反应能生成二氧化碳:CaCO3+H2SO4==CaSO4+H2O+CO2但生成的CaSO4微溶于水,覆盖在大理石表面,形成一层薄膜,使大理石与酸不能接触,反应难以进行。
实验室制取二氧化碳能不能用稀硫酸代替稀盐酸
稀盐酸与碳酸钠粉未反应
反应非常剧烈,短时间产生大量气泡
碳酸钠粉未的表面积很大,与盐酸接触面积大,反应速度很快,不易控制
实验室不能用碳酸钠粉未或大理石粉未等粉未状物质制取二氧化碳
该反应的化学方程式为:
Na2CO3+2HCl=2NaCl+H2O+CO2
实验室制取二氧化碳能不能用浓盐酸代替稀盐酸?
不能。因为浓盐酸有强烈的挥发性,会挥发出氯化氢气体,使制得的二氧化碳不纯。
反应条件(是否需要加热、加催化剂等)
密度比空气的大——向上排空气法
密度比空气的小——向下排空气法
排水法(不易溶于水、不与水发生反应)
实验室制取气体的装置由哪几部分组成?
两部分装置:一、发生装置二、收集装置
发生装置的确定需考虑的因素:1.反应物的状态(如液态、固态)2.反应条件(如加热,不加热)
反应物有两种(固体+液体)且不需加热
收集气体一般有两种:排空气法(1)向上排空气法(2)向下排空气法排水法
确定收集装置时主要应以两个物理性质方面去考虑
(1)气体的密度与空气密度比较(2)气体在水中的溶解性
空气的平均相对分子质量为29。如果某气体的相对分子质量大于29,则这种气体的密度比空气的密度大;如果小于29,则这种气体的密度比空气的密度小。
●确定二氧化碳气体发生装置应考虑的因素?
●确定二氧化碳气体收集装置应考虑的因素?
实验室制取二氧化碳的几种简易装置:
注意事项:长颈漏斗必须液封导管应在橡皮塞下少许导管应接近集气瓶底部
防止气体从长颈漏斗口逸出
能充分排走集气瓶中的空气
实验室制取二氧化碳的装置
导气管不能伸入液面以下
装置气密性的检查方法:
2.从长颈漏斗向锥形瓶中加水,至水面没过长颈漏斗下端;
3.一段时间后若长颈漏斗中液面不再下降,说明装置气密性良好。
实验室制取二氧化碳 操作步骤
检查气密性 ②
加大理石 ③
加稀盐酸 ④
关于收集较纯的二氧化碳的处理
CO2的验证方法和验满方法
你能不能设计一套装置来随时控制反应的发生和停止呢?
药品:大理石或石灰石、稀盐酸
原理:CaCO3 + 2HCl == CaCl2 + H2O + CO2 ↑
操作步骤:检查装置气密性、装药品、收集气体
检验: 将气体通入澄清石灰水,石灰水变浑浊
验满:将燃着木条 放在集气瓶口,若木条熄灭, 则集满。
以下是设计的部份发生装置,试分析各有什么优点。
BC可以随时添加液体药品
DEF可控制反应的速率
GHIJ可以使反应随时发生,随时停止
(1)长颈漏斗下端管口没有伸入液面下;会导致CO2从长颈漏斗逸出。(长颈漏斗下端管口应伸入液面以下)
(2)出气导管管口不应伸入液面下;这样CO2会把酸液压出,无法收集到CO2 。(出气导管口应略露出胶塞)
(3)不应用向下排空气法收集CO2; 这样CO2会从瓶口逸出。(应改用直形导管并用向上排空气法收集)
CaCO3+2HCl==CaCl2+H2O+CO2↑
初中化学人教版九年级上册课题2 二氧化碳制取的研究备课ppt课件: 这是一份初中化学人教版九年级上册课题2 二氧化碳制取的研究备课ppt课件,共18页。PPT课件主要包含了大理石或石灰石,不需要,向上排空气法,反应原理,实验装置,验证气体,反应条件,反应物状态,不需要加热,固体和液体等内容,欢迎下载使用。
初中化学人教版九年级上册课题2 二氧化碳制取的研究习题ppt课件: 这是一份初中化学人教版九年级上册课题2 二氧化碳制取的研究习题ppt课件,共22页。PPT课件主要包含了知识精讲,实验室制取二氧化碳,活动探究,大理石,石灰石,稀盐酸,向上排空气,澄清的石灰水,燃着的木条,立即熄灭等内容,欢迎下载使用。
化学九年级上册课题2 二氧化碳制取的研究精品ppt课件: 这是一份化学九年级上册课题2 二氧化碳制取的研究精品ppt课件,文件包含课题2《二氧化碳制取的研究》课件pptx、二氧化碳的实验室制取与性质mp4等2份课件配套教学资源,其中PPT共34页, 欢迎下载使用。